Un voyage à Sri Lanka : quelques observations floristiques et phytosociologiques
Title
A trip in Sri Lanka: some floristic and phytosociological observations
Résumé
Cet article relate et illustre la flore et la végétation rencontrées lors d’un séjour à Sri Lanka en janvier-février 2022. Deux associations originales sont décrites, l’Aponogetono natantis-Nymphoidetum hydrophyllae et le Berberido ceylanicae-Rhodomyrtetum tomentosae, ainsi qu’une alliance, l’Ipomoeo pedis–caprae-Sipinificion littorei.
Abstract
This article relates and illustrates the flora and vegetation encountered during a stay in Sri Lanka in January-February 2022. Two new associations are described, Aponogetono natantis-Nymphoidetum hydrophyllae and Berberido ceylanicae-Rhodomyrtetum tomentosae, as well as an alliance, Ipomoeo pedis-caprae-Spinificion littorei.
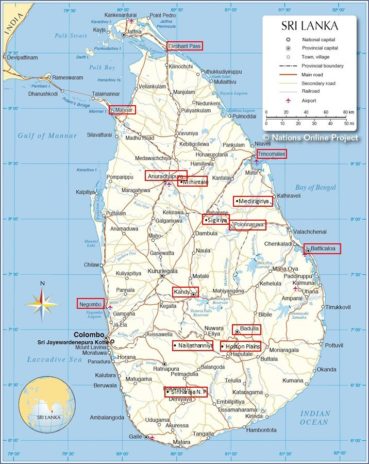
Du 14 janvier au 11 février 2022, un voyage à Sri Lanka (terme utilisé ici sans article, comme Sumatra, Madagascar…, au contraire de la Corse, la Sardaigne…) a donné lieu à des observations floristiques, phytosociologiques et ethnologiques. Ces dernières seront reprises dans un autre article en préparation, les premières faisant l’objet de la présente contribution. La carte 1 précise les principales localités ayant donné lieu à de telles observations et citées dans le texte qui suit.
D’une superficie de 65 610 km², cette île prolonge l’Inde vers le sud-est ; elle s’en est détachée à la fin du Miocène. On peut distinguer une partie méridionale plus montagneuse, pour un sixième de la superficie totale, à une altitude moyenne de 1 400 à 1 600 m ; le climat humide y favorise développement de belles forêts tropicales humides, en partie détruites pour laisser place aux plantations de thé introduites par les Britanniques dans la seconde moitié du xixe siècle, un certain Thomas Lipton les ayant développées. Les basses terres ont une altitude moyenne de 300 m, c’est là que s’étendent les sites historiques, la plupart inscrits au Patrimoine mondial de l’humanité par l’UNESCO.
Les déterminations botaniques ont été facilitées par la consultation de Flora of Sri Lanka (www.floraofsrilanka.com), malheureusement assez incomplet et dépourvu de clés, puis de Flora of India (www.efloraofindia.com), mais cela n’a pas toujours suffi pour aller jusqu’au niveau de l’espèce, parfois même du genre. La nomenclature des taxons suit Catalogue of life (www.catalogueoflife.org). Les noms de deux taxons voisins mais non séparés seront reliés par le signe /.
1. Des associations déjà connues
Tout d’abord, les observations réalisées permettent d’étendre à cette île l’aire de deux associations décrites d’autres régions d’Asie du Sud-est, à savoir le Calotropido giganteae-Ricinetum communis B. Foucault in B. Foucault & J.-M. Royer 2016 (de Foucault & Royer, 2016), association arbustive des zones rudéralisées en plaines plutôt sèches (photo 1), et le Peperomio pellucidae-Pileetum microphyllae B. Foucault 2014 (de Foucault, 2014), microphorbiaie colonisant les murs humides à suintants dans une grande partie des zones tropicales (photo 2). Dans les zones montagneuses de l’île, donc sous climat plus tempéré, le Calotropido giganteae-Ricinetum communis est remplacé par un fourré lui-même rudéral marqué par Tithonia diversifolia (photo 3), Solanum mauritianum, Brugmansia suaveolens, Ricinus communis, Calliandra calothyrsus, Lantana camara, Sambucus javanica, Chromolaena odorata, qui rappelle assez le Calliandro calothyrsi-Sambucetum javanicae B. Foucault in B. Foucault & J.-M. Royer 2016 d’Indonésie (de Foucault & Royer, 2016), lequel se range dans le Leucaeno leucocephalae-Ricinion communis B. Foucault 2020.
2. La végétation des plages
Plusieurs plages ont été parcourues à la recherche d’une végétation quelque peu naturelle tant elles sont polluées par divers déchets (plastiques, déjections…) et influencées par de multiples activités humaines.
Sur la côte orientale, à Trincomalee, on a réalisé plusieurs relevés ; malheureusement plusieurs taxons paraissant caractéristiques, dont une Acanthaceae (photo 4), n’ont pu être déterminés plus bas que le rang famille. En témoigne le relevé suivant :
Trincomalee, au sud des Golden Beach Cottages, approximativement N 08° 36’ 15,8’’, E 81° 13’ 14,7’’, 30 m², 75 %, 28 janvier 2022, 12 taxons, photo 6
- combinaison caractéristique : Ipomoea pes-caprae 5, Vigna marina 2 (photo 5), Amaryllidaceae (un Hymenocallis naturalisé ?) 2, Canavalia rosea 1, Acanthaceae 1, Spinifex littoreus 1,
- autres taxons : Pedalium murex 2, Tridax procumbens 1, Aerva javanica 1, Calotropis gigantea j +, Vitex sp. j 2, Scaevola taccada j +.
Ces limites taxonomiques ne permettent évidemment pas de définir ici une nouvelle association.
À Mannar, la végétation de plage est assez différente de la précédente : au sud-est de Keei Beach
(N 08° 58’ 37,6’’, E 79° 52’ 37,7’’), elle est surtout constituée de Ipomoea pes-caprae, Spinifex littoreus, Vigna marina, Rubiaceae, Salvadora persica j couché sur le sable, Pergularia daemia (photo 7).
Enfin, à Negombo (ouest de l’île), elle est encore différente des deux précédentes :
au droit du Sherry Land, N 07° 14’ 26,5’’, E 79° 50’ 27,9’’, 10 février 2022, 9 taxons
- combinaison caractéristique : Ipomoea pes-caprae 4, Hydrophylax maritima 2 (photo 8), Cyperaceae 2, Fabaceae (non Vigna marina) 1, Rubiaceae 1,
- autres taxons : Tridax procumbens 2, Pedalium murex +, Boerhavia diffusa +, Lantana camara j +.
Dans toutes ces observations, la rudéralisation de la végétation dunaire est perceptible à travers la présence de Tridax procumbens, Pedalium murex, Passiflora foetida, des Boerhavia…
S’il n’est guère possible de définir ici des associations, avec Spinifex littoreus (photo 9) cette végétation rappelle celle qui a été décrite des plages de Thaïlande méridionale sous le nom de Spinifici littorei-Viticetum litoralis B. Foucault 1994 ex 2019 (de Foucault, 1994, 2019). On peut dès lors reconnaître au moins une alliance originale, l’Ipomoeo pedis-caprae-Spinificion littorei all. nov. hoc loco, typus nominis hoc loco : Spinifici littorei-Viticetum litoralis B. Foucault 1994 ex 2019 (J. Bot. Soc. Bot. France 86 : 98), rassemblant des végétations paucispécifiques de plages paléotropicales caractérisées par Spinifex littoreus, Ipomoea pes-caprae, Vigna marina, Canavalia rosea. Cette alliance apparaît vicariante tropicale du Spinifici sericei-Ficinion nodosae B. Foucault 2022 décrit des côtes de régions australes moins tropicales (Nouvelle-Zélande, Tasmanie ; de Foucault, 2022). Il est probable que la végétation observée à Negombo s’y rattache aussi malgré la non-observation de S. littoreus en dépit de recherches assidues.
3. La végétation hydro- et hygrophile de plaine
Les grands sites historiques et les plaines de Sri Lanka hébergent souvent des mares ou des pièces d’eau colonisées par les hydrophytes. On peut séparer :
- des herbiers thérophytiques flottants à Utricularia gibba/aurea, Salvinia molesta, Azolla pinnata, Pistia stratiotes (photo 10) rappelant la végétation plus tempérée des Lemnetea minoris;
- des herbiers vivaces fixés à Nymphaea pubescens, Nymphoides hydrophylla (photo 11), Neptunia oleracea (photo 12), Aponogeton natans (photo 13), Myriophyllum verticillatum/spicatum.
La présence d’un Aponogeton est particulièrement intéressante d’un point de vue phytogéographique. À l’état spontané, la famille dont elle le seul genre est distribuée surtout en Afrique du Sud, Madagascar, Inde, sud-est de l’Asie et Australie, c’est donc une famille typiquement centre- et est-gondwanienne ; sa présence à Sri Lanka rappelle que l’Inde se rattache bien au Gondwana et que l’île s’est ultérieurement détachée de la péninsule indienne. Le relevé suivant décrit plus finement la végétation observée :
Polonnaruwa, approximativement N 07° 56’ 36’’, E 81° 00’ 47’’, 56 m, 30 m², 75 %, 22 janvier 2022, 5 taxons
Nymphaea pubescens 4, Nymphoides hydrophylla 3, Aponogeton natans 3, Neptunia oleracea 1, Myriophyllum verticillatum/spicatum 2,
typus nominis hoc loco de l’Aponogetono natantis-Nymphoidetum hydrophyllae ass. nov. hoc loco (photo 14).
Quelquefois, les sites historiques ont été installés dans des zones où affleurent des rochers plus ou moins inclinés. Dans l’un d’eux (Medirigiriya) a été observée une intéressante petite pelouse mésohygrophile dont l’étude (sous le regard interrogateur d’un Varanus bengalensis ; photo 15) a révélé la présence d’Eriocaulon subglaucum, Drosera burmannii, un Selaginella, Ophioglossum costatum, la gentianacée Hoppea fastigiata (photos 16 à 19). C’est une végétation globalement thérophytique qui relève de la S(Lythraceae-Gentianaceae), alors que la végétation vivace relève plutôt de la S(Xyridaceae-Eriocaulaceae). L’écologie de cet Ophioglosse est conforme à celle d’autres espèces du même genre, dont les trois présentes en France (sur tout ceci, voir de Foucault, 1988). C’est aussi le cas de mares temporaires californiennes ; une étude écologique de Bauder (2000) montre ainsi la différenciation entre
- un niveau topographique moyen où une communauté vivace à Ophioglossum californicum est reliée à une communauté thérophytique à Juncus bufonius, Lythrum hyssopifolia, Plantago elongata, Psilocarphus tenellus (Asteraceae), Navarretia hamata (Polemoniaceae),
- un niveau topographique inférieur où une communauté vivace à Isoetes orcuttii, Brodiaea orcuttii, Eleocharis macrostachya, Eryngium aristulatum parishii, Downingia cuspidata (Campanulaceae) est reliée à une communauté thérophytique à Deschampsia danthonioides, Lysimachia minima, Polypogon monspeliensis, Crassula aquatica, Psilocarphus brevissimus, Lilaea scilloides (Juncaginaceae).
Notamment, pour le niveau inférieur, on remarque les symétries floristiques familiales ou génériques avec d’autres mares temporaires connues en Europe (Isoetes, Eryngium, Crassulaceae, Campanulaceae). On ne peut que regretter que les botanistes et phytoécologues américains ne soient pas plus phytosociologues…
Hoppea est un genre riche d’une seconde espèce, H. dichotoma (photo 20), qui a été rencontrée associée à d’autres thérophytes (un Murdannia, Ammannia baccifera, une Lythraceae ; photos 21 et 22), dont la gentianacée Canscora heteroclita (rappelant un Centaurium, mais à fleurs zygomorphes ; photo 23), sur les sables plus ou moins salés et frais d’Elephant Pass, juste à l’entrée de la péninsule de Jaffna ; la végétation vivace combine Enicostema axillare, Synostemon bacciformis, Tecticornia indica, Aeluropus lagopoides (photos 24 à 27). Alors que celle-ci rappelle la végétation des Sarcocornietea fruticosae, la première rappelle plutôt celle des Saginetea maritimae. Sur les Gentianaceae des genres Hoppea et Canscora, voir Thiv (2003) ; à noter la présence de Canscora alata dans une pelouse herbeuse de Mihintale (photo 28), alors que C. diffusa fut observé au niveau de cascades au Togo vers la fin des années 1990.
4. La végétation d’altitude
La végétation d’altitude a surtout été parcourue au niveau du parc national d’Horton Plains, par ailleurs labellisé Patrimoine mondial de l’humanité (sous la dénomination française Hauts Plateaux du centre de Sri Lanka). Ce parc doit son nom au gouverneur britannique Sir Robert Wilmot Horton (1784-1841) et culmine à plus de 2 000 m. Cette végétation avait déjà été abordée lors d’un précédent voyage, en 2004, si bien que des photographies de ce premier séjour ont pu être ajoutées à notre iconothèque (scans de diapositives).
Le paysage (photo 29) est surtout marqué par les patanas (nom local des prairies) à Chrysopogon nodulibarbis, Cymbopogon nardus, Aristea ecklonii (taxon naturalisé originaire d’Afrique méridionale), Wahlenbergia marginata, des Helichrysum, Hedyotis plantaginifolia et, dans les thalvegs plus humides, le bambou Kuruna densifolia (photos 31 à 35). Cet ensemble est parcouru par des troupeaux de Rusa unicolor, un cervidé d’Asie méridionale et d’Australie (photo 30). D’après Green (1990), il y aurait aussi des mares oligotrophiles à Aponogeton jacobsenii, Isolepis fluitans et des Utricularia, des bas-marais à Juncus prismatocarpus, Garnotia mutica, des Eriocaulon, Drosera indica, des Exacum (photo 36)… La rencontre de Gaultheria leschenaultii (photo 37) incite à poser l’hypothèse de l’existence d’une lande à Ericaceae.
Lobelia leschenaultiana (photo 38) n’a pas été observé sur les sentiers parcourus ; ce taxon endémique des massifs d’Inde méridionale et de Sri Lanka est remarquable, car il rappelle par son architecture les Lobelia des montagnes d’Afrique orientale tels que L. telekii, L. rhynchopetalum, L. bequaertii, L. deckenii… Mais le taxon sri-lankais paraît plutôt à rapprocher de L. giberroa qui occupe des lisières (photo 39 ; voir aussi Jeannel, 1950, et Schnell, 1977 : 123). En outre, dans le parcours entre Nallathanniya et Kandy, un autre Lobelia a été observé dans des lisières de plus basse altitude, L. nicotianifolia ; ce dernier taxon n’appartient donc pas au groupe précédent, bien que selon Lammers (2011) tous ces taxons appartiennent à la même section Rhynchopetalum (Fresen.) Benth.
La végétation arbustive est marquée par Rhodomyrtus tomentosa, Berberis ceylanica, Gnidia glauca, Hypericum mysorense, Hedyotis ceylanica, Rubus leucocarpus (photos 41 à 45) et des formes juvéniles de Rhododendron arboreum. Plus précisément, voici un relevé réalisé le long de la boucle de World’s End partant de Farr Inn :
approximativement N 06° 47’ 38’’, E 80° 48’ 12’’, 2 145 m, le 16 janvier 2022, 7 taxons
- combinaison caractéristique : Rhodomyrtus tomentosa 3, Hedyotis ceylanica 2, Berberis ceylanica 1, Rubus leucocarpus 1, Hypericum mysorense +, Gnidia glauca +,
- autre taxon : Rhododendron arboreum j 3,
typus nominis hoc loco du Berberido ceylanicae-Rhodomyrtetum tomentosae ass. nov. hoc loco (photo 46).
Rhododendron arboreum optimal (photo 47) caractérise plutôt les boisements montagnards (rain forests ; photo 48) dominés en outre par Calophyllum walkeri, des Lauraceae (genres Litsea, Cinnamomum, Actinodaphne), des Myrtaceae (Syzygium rotundifolium, S. sclerophyllum), Magnolia nilagirica (photo 49) ; on pourrait y ajouter les Hortonia, genre endémique de la famille typiquement gondwanienne des Monimiaceae, non rencontrés à Horton Plains mais vus en 2004 lors de l’ascension d’Adam’s Peak qui culmine à 2 243 m (photo 50). Le sous-bois est dominé par des Strobilanthes, de petits bambous (Indocalamus, Ochlandra ; photo 51), des Impatiens, dont I. leptopoda (photo 52).
5. Quelques végétations à fougères
Dans les végétations diverses, on doit surtout signaler les rochers subverticaux riches en Adiantum longés lors de la visite de Duhinda Falls, près de Badulla ; au moins trois taxons de ce genre ont été distingués d’après leur morphologie, parfois associés à Mickelopteris cordata (photos 53 et 54). Par son écologie et sa composition floristique, cette végétation rappelle beaucoup celle des Adiantetea capilli-veneris (de Foucault, 2015).
On peut enfin évoquer les talus à fougères observés lors d’une randonnée à la réserve d’Udawattakele, à Kandy, avec notamment Tectaria zeilanica (photos 55 et 56). On étend ainsi à Sri Lanka ces végétations herbacées subverticales évoquées et illustrées dans une publication antérieure (de Foucault, 2020 : 86-87).
6. Conclusion
Ce voyage de 2022 a donc permis de visiter de hauts lieux du Patrimoine mondial naturel, mais aussi, d’un point de vue phytosociologique, de décrire deux associations végétales et une alliance nouvelles, et d’étendre à cette île deux associations (voire trois) antérieurement décrites. Ce compte-rendu a montré aussi que la limite de la description de la végétation est liée de près aux connaissances taxonomiques : le phytosociologue perçoit clairement les unités végétales élémentaires, cette perception ne dépendant pas de la connaissance de la flore comme on le pense ou l’écrit parfois, mais il ne pourra aller plus loin s’il n’a pas accès à la connaissance de cette flore.
Relativement à celui antérieur de 2004, ce voyage n’a pas donné lieu à un parcours dans le parc national de Sinharaja. En 2004, on y avait notamment rencontré Nepenthes distillatoria (photos 57 et 58), membre de la famille monogénérique des Nepenthaceae dont l’aire s’étend de Madagascar (avec N. masoalensis et N. madagascariensis ; photo 59) aux Seychelles (N. pervillei), à toute l’Asie du Sud-est, jusqu’à la Nouvelle-Calédonie (avec N. vieillardii ; photo 60).
Bibliographie
Bauder E.T., 2000. Inundation effects on small-scale plant distributions in San Diego, California vernal pools. Aquatic Ecology 34 (1) : 43-61.
Foucault B. (de), 1988. Les végétations herbacées basses amphibies : systémique, structuralisme, synsystématique. Dissertationes Botanicae 121 : 1-150.
Foucault B. (de), 1994. Notes analytiques et comparatives sur la végétation tropicale observée en Asie du Sud-Est. Bulletin de la Société de botanique du nord de la France 47 (2) : 29-39.
Foucault B. (de), 2014. Contribution au prodrome des végétations de France : les Parietarietea judaicae Rivas-Mart. in Rivas Goday 1964. Acta Botanica Gallica: Botany Letters 161 (4) : 403-427.
Foucault B. (de), 2015. Contribution au prodrome des végétations de France : les Adiantetea capilli-veneris Braun-Blanq. ex Braun-Blanq., Roussine & Nègre 1952. Acta Botanica Gallica: Botany Letters 162 (4) : 375-403.
Foucault B. (de), 2019. Errata et compléments à propos du Prodrome des végétations de France, sixième note. Journal de botanique de la Société botanique de France 86 : 93-102.
Foucault B. (de), 2020. Éloge du paradigme synusial : alternative à la classification phytosociologique de la végétation forestière européenne, ouest-asiatique et nord-africaine. Evaxiana 7 : 5-248.
Foucault B. (de), 2022. Validation de syntaxons invalidement publiés en 2021. Carnets botaniques 79 : 1-12, https://doi.org/10.34971/dxjk-t193.
Foucault B. (de) & Royer J.-M., 2016. Contribution au prodrome des végétations de France : les Rhamno catharticae-Prunetea spinosae Tüxen 1962. Documents phytosociologiques, 3e série, 2 : 150-343.
Green M.J.B., 1990. Sri Lanka: Horton Plains National Park. In IUCN Directory of South Asian protected areas, IUCN, Gland : 216-220.
Jeannel R., 1950. Hautes montagnes d’Afrique : vers les neiges éternelles sous l’équateur. Publications du Muséum national d’histoire naturelle, suppl. 1, 253 p.
Lammers T.G., 2011. Revision of the infrageneric classification of Lobelia L. (Campanulaceae: Lobelioideae). Annals of the Missouri Botanical Garden 98 : 37-62.
Schnell R., 1977. Flore et végétation de l’Afrique tropicale, 2. Gaulthier-Villars, Paris, 375 p.
Thiv M., 2003. A taxonomic revision of Canscora, Cracosna, Duplipetala, Hoppea, Microrphium, Phyllocyclus and Schinziella (Gentianaceae-Canscorinae). Blumea 48 : 1-46.
Remerciements
à M. Boudrie pour la détermination de Tectaria zeilanica, à lui-même et à Ch.-R. Fraser-Jenkins pour la confirmation d’Ophioglossum costatum, à J.-M. Tison pour l’article de T.G. Lammers sur le genre Lobelia et à P. Coulot pour la détermination de Vigna marina.