Redécouverte de Cephalaria syriaca (L.) Schrad. ex Roem. & Schult., 1818 (Caprifoliaceae) en France hexagonale
Title
Rediscovery of Cephalaria syriaca (L.) Schrad. ex Roem. & Schult., 1818 (Caprifoliaceae) in mainland France
Résumé
Quarante ans après sa dernière mention en France, Cephalaria syriaca a fait l’objet, depuis 2017, de plusieurs observations réparties sur différentes régions du territoire. Nous proposons ici une synthèse des données historiques et des observations récentes, ainsi qu’une discussion sur le statut de l’espèce. Cephalaria syriaca est actuellement protégée au niveau national. L’examen de la littérature indique toutefois qu’il s’agit d’une espèce néophyte, introduite relativement récemment (au début du xixᵉ siècle) en France et généralement instable dans ses stations historiques. Son association étroite avec le blé, notamment liée au mimétisme de ses semences, ainsi que sa présence dans des contextes riches en messicoles caractéristiques, conduisent toutefois à l’intégrer dans des démarches de conservation. Enfin, plusieurs observations récentes sont associées à des cultures de Fenugrec, qui semblent constituer un nouveau vecteur de diffusion de l’espèce en Italie et en France.
Abstract
Forty years after its last record in France, Cephalaria syriaca has been observed multiple times since 2017 across different regions of the country. Here, we provide a synthesis of historical data and recent observations, along with a discussion of the species’ status. Cephalaria syriaca is currently legally protected at the national level. However, a review of the literature indicates that it is a neophyte species, introduced relatively recently (in the early 19th century) in France, and generally unstable at its historical sites. Its close association with wheat, notably through seed mimicry, as well as its occurrence in habitats rich in characteristic arable weed species, nonetheless support its inclusion in conservation initiatives. Finally, several recent records are associated with fenugreek crops, which appear to constitute a new vector for the species’ dispersal in both Italy and France.
1. Introduction
Quarante ans après sa dernière mention en France – signalée en 1977 dans les Bouches-du-Rhône (Verlaque, 1980) – Cephalaria syriaca (L.) Schrad. ex Roem. & Schult. a fait l’objet, ces dernières années, de plusieurs observations presque simultanées dans l’ouest comme dans le midi de la France, et plus ponctuellement dans les Hauts-de-France. Espèce messicole rare et particulièrement fugace sur le territoire national, elle avait été intégrée à la liste des taxons protégés au niveau national lors du premier arrêté du 20 janvier 1982.
Après un rappel de sa position taxonomique et de sa description, nous examinerons le contexte de ces observations, tant anciennes que récentes, ainsi que l’évolution du statut de ce taxon.
2. Taxonomie et description
Le genre Cephalaria Schrad. comprend près d’une centaine d’espèces (Göktürk & Sümbül, 2014 ; POWO, 2025) dont la répartition s’étend de la région méditerranéenne jusqu’à l’Asie centrale, ainsi que de l’Afrique tropicale nord-orientale jusqu’à l’Afrique australe (POWO, 2025). Quatre espèces sont présentes en France : C. alpina (montagnarde et subalpine, Jura, Alpes, indigène), C. leucantha (eury-méditerranéenne, indigène), C. transylvanica (Provence orientale : archéophyte ?, Sud-Ouest : néophyte) et C. syriaca objet de cet article.
2.1. Description morphologique
La description qui suit synthétise celles données dans diverses flores consultées (Rouy & Foucaud, 1893-1913 ; Bonnier & Douin, 1912‑1935 ; Coste,1937 ; Bojňanský & Fargašová, 2007 ; Ghazanfar & Edmondson, 2013 ; Tison et al. 2014).
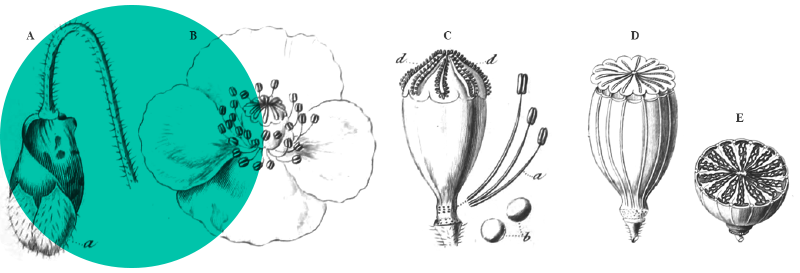
Cephalaria syriaca est une espèce annuelle de 20 à 80 cm de hauteur. La plantule présente des cotylédons ovales tronqués au sommet, avec une nervure centrale bien visible et des nervures secondaires réticulées (photo 1). Les tiges sont grêles, simples ou ramifiées, à poils rudes-hérissés (planche 1). Les feuilles sont pubescentes, oblongues à oblancéolées, simples, plus ou moins ciliées, les inférieures entières ou denticulées, les supérieures généralement entières et connées à la base (planche 1).
Les fleurs sont réunies en capitules ovoïdes, de 10 à 20 mm de long, portés par un pédoncule long, mince, sillonné et plus ou moins hérissé de soies, ou sessile dans les fourches des rameaux (planche 1). Les bractées de l’involucre sont longuement ovales ou largement triangulaires, les externes acuminées, de 8-12 × 2-5 mm, oblongues, les internes aristées, pubescentes. Les bractéoles de l’involucre mesurent 8-12 × 3-5 mm, sont oblongues, abruptement atténuées, aristées, pubescentes, ciliées sur les marges supérieures. Le calice est aristé, muni de soies de 1 à 1,5 mm de long et soyeux ou rarement pubescent. Les corolles, d’un bleu pâle ou lilas, sont soyeuses à l’extérieur, de 8 à 14 mm de long, à lobes de 3 à 5 mm de long.
Les semences sont des akènes ellipsoïdes avec un calice cupulé, un involucre poilu octogonal terminé par des épines apicales (quatre plus longues, quatre plus courtes ; planche 2). Leur surface est mate ou légèrement luisante, pubescente, brun jaunâtre. Les akènes mesurent 6,5 mm de longueur, 2,5 mm de largeur et 2,1 mm d’épaisseur, le poids de 100 akènes est de 1,97 g (données non publiées, mesures effectuées sur le lot de semences récolté dans le Var en 2025).
2.2. Variations infraspécifiques
Traditionnellement, deux formes étaient distinguées : f. pedunculata DC. aux capitules longuement pédonculés et f. sessilis DC. aux capitules subsessiles (Rouy & Foucaud, 1893-1913). Verlaque (1980) précise toutefois que ces formes n’ont pas de réelle valeur systématique, étant trouvées en mélange dans les mêmes populations. Plus tard, les travaux de Bobrov (1928-1929) et de Szabó (1940) ont proposé une subdivision en cinq sous-espèces, principalement différenciées par les caractères morphologiques de leurs fruits. Ce sont les suivantes : subsp. syriaca, subsp. phoeniciaca Bobrov, subsp. transcaucasica Bobrov, subsp. turanica Bobrov et subsp. emigrans Szabó (Verlaque, 1980). Selon cette conception, les populations introduites en France appartiendraient à la sous-espèce emigrans (Tison & de Foucault, 2014), également observée en Espagne, en Italie, en Sicile, dans les Balkans, en Asie mineure et au Kurdistan. Ce découpage est toutefois controversé et il n’est aujourd’hui plus reconnu par les spécialistes du genre (Ghazanfar & Edmondson, 2013 ; Göktürk & Sümbül, 2014).
Actuellement, les référentiels TaxRef v. 18 (Gargominy, 2025), LCVP – Leizig Catalogue of Vascular Plants (Freiberg, 2020), WP – WorldPlants (Hasslzer, 1994) et WFO – World of flora online (2025) reconnaissent uniquement Cephalaria syriaca, tandis que WCVP – World checklist of vascular plants (Govaerts, 2026) accepte la variété sessilis Boiss. ex Post.
3. Distribution en France
3.1. Présence historique
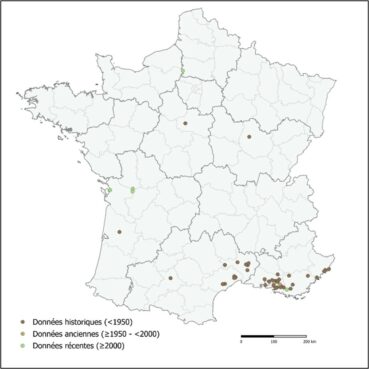
Cephalaria syriaca a été principalement signalée en région méditerranéenne dans les départements de l’Hérault, du Gard, du Vaucluse, des Bouches-du-Rhône, du Var et des Alpes-Maritimes (carte 1). Les premières mentions de l’espèce en France remontent vraisemblablement au début du xixe siècle dans le Gard (Conservatoire botanique national méditerranéen, 2025). Les indications figurant sur les étiquettes des parts d’herbier correspondant à ces premières récoltes mentionnent : « Nîmes, dans le blé » (récolte de Marschal, 18 juin 1812) et « aux environs de Nîmes, parmi les moissons. fl. Juin–juillet » (récolte de Johann Albert Luyken, 1812). Par la suite, C. syriaca est documentée autour d’Uzès entre 1858 et 1897, à Anduze (Pouzolz, 1862) et jusque sur les contreforts des Cévennes à Aumessas (Herbier des Phanérogames du Muséum national d’histoire naturelle de Paris, 1847).
Dans l’Hérault, Aimant Touchy la note d’abord à Montpellier à proximité d’un moulin à blé en 1847, puis en 1858 parmi les nombreuses plantes exogènes listées au Port-Juvénal, haut-lieu d’introduction d’adventices introduites avec les laines (Cosson, 1864). Après l’avoir relevée en abondance dans un champ inculte près de Montpellier, Loret la considère comme naturalisée (Loret, 1869). La plante fera l’objet d’observations jusqu’en 1907 autour de Montpellier, mais aussi dans les moissons de la vallée de l’Hérault à Montagnac et à Pézenas dans les années 1877-1880 (Conservatoire botanique national méditerranéen, 2025).
Dans les Alpes-Maritimes, C. syriaca apparaît plus tardivement, de 1875 à 1913, dans la région littorale entre Cannes et Gorbio près de Menton (Burnat et al., 1913). Selon ces auteurs, elle revêt « tous les caractères d’une plante adventice ».
Dans le Var, les premières mentions datent du début du xxe siècle dans trois zones distinctes : aux abords du plateau de Canjuers à Seillans avant 1908, à La Verdière en 1933 et autour du massif de la Sainte-Baume, dans un champ de blé à Plan-d’Aups-Sainte-Baume et de l’autre côté du massif à Méounes-lès-Montrieux (Decrock & Coste, 1911). À noter que c’est dans ce secteur, à un peu plus de 6 km des stations connues de Decrock et Coste, que la plante a été retrouvée par l’un d’entre nous (HM ; cf. infra).
Les Bouches-du-Rhône représentent la zone où C. syriaca a connu la plus grande extension géographique et temporelle, avec une présence dans quinze communes comprises entre Miramas, Martigues, la Sainte-Baume et la Sainte-Victoire, sur plus d’un siècle et demi (1847-1977). Les premières mentions concernent les quartiers de Sainte-Marthe, la Joliette et Château-Gombert où Marius Blaize l’a relevée à plusieurs reprises entre 1847 et 1856 (Conservatoire botanique national méditerranéen, 2025). Dès 1858, elle est signalée comme messicole dans les blés du bassin d’Aix-en-Provence (Milles, Roquefavour) où elle sera observée jusqu’en 1951. Situation semblable à Vauvenargues où elle sera notée dans les moissons de 1923 à 1936 (Laurent, 1933 ; Conservatoire botanique national méditerranéen, 2025).
Dans le Vaucluse, une récolte (Herbier Montpellier Université MPU) de l’abbé Terré de juillet 1939 atteste de sa présence à Pertuis, dans une céréale, route de Cucuron.
En dehors de la région méditerranéenne, C. syriaca n’a été recensée que cinq fois entre 1834 et 1937. Elle est d’abord mentionnée à Bordeaux, au bord de la Garonne, sur les quais de Paludate, en 1834 et 1835 (Laterrade, 1846). Timbal-Lagrave la note en 1855 parmi d’autres adventices au port Saint-Étienne à Toulouse, où le débarquement de marchandises et « l’épuration des blés étrangers dont les résidus sont jetés dans les champs environnants » favorisent l’introduction de nombreuses espèces exogènes (Académie des sciences, inscriptions et belles-lettres de Toulouse, 1855). La plante figure également sur une liste d’adventices introduites à Orléans par les « fourrages de la guerre » : signalée à l’été 1871, elle n’y est plus observée en 1872 (Nouel, 1873). Enfin, un compte rendu d’excursion la mentionne parmi les adventices « fugaces ou périodiques » de la région de Flavigny-sur-Ozerain dans l’Auxois, sans dates précises, d’après les notes de Georges Desplantes (Chouard, 1952).
3.2. Présence actuelle
Découverte de C. syriaca dans l’ouest de la France
La première observation récente dans l’Ouest remonte au 7 juin 2021. Timothée Vial note deux individus à Villiers-Couture (Charente-Maritime) dans une culture de Tournesol (Helianthus annuus) « au bout d’un champ » (T. Vial, pers. com., 2025). Le 19 juin 2024, l’un d’entre nous (FT) observe à son tour cinq pieds de C. syriaca en bordure d’une parcelle cultivée de Fenugrec (Trigonella foenum-graecum) au lieu-dit les Champs des Bois sur la commune d’Aubigné (Deux-Sèvres) à seulement 10 km de la station de 2021. Cette parcelle comprenait également Adonis annua, Anthemis cotula, Lysimachia arvensis, Roemeria argemone, Senecio vulgaris, Scandix pecten-veneris, Sinapis arvensis, Torilis arvensis, Valerianella eriocarpa, Veronica persica, etc. La plante n’a pas été revue en 2025 dans la même parcelle ensemencée en blé.
La station contemporaine la plus importante est probablement celle que nous (EC) avons découverte sur la ferme INRAE de l’Unité expérimentale de Saint-Laurent-de-la-Prée (Charente-Maritime) le 2 juin 2025 (stade végétatif à boutons) et identifié le 13 juin 2025 (BB). En poussant les investigations, environ 1 600 individus de C. syriaca ont été dénombrés dans trois parcelles (6,6 ha) semées en Fenugrec mi-avril 2025. Ces parcelles, situées dans le marais en zone naturelle d’intérêt écologique faunistique et floristique, sont conduites en agriculture biologique depuis 2017. Elles comprenaient par ailleurs le cortège d’adventices suivant : Alopecurus myosuroides, Atriplex prostrata, Avena fatua, Helminthotheca echioides, Kickxia spuria, Lepidium squamatum, Lolium sp., Lysimachia arvensis, Medicago arabica, M. polymorpha, Persicaria lapathifolia, Polygonum aviculare, Polypogon monspeliensis, Phalaris paradoxa, Ranunculus sardous, Rumex crispus, Senecio vulgaris, Sinapis arvensis, Sonchus asper, S. oleraceus, Trifolium alexandrinum, T. hybridum, Veronica persica et Vicia sativa. Parmi elles, se trouvait également Centaurea diluta.
Redécouverte de C. syriaca en Provence
En 2023, la Fédération de chasse du Var (FDC83) sollicite le CBNMed pour un partenariat sur les cultures faunistiques du plateau de Siou Blanc sur la commune de Signes (Var). La Fédération souhaite améliorer et mettre en valeur la biodiversité de ses parcelles et procéder à un inventaire de la diversité végétale existante. C’est lors de l’inventaire de ces parcelles, en juin 2024, qu’un individu de C. syriaca a été observé (HM). Le site est riche en messicoles caractéristiques, les relevés de 2024 ont permis de noter : Achillea collina, Adonis annua, Aegilops neglecta, Agrostemma githago, Aira cupaniana, Allium rotundum, Anthemis arvensis subsp. arvensis, Aphanes arvensis, Bromus arvensis, Bunias erucago, Bupleurum rotundifolium, Carthamus lanatus, Caucalis platycarpos, Convolvulus arvensis, Cota altissima, Cynosurus echinatus, Delphinium ajacis, Euphorbia falcata, Filago germanica, F. pyramidata, Galium divaricatum, G. parisiense, G. tricornutum, Gastridium ventricosum, Gypsophila vaccaria, Hypericum perforatum, Linum trigynum, Lysimachia foemina, Medicago sativa subsp. sativa, Ononis spinosa subsp. antiquorum, Phleum nodosum, Pisum sativum subsp. sativum, Poa compressa, Poterium sanguisorba, Ranunculus arvensis, Sinapis arvensis, Stachys germanica subsp. salviifolia, Trigonella esculenta, Valerianella discoidea, Vicia sativa, V. villosa.
La FDC83 réalise des rotations annuelles pour les semis. En 2024, la parcelle avait été semée avec un mélange conventionnel « GP tout vert » (Seigle forestier, Vesce commune ‘gravesa’, Pois fourrager ‘arkta’ et Avoine rude ‘alhama’). En 2025, la parcelle était composée d’un mélange de céréales, malgré cela la C. syriaca n’a pas été retrouvée. Cette parcelle, comparée à d’autres parcelles du secteur, présente un faible développement de la flore, messicole ou céréalière malgré une amélioration de la gestion et du choix des semences.
À la suite de ce constat, la moitié des semences a été récoltée (vingt-deux akènes) et conservée au CBNMed jusqu’à l’automne 2024, où ces akènes ont été semés dans deux exclos de 4 m² sur une autre parcelle riche en messicoles, afin de permettre le développement de l’espèce sur le plateau. La parcelle a été semée en mélange de céréales cultivées localement dans les Alpes (barbu de Briançon, blé meunier d’Apt, barbu de Langogne, rouge de Bordeaux, Florence Aurore, touzelle, orge, avoine, seigle) avec une densité de 100 kg par hectare afin de permettre une bonne expression des messicoles. Au printemps 2025, dix-neuf plants de C. syriaca ont ainsi pu se développer et produire de nombreuses semences. Dans l’objectif de faire une parcelle source conservatoire de messicoles, le même procédé a été répété en 2025 afin de garantir l’expansion de l’espèce sur le plateau de Siou Blanc.
Observation de l’espèce dans les Hauts-de-France
Un pied de C. syriaca a été observé en 2017 par Bénédicte Killian, en bordure de chemin dans un champ cultivé en agriculture biologique pâturé par des moutons, sur la commune de Sérifontaine (Oise) à la plaine de Droitecour. L’indentification a été réalisée d’après photos par Thibaud Daumal.
4. Discussion sur le statut de l’espèce en France
4.1. Archéophyte ou néophyte ?
L’aire d’origine de Cephalaria syriaca inclut le pourtour oriental de la Méditerranée au Proche et Moyen-Orient, et s’étend jusqu’au Caucase et à l’Asie centrale (Ghazanfar & Edmondson, 2013 ; POWO, 2025). Dans cette aire, elle occupe des habitats naturels du type « clairières dans les chênaies, éboulis serpentiniques, terrains rocheux, argilo-sableux », mais elle est aussi adventice dans les « plantations de laitue » et les champs cultivés (blé, lin) (Ghazanfar & Edmondson, 2013).
À la lecture de la littérature, il ne fait aucun doute sur le caractère exogène de Cephalaria syriaca en France. Dans les pays voisins, dans l’ouest du bassin méditerranéen – en Italie, en Espagne, en Algérie et au Maroc – elle est considérée comme exogène. On peut toutefois s’interroger sur la date d’introduction et le statut archéophyte ou néophyte. Son association étroite avec les moissons peut laisser penser à une messicole archéophyte (Jauzein, 2001). Ce statut, associé à sa rareté et ses apparitions fugaces peut expliquer qu’elle figure sur la liste des espèces protégées au niveau national.
Les éléments factuels en notre possession amènent plutôt à le considérer comme un taxon néophyte introduit assez récemment, peut-être seulement au xixe siècle. Alors que les Bouches-du-Rhône semblent être le département où C. syriaca a été le plus répandue, il n’est pas mentionné dans l’ouvrage de Garidel (1715). Sa première mention dans une flore nationale remonte au tome V de la Flore française initiée par Lamarck et rédigé par de Candolle (1815). Il indique que MM. Delavaux et Luyken ont trouvé la plante « dans les moissons, à deux lieux au nord de Nismes » (cf. supra). La première mention connue date donc de 1812 dans le Gard.
Il est clairement établi que l’espèce a été introduite comme contaminant de semences de blé (Balland, 1894). Une part d’herbier de 1854 à Aumessas (Gard) mentionne « espèce exotique venue de graines mêlées à du froment de Syrie » (Conservatoire botanique national méditerranéen, 2025). De nombreux ouvrages d’agronomie de cette période la citent parmi les adventices qu’il faut trier du blé (Serrand, 1891). Dans une enquête ethnobotanique consacrée à la parabole biblique du « bon grain et de l’ivraie », visant à identifier l’espèce correspondant à l’ivraie, Musselman (2000) retient Lolium temulentum et Cephalaria syriaca. Il souligne que ces deux espèces sont indistinctement désignées par les paysans du Proche-Orient sous le nom de zawān (ivraie), que leur cycle de développement est synchronisé avec celui du blé et que leurs semences présentent une taille et une morphologie proches de celles du blé. Toutefois, contrairement à Lolium temulentum, Cephalaria syriaca n’a jamais été identifiée dans les restes de récoltes de blé mis au jour lors de fouilles archéologiques. Il semble ainsi que C. syriaca ne soit devenue une adventice caractéristique des cultures de blé que plus tardivement, sans que les changements de pratiques agricoles à l’origine de cette évolution aient pu être clairement établis (Musselman, 2000).
Au xixe siècle, les blés importés de Syrie et d’Égypte étaient particulièrement connus pour être « contaminés » par des akènes de C. syriaca, au point que dans le commerce de la minoterie elles étaient connues sous le nom de « graines de dattes » (Cornevin, 1892). Les blés qui en contenaient étaient déclassés et vendus à bas prix à des vermicelliers (Balland, 1894). Balland (1907) rapporte encore que le pain de munition (pour l’approvisionnement des armées) fabriqué avec des blés d’Égypte prenait une saveur amère et une teinte ardoisée même à la dose de 2 à 5 g de C. syriaca pour 1 kg de blé. À ce propos, la flore d’Iraq précise qu’« en contaminant les grains à une époque de pénurie et en rendant le pain sombre et malodorant, [C. syriaca] a failli provoquer une révolte à Bagdad en 1948-49 » (Ghazanfar & Edmondson, 2013). L’expérience géorgienne est très différente : Kacharava et Epitashvili (2019) notent que l’impossibilité d’éliminer complètement les semences de C. syriaca fait qu’elles sont moulues avec le blé, ce qui confère au pain une teinte légèrement bleutée, un goût agréable et particulier, ainsi qu’une texture moelleuse. Cette pratique accidentelle est même devenue intentionnelle est fait partie de la culture gastronomique géorgienne. Ainsi le pain de Kakheti, appelé Kakhuri Shoti, est produit avec des variétés locales de blé tendre de la région de Kakheti et certaines boulangeries ajoutent une petite quantité d’akènes de Makhobeli (C. syriaca) (maximum 2 %) à la farine, ce qui confère au pain une teinte bleutée violette ainsi qu’une fraîcheur durable (United Nations Industrial Development Organization (UNIDO), 2020). Nous refermons ici cette parenthèse ethnobotanique qui montre le lien très étroit entre blé et Cephalaria syriaca.
Revenons au statut de la plante. En plus d’être néophyte, on peut se demander si Cephalaria syriaca a vraiment été naturalisée en France ou si elle n’a jamais été qu’occasionnelle. Certains auteurs, comme Godron (1854), la listent parmi les espèces naturalisées dans les moissons. De même, Loret (1869) semble l’admettre comme naturalisée après l’avoir observée en abondance dans un champ inculte, et non plus seulement aux abords de moulins (sous-entendu introduite avec le blé). À cette époque, la distinction entre taxon occasionnel (adventice) et taxon véritablement naturalisé n’était pas toujours clairement établie.
Thellung (1912), qui adopte une vision résolument moderne concernant le statut des plantes introduites (Kowarik & Pyšek, 2012), résume sa présence en précisant qu’elle est « rare et probablement seulement adventice [c’est-à-dire occasionnelle, non naturalisée] dans le Midi de la France (Bouches-du-Rhône, Gard, Hérault) ainsi qu’en Ligurie ». Ce constat confirme celui de Marnac et Reynier (1910) qui, après avoir recensé les localités bucco-rhodaniennes, concluent : « De toutes les localités susdites, nous n’en connaissons aucune où cette Dipsacée soit véritablement naturalisée ». Il apparaît donc que la plupart des stations étaient éphémères, comme le confirment de nombreuses flores et articles sur l’espèce. Bonnier et Douin (1912‑1935) notaient par exemple : « çà et là dans les champs d’où il disparaît quelquefois l’année qui suit l’ensemencement du blé qui en contenait les graines ».
On ne peut totalement exclure que C. syriaca ait été temporairement naturalisée, notamment dans le bassin d’Aix-en-Provence, où des observations s’échelonnent sur plusieurs dizaines d’années. Toutefois, une présence durable pourrait aussi résulter d’un flux continu d’introduction via des lots de semences de blé – l’espèce étant, comme on l’a vu, difficile à séparer du grain –, ce qui, dans ce cas, correspond toujours au statut d’espèce occasionnelle (Fried et al., 2024).
4.2. Discussion sur les stations contemporaines
Il est intéressant de noter que deux des observations récentes dans l’ouest de la France sont associées au Fenugrec. L’analyse d’un des sacs du lot de semence de Fenugrec utilisés par l’Unité expérimentale de l’INRAE à Saint-Laurent-de-la-Prée a révélé la présence de semences de C. syriaca (trois sous-échantillons de 75 g contenaient respectivement douze, douze et dix akènes de C. syriaca). Ce Fenugrec certifié Agriculture Biologique a été produit en Italie où l’espèce est rare, mais a fait l’objet d’observations récentes (2017 et 2021) dans des parcelles de Fenugrec (Galasso et al., 2018).
Le fait que C. syriaca ait également été observée dans du Fenugrec en Italie suggère que cette culture pourrait désormais représenter un nouveau vecteur de diffusion de l’espèce. En revanche, le blé ne semble plus jouer ce rôle : les méthodes modernes de tri sont probablement devenues plus efficaces. Musselman (2000) avance aussi que les variétés contemporaines de blé présentent des grains plus gros que les blés anciens, rendant le mimétisme entre les deux types de fruits beaucoup moins évident (même si cette hypothèse néglige l’éventuelle capacité évolutive de C. syriaca et la possibilité de sélection involontaire d’akènes de C. syriaca plus gros).
Si plusieurs observations récentes semblent étroitement liées à la culture du Fenugrec, cette association n’est toutefois pas systématique. En effet, la station varoise découverte en 2024 ne présente aucun lien avec cette espèce cultivée : l’unique individu observé s’est développé dans une parcelle ensemencée avec un mélange fourrager conventionnel « GP tout vert ». Depuis plusieurs années, cette parcelle est cultivée soit avec un mélange de fleurs pour culture faunistique (40 % phacélie, 35 % navette malwira, 15 % radis chinois et 10 % moutarde brune), soit avec du blé. Cette occurrence montre que C. syriaca peut également apparaître en dehors du contexte du Fenugrec, ce qui élargit les hypothèses sur ses voies actuelles de dissémination.
Une question demeure toutefois majeure : l’espèce est‑elle en mesure de se maintenir localement par elle‑même ou dépend‑elle d’introductions répétées pour perdurer ? Si l’espèce dispose d’une capacité réelle de pérennisation, il est plausible qu’elle soit déjà présente dans d’autres secteurs du plateau de Siou Blanc, où plusieurs parcelles à gestion extensive demeurent difficilement accessibles. Ce secteur, encore faiblement prospecté pour la flore inféodée aux agrosystèmes, pourrait ainsi abriter d’autres individus passés inaperçus.
5. Perspectives
Pour le botaniste souhaitant observer C. syriaca, la prospection des parcelles de Fenugrec peut s’avérer pertinente. Les surfaces consacrées à cette culture demeurent modestes en France ; elle est actuellement testée comme plante fourragère ou, plus fréquemment, utilisée comme couvert végétal en interculture ou dans les inter-rangs de vigne, afin d’améliorer la structure du sol et de favoriser la fixation de l’azote. Il serait également utile d’assurer le suivi des stations récemment découvertes, afin d’évaluer la stabilité de ces populations, en regard du caractère historiquement instable attribué à ce taxon.
Dans cette perspective, le CBNMed assure déjà le suivi de la parcelle de découverte de l’espèce. Afin d’optimiser les connaissances et de sécuriser la conservation de l’espèce, le CBNMed a mis en place un protocole spécifique de récolte et de multiplication des semences in situ sur des parcelles plus favorables au développement de messicoles, permettant d’envisager à terme une meilleure compréhension du fonctionnement local de la population et le développement d’actions de conservation adaptées. Cette démarche s’inscrit dans l’idée que, malgré son caractère néophyte, l’espèce demeure une messicole caractéristique du cortège du Roemerion hybridae.
Par ailleurs, la collaboration entre le CBNMed et la Fédération départementale des chasseurs du Var, déjà engagée dans la gestion des messicoles, constitue un levier favorable pour le maintien et la restauration de ces espèces messicoles patrimoniales sur le plateau de Siou Blanc, contribuant ainsi à l’amélioration de la diversité végétale de ce territoire à forts enjeux écologiques.
Bibliographie
Académie des sciences, inscriptions et belles-lettres de Toulouse, 1855. Bulletin des travaux de l’Académie pendant l’année 1855. Mémoires de l’Académie impériale des sciences, inscriptions et belles-lettres de Toulouse : 420-421.
Balland A., 1894. Recherches sur les blés, les farines et le pain. Henri Charles-Lavauzelle, Paris, 306 p.
Balland A., 1907. Les aliments : analyse, expertise, valeur alimentaire, II – Céréales. Librairie J.-B. Baillière & Fils, Paris, 432 p.
Bonnier G. & Douin R., 1912‑1935. Flore complète illustrée en couleurs de France, Suisse et Belgique (comprenant la plupart des plantes d’Europe). Librairie générale de l’enseignement, Paris, Delachaux & Niestlé, Neuchâtel, Lebègue & Cie / Office de Publicité, Bruxelles, 12 tomes + 1 volume de tables, 721 planches en couleurs.
Bojňanský V. & Fargašová A., 2007. Atlas of seeds and fruits of central and east European flora: The Carpathian Mountains region. Springer, 1 046 p.
Burnat E., Briquet J. & Cavillier F.,1913. Flore des Alpes maritimes ou catalogue raisonné des plantes qui croissent spontanément dans la chaîne des Alpes maritimes, V. H. Georg et Cie, Genève, Bâle, Lyon, 375 p.
Candolle A.-P. (de), 1815. Flore française, ou descriptions succinctes de toutes les plantes qui croissent naturellement en France (tome 5 [= 6ᵉ vol.], contenant 1 300 espèces non décrites dans les cinq premiers volumes), Desray, Paris, 662 p.
Chouard P., 1952. Commentaire botanique des excursions de juillet 1951 dans le sud-est du Bassin parisien. Bulletin de la Société botanique de France 99 (10), 54-69, https://doi.org/10.1080/00378941.1952.10836512.
Conservatoire botanique national méditerranéen, 2025. SIMETHIS – module Flore [online], http://simethis.eu [21/11/2025].
Cornevin C., 1892. Des résidus industriels dans l’alimentation du bétail. Firmin-Didot, Paris, 552 p.
Coste H., 1937. Flore descriptive et illustrée de la France, de la Corse et des contrées limitrophes, réédition. Librairie des Sciences et des Arts / A. Blanchard, Paris, 3 vol.
Cosson E. 1864. Appendix florulae juvenalis altera ou deuxième liste de plantes étrangères récemment observées par M. Touchy au Port-Juvénal près Montpellier. Bulletin de la Société botanique de France 6 : 159-164.
Decrock E. & Coste F.J., 1911. Herborisation à la forêt de Montrieux. Le Chêne 5 : 259-267.
Freiberg M. ,2020. The Leipzig catalogue of vascular plants. German Centre for Integrative Biodiversity Research (iDiv) Halle-Jena-Leipzig. Checklist dataset https://doi.org/10.15468/9qxmn3 accessed via GBIF.org [18/12/2025].
Fried G., Affre L., Albert A. et al., 2024. Analyse de la terminologie relative aux plantes vasculaires exogènes : application à l’inventaire des archéophytes et néophytes de France hexagonale. Naturae 2024 (4) : 69-97, https://sciencepress.mnhn.fr/fr/periodiques/naturae/2024/4.
Galasso, G., Domina G., Adorni M. et al., 2018. Notulae to the Italian alien vascular flora, 5. Italian Botanist 5 : 45-56.
Gargominy O., 2025. TAXREF v. 4.17. UAR PatriNat (OFB-MNHN-CNRS-IRD), Paris. Checklist dataset https://doi.org/10.15468/vqueam accessed via GBIF.org [18/12/2025].
Garidel P.-J., 1715. Histoire des plantes qui naissent aux environs d’Aix, et dans plusieurs autres endroits de la Provence. Joseph David, Aix-en-Provence, 522 p.
Ghazanfar S.A. & Edmondson J.R. (éds), 2013. Flora of Iraq, V (2), Lythraceae to Campanulaceae. Royal Botanic Gardens, Kew, 349 p.
Godron G., 1854. Considérations sur les migrations des végétaux, et spécialement de ceux qui, étrangers au sol de la France, y ont été introduits accidentellement. Veuve Bouchard-Huzard, Paris.
Göktürk R.S. & Sümbül H., 2014. A taxonomic revision of the genus Cephalaria (Caprifoliaceae) in Turkey. Turkish Journal of Botany 38 (5), article 9, https://doi.org/10.3906/bot-1310-6.
Govaerts R., 2026. The World Checklist of Vascular Plants (WCVP). Royal Botanic Gardens, Kew. Checklist dataset https://doi.org/10.15468/6h8ucr accessed via GBIF.org [18/12/2025].
Jauzein Ph., 2001. Biodiversité des champs cultivés : l’enrichissement floristique. Dossier de l’environnement de l’INRA 21 : 43-64.
Hassler M., 1994-2025 World Plants. Synonymic Checklist and Distribution of the World Flora, v. 25.12, last update Dec. 21st, 2025, www.worldplants.de [18/12/2025].
Kacharava T. & Epitashvili T., 2019. Ethnobotanical value of Cephalaria syriaca. 4th Edition of Global Conference on Plant Science and Molecular Biology (GPMB‑2019), 19-21 septembre 2019, Londres, Royaume‑Uni : 117.
Kowarik I. & Pyšek P., 2012. The first steps towards unifying concepts in invasion ecology were made one hundred years ago: revisiting the work of the Swiss botanist Albert Thellung. Diversity and Distributions 18 (12) : 1243-1252, https://doi.org/10.1111/ddi.12009.
Laterrade J.-F., 1846. Flore bordelaise et de la Gironde : description caractéristique des plantes qui croissent naturellement dans ce département, précédée de notions élémentaires de botanique (4e éd.). Feret et fils, Bordeaux, 690 p.
Laurent L., 1933. À propos d’une station de Cephalaria syriaca Schrad. (Scabiosa syriaca L.). Le Monde des plantes 4 (202) : 28.
Loret H., 1869. Note sur une dizaine de plantes nouvelles pour la flore de Montpellier et de l’Hérault. Bulletin de la Société botanique de France 16 : 285-289.
Marnac E. & Reynier A., 1910. Préliminaires d’une flore des Bouches-du-Rhône (suite). Bulletin de l’Académie internationale de géographie botanique 244 : 57-88.
Musselman L., 2000. Zawan and tares in the Bible. Economic Botany 54 (4) : 537-542, https://doi.org/10.1007/BF02866551.
Nouel E. 1872. Sur un certain nombre de plantes adventices qui ont été recueillies à Orléans, dans l’année 1871. Mémoires de la Société d’agriculture, sciences, belles-lettres et arts d’Orléans 14 : 35-39.
Pouzolz P.M.C. (de), 1862. Flore du Département du Gard ou description des plantes qui croissent naturellement dans ce département. Ed. Coulet, Montpellier, Delahaye, Paris, 2 tomes.
POWO, 2025. Plants of the World Online, facilitated by the Royal Botanic Gardens, Kew, retrieved [29/10/2025], from https://powo.science.kew.org.
Rouy G. & Foucaud J., 1893-1913. Flore de France ou Description des plantes qui croissent spontanément en France, en Corse et en Alsace-Lorraine. G. Rouy, Asnières-sur-Seine, 14 vol.
Serand E.-H.-L., 1891. Étude agronomique, statistique et commerciale sur les céréales : le blé, culture, classification, géographie agricole et commerciale, trafic (tome 1). Paris [s.n.].
Thellung A., 1912. La flore adventice de Montpellier. Mémoires de la Société nationale des sciences naturelles et mathématiques de Cherbourg 38 : 57‑728.
Tison J.-M. & de Foucault B. (coord.), 2014. Flora Gallica, Flore de France. Éditions Biotope, Mèze, xx +1 196 p.
Tison J.-M., Jauzein Ph. & Michaud H., 2014. Flore de la France méditerranéenne continentale. Naturalia Publications / Conservatoire botanique national méditerranéen, Turriers, p.
United Nations Industrial Development Organization (UNIDO), 2020. Typical Georgian Food Products: A National Mapping Summary. Rapport du projet “Identification of Typical Georgian food/terroir products”, coordonné par Giorgi Todua et Ebe Muschialli. Tbilissi : UNIDO
World Flora Online, http://www.worldfloraonline.org/ [18/12/2025].
Verlaque R., 1980. Étude caryologique de Cephalaria syriaca (L.) Schrader (Dipsacaceae). Caryologia 33 (3) : 353-386, https://doi.org/10.1080/00087114.1980.10796850.
Remerciements
Nous remercions Aurélien Caillon (CBNSA), Thibaud Daumal, Bénédicte Killian et Timothée Vial pour le contexte de leurs observations, ainsi que Saskia Bastin (Anses) et Olivier Jonquet pour leurs photos.