Translocation de deux géophytes méditerranéennes en Occitanie : peut-on parler de succès ?
Title
Translocation of two Mediterranean geophytes in the Occitanie region: can we call it a success?
Résumé
Deux géophytes méditerranéennes, inscrites sur la liste de protection nationale en France, ont fait l’objet de translocations en région Occitanie. Pour Iris xiphium, des renforcements ont été conduits dans son unique site en France, sur la commune de Portiragnes. Pour Allium chamaemoly, une réintroduction a été réalisée pour accompagner la compensation liée aux impacts répétés subis par ses populations dans le cadre d’aménagements divers. L’intérêt, pour les translocations, du suivi parallèle de populations naturelles de référence, de l’utilisation conjuguée de graines et de bulbes, et des suivis à long terme est discuté pour les deux cas d’étude.
Abstract
Two Mediterranean geophytes, listed for national protection in France, have been translocated in the Occitanie region. For Iris xiphium, reinforcement measures were carried out at its only site in France in the municipality of Portiragnes. For Allium chamaemoly, a reintroduction programme was implemented to compensate for repeated impacts on its populations due to various development projects. The benefits for translocations of parallel monitoring of natural reference populations, the combined use of seeds and bulbs, and long-term monitoring are discussed for both case studies.
1. Introduction
Depuis plusieurs décennies, force est de constater que la biodiversité végétale subit des déclins incontestables. Dans un article qui sonnait l’alarme sur l’état appauvri du monde végétal dans une large diversité de régions de la planète, Zecchini (1998 : 28) posait la question suivante : « le patrimoine végétal de la planète a-t-il encore un avenir ? ». L’ampleur des pertes est dramatique et la biodiversité végétale est souvent réduite à des « poches » où certaines espèces en cours de raréfaction se retrouvent isolées. Ces espèces risquent non seulement de continuer à décliner, mais aussi de disparaître dans l’avenir, d’où le titre de l’article : « la nature est en sursis ». Autrement dit, leur avenir est compromis par une dette écologique, une dette qui les mènera à l’extinction (par exemple voir Vellend et al., 2006).
En région méditerranéenne le déclin de la flore est particulièrement préoccupant (Médail & Diadema, 2006 ; Thompson, 2020). Les suivis d’espèces végétales rares et menacées, même lorsqu’elles figurent sur les listes de protections réglementaires, montrent souvent leur forte vulnérabilité liée à leur faible abondance qui induit une dynamique temporelle de déclin (Gauthier et al., 2019a, b). Faute de mesures de gestion et de protection fortes de leurs habitats, l’augmentation du taux d’espèces végétales menacées d’extinction dans la région va encore s’accélérer.
Parmi les différentes formes de gestion instaurées pour les espèces vulnérables, la translocation d’individus, voire de populations entières, est un outil de plus en plus utilisé. Il s’agit d’une technique d’ingénierie écologique basée sur deux méthodes. La première a comme objectif de renforcer des populations d’une espèce dans lesquelles un déclin ou une certaine vulnérabilité sont constatés ; l’objectif est de stimuler une augmentation des effectifs de la population par la mise en culture ex situ et la réimplantation d’un grand nombre d’individus ou de graines dans et/ou autour de son site d’origine. La seconde méthode a pour objectif de créer une population dans un site nouveau au sein de l’aire de répartition de l’espèce par la réintroduction de plantes provenant le plus souvent d’une autre population naturelle. Dans bien des cas, cette méthode est employée suite à la destruction d’un site où l’espèce était présente, notamment dans cadre de l’application de la séquence Éviter – Réduire – Compenser (ERC) qui est un dispositif légal du code de l’environnement (article L. 110-1).
Depuis les premières expérimentations de translocation, les auteurs se sont beaucoup interrogés sur la manière d’évaluer leur efficacité, voire leur succès. Pavlik (1996) et Primack & Drayton (1997) ont été parmi les premiers à réfléchir à cette question et à montrer que le « succès » peut être défini de plusieurs manières. Si l’objectif de la translocation est de recréer une nouvelle population viable ou de rendre plus viable une population existante, alors « le succès » sera atteint seulement si la population produit des fleurs et des graines et par la suite une nouvelle génération de plantes en fleurs. Ainsi, une translocation sera un succès si la population augmente en nombre d’individus ou en termes d’occupation de l’espace. Le succès ne se résume donc pas simplement à la survie des individus transloqués même s’ils fleurissent (Menges, 2008), mais nécessite les indications d’une bonne dynamique qui assure la persistance de la population dans l’avenir. Ainsi, la dissémination à partir des parcelles de réimplantation pour créer des nouvelles taches d’individus et des populations constitue un gage de succès (Primack & Drayton, 1997), même lorsque les plantes de la translocation initiale disparaissent. Plus récemment, Godefroid et al. (2011) ont introduit un nouveau critère de succès, « la capacité de s’adapter aux conditions du milieu qui évoluent ».
Récemment, l’analyse d’un grand nombre de tentatives de translocations a montré que, au moins à court terme et malgré la persistance des plantes transloquées, le résultat le plus commun est un échec avec l’absence de création de nouvelles populations d’individus reproducteurs (Drayton & Primack, 2012 ; Godefroid et al., 2011, 2025). Cependant, peu de translocations ont été suivies à long terme, c’est-à-dire plus que cinq-six ans.
C’est dans ce cadre que nous avons proposé et suivi les translocations de deux espèces de géophytes méditerranéennes. Dans le premier cas, nous avons procédé au renforcement de la population d’une espèce existant dans un seul site en France, où elle présente une vulnérabilité forte du fait de sa rareté et des milieux qu’elle colonise. Pour la deuxième espèce, qui subit des impacts dans un grand nombre de sites en région Occitanie, nous avons procédé à la réintroduction d’une population (suite à la destruction de son site d’origine) dans un site nouveau dans le cadre de mesures de compensation. Pour les deux espèces, nous avons implanté des graines et des bulbes et mis en place un suivi annuel pendant plus de dix ans.
L’objectif principal de cette étude est de tester l’importance de différents éléments liés à la méthodologie de la translocation et au suivi de l’expérimentation. Nous tentons, en effet, de répondre à trois questions clefs. Premièrement, est-ce que le suivi des populations naturelles et la comparaison de leurs dynamiques avec celles des individus dans les parcelles de translocation permettent de mieux juger du succès de l’expérimentation ? Deuxièmement, est-ce que la combinaison de semis avec les plantations de bulbes apporte une complémentarité qui augmente l’efficacité des expérimentations à long terme ? Troisièmement, sachant que les deux espèces sont pérennes en région méditerranéenne où les variations interannuelles des cumuls de pluie sont très fortes, quelle est la pertinence de suivre ces expérimentations à long terme (plus de dix ans) ?
2. Espèces et sites d’étude
2.1. Iris xiphium L.
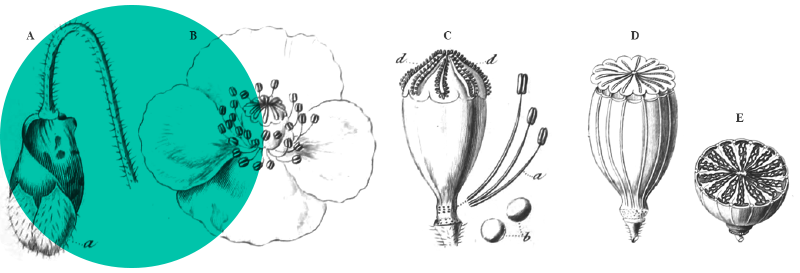
Iris xiphium, l’Iris d’Espagne, est une géophyte à bulbe. Ses inflorescences composées de 1 à 2 (voire 3) fleurs violettes à étendard avec une tache jaune remarquable au centre s’épanouissent de fin mai à mi-juin et mesurent jusqu’à 1 m de hauteur (planche 1, gauche). Ses feuilles bleutées en gouttière étroite peuvent se confondre avec celles des graminées.
Cette espèce est présente en Espagne, au Portugal et en Afrique du Nord où elle colonise des habitats variés depuis les prés salés d’arrière-dunes sur les littoraux aux pelouses et garrigues ouvertes d’arrière-pays (carte 1, a). En France, I. xiphium présente une seule localité spontanée sur la commune de Portiragnes au sud-est du site Natura 2000 de la grande Maïre (Hérault ; carte 1, b et c). I. xiphium est classé comme « préoccupation mineure » (LC) sur la Liste rouge globale de l’IUCN, alors qu’en France sa faible abondance associée à une répartition limitée à une seule localité et une niche originale le rendent très vulnérable à une extinction. Il est donc classé « en danger critique » (CR) et figure sur la liste des espèces protégées au niveau national.
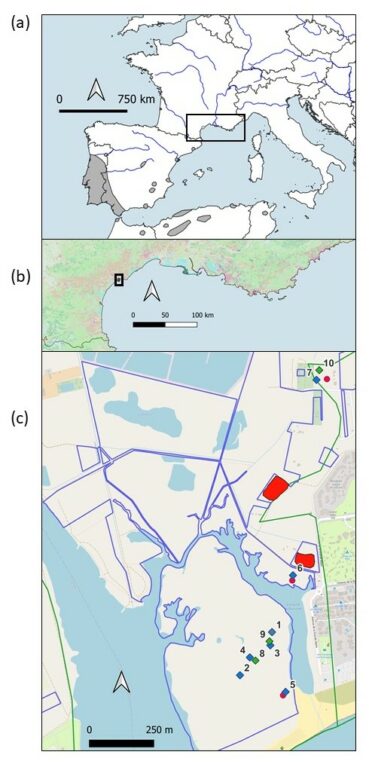
Carte 1. Répartition d’Iris xiphium (a) autour de la Méditerranée (d’après de Bolòs & Vigo, 1984), (b) dans le sud de la France et (c) localisation des taches naturelles (en rouge) et des sites de renforcement de 2012 (losanges bleus numérotés de 1 à 7) et de 2014 (losanges verts numérotés de 8 à 10) sur le site Natura 2000 de la Grande Maïre à Portiragnes-Plage (limites bleues) qui est situé sur un site du Conservatoire du littoral (limites vertes) ; P. Gauthier, CC-BY-NC-ND.
2.2. Allium chamaemoly L.
Allium chamaemoly, le petit Ail doré, est une géophyte à bulbe ovoïde. Ses inflorescences à fleurs blanc pur en ombelles pauciflores rasant le sol s’épanouissent de décembre à février (planche 1, droite). Ses feuilles linéaires lancéolées, souvent tordues et la plupart du temps très velues, sont appliquées au sol.
L’aire de répartition d’A. chamaemoly s’étend dans toute l’Europe méditerranéenne, de l’Espagne à la Grèce, ainsi qu’en Afrique du Nord (au Maroc, en Tunisie et en Algérie) (carte 2, a). En France, ses populations se distribuent sur une frange de faible altitude le long du littoral méditerranéen depuis la frontière espagnole jusqu’à la Côte d’Azur (carte 2, b) et en Corse. Cette espèce colonise des habitats ouverts variés comme des garrigues basses ou des pelouses rocailleuses (Corine-biotopes 34.51) souvent sur calcaire, mais aussi sur des affleurements basaltiques et des dunes grises (Corine-biotopes 16.22). A. chamaemoly est classé comme « LC » sur les listes rouges globale et française de l’IUCN en raison de sa distribution relativement large aux deux échelles. Elle apparait néanmoins sur la liste des espèces protégées au niveau national en France et est régulièrement impactée par les travaux d’aménagement qui s’intensifient sur la frange méditerranéenne française.
Des opérations de translocation ont été menées dans des cadres différents pour ces deux espèces :
- dans le cas d’I. xiphium pour limiter le risque de son extinction lié à son isolement et à ses faibles effectifs ;
- dans le cas d’A. chamaemoly pour atténuer les pertes de populations régulièrement observées dans le cadre d’aménagements sur son aire de répartition.
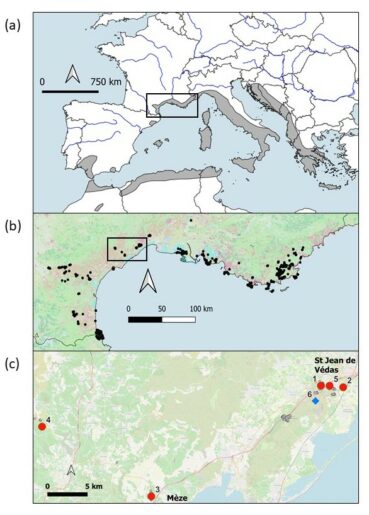
Carte 2. Répartition d’Allium chamaemoly (a) autour de la Méditerranée (d’après de Bolòs & Vigo, 1984), (b) dans le sud de la France (données du Conservatoire botanique méditerranéen issues de https://simethis.eu/) et (c) localisation des populations naturelles suivies (cercles rouges) et de la population de réintroduction (losange bleu) ; 1 = Saint-Jean-de-Védas, 2 = bois de Maurin, 3 = Mèze, 4 = Caux, 5 = Saint-Jean-de-Védas-Péage et 6 = introduction de la Gardiole ; P. Gauthier, CC-BY-NC-ND.
3. Méthodologie et suivi des translocations
Pour les deux espèces, les suivis (dénombrement ou occupation) sur les populations naturelles constituent des « dynamiques de références ». Leur utilité principale est de voir si les fluctuations de floraison ou d’occupation observées sur les parcelles de translocation sont liées à des problèmes d’implantation ou à des oscillations « naturelles » des populations.
3.1. Iris xiphium
En juin 2007, une étude préliminaire a montré que la population de Portiragnes se présente sous la forme de deux taches principales (« sous-populations ») et de trois petites taches (carte 1, c) où un total de 1 045 tiges florales a été dénombré. Sur ce site Iris xiphium se développe dans des prés halo-psammophiles (Corine-biotopes 15.53). Cet habitat, à faible salinité, est situé à un niveau topographique supérieur sur le revers continental du bourrelet dunaire où il ne subit généralement pas d’inondation. Ses apports d’eau douce proviennent de la lentille d’eau captive des sables et aboutissent à un dessalement complet en saison froide suivi de remontées faibles de sel en saison chaude. Cet habitat occupe une place importante et reconnaissable sur la zone où se développe I. xiphium.
À partir d’une récolte de graines réalisée sur le site, en 2004, par J. Molina (CBNMed) et M. Debussche (CEFE, CNRS), notre équipe disposait de 2 000 plantes en pots sur le terrain d’expérience du CEFE (plateforme TE) et d’un important stock de graines suite à leur floraison en 2012.
En juin 2012, une étude de la niche écologique fine (Lorin, 2012) a montré que la présence d’I. xiphium est souvent associée à celle de taxons caractéristiques des prés halo-psammophiles comme Schoenus nigricans L. et Elytrigia spp. Des analyses du sol dans les différentes zones de présence ont aussi indiqué que l’espèce colonise toujours des sols à salinité moyenne à faible. À partir de ces critères, nous avons prospecté entre les deux taches naturelles les plus éloignées et recherché des parcelles potentiellement favorables à l’implantation de renforcements. Nous avons ainsi retenu dix parcelles pour la translocation, quatre proches de taches naturelles et six plus éloignées, mais toutes au sein de l’aire géographique occupée par l’espèce (carte 1, c).
En octobre 2012, 1 295 bulbes et 12 250 graines ont été introduits dans sept de ces dix parcelles déterminées comme favorables. Dans chaque parcelle, le dispositif était le suivant : quinze placettes d’1 m² ont été disposées le long de transects localisables à l’aide de piquets fixes comprenant, aléatoirement, cinq placettes avec 25 bulbes, cinq avec 12 bulbes et cinq avec 350 graines.
En octobre 2014, les trois parcelles restantes ont été utilisées pour des renforcements supplémentaires mais avec seulement cinq placettes avec 25 bulbes et cinq placettes avec 12 bulbes, soit 555 bulbes supplémentaires. Sur chaque placette les bulbes ont été introduits individuellement à l’aide d’une tarière manuelle et à distance régulière. Au total, 1 850 bulbes ont ainsi été implantés dans dix localités sur le site (carte 1, c). Les fleurs ont été dénombrées sur chacune de ces placettes, annuellement, depuis le printemps 2013.
Dès juin 2012, un suivi de référence a été mis en place dans chacune des deux grandes sous-populations naturelles : les fleurs ont été dénombrées, annuellement, au pic de floraison (mi-juin), sur quinze placettes fixes de 4 m² subdivisées en cellules d’1 m² et disposées le long d’un transect localisable à l’aide de piquets fixes. En 2012, puis annuellement de 2016 à 2025, toutes les fleurs observées sur les parcelles naturelles ont aussi été comptées.
3.2. Allium chamaemoly
En 2013, dans le cadre d’une mesure d’accompagnement, liée au doublement de l’autoroute A 9, soixante-dix individus d’Allium chamaemoly localisés sur le tracé même du doublement ont été prélevés avant destruction. Conservés en jauges sur le terrain d’expérience du CEFE, pendant deux ans en attendant l’acquisition de terrains de compensation, ces plantes se sont dédoublées et ont produit des graines. En 2015, 315 bulbes et 1 200 graines étaient disponibles pour une réintroduction.
En 2011, une caractérisation biotique et abiotique de la niche fine d’A. chamaemoly réalisée dans quinze stations du sud de la France, entre Narbonne et Marseille, a montré que le pourcentage de roche mère affleurant est significativement plus important et le sol significativement plus pauvre en présence de l’espèce qu’en son absence (de Nervo, 2011). Cette étude a été utilisée pour localiser une parcelle potentiellement favorable sur le site de compensation en gestion par le CEN-Occitanie sur le massif de la Gardiole où la population de réintroduction d’A. chamaemoly a finalement été réimplantée fin mai 2015.
Sur la parcelle, les 315 bulbes ont été réintroduits sur sept placettes et 1 200 graines semées sur trois autres placettes. Pour les bulbes, sur chaque placette d’1 m² divisée en cent cellules de 10 cm*10 cm, 45 bulbes étaient plantés par groupe de trois aléatoirement dans quinze cellules. Pour les graines sur chaque placette, 400 graines étaient semées sur un sol gratté superficiellement puis recouverte d’une fine pellicule de sol tassé. L’emplacement des placettes était localisable grâce à un marquage permanent et trois des sept placettes de bulbes étaient protégées par une grille solidement ancrée au sol. Dès 2016, au pic de floraison d’A. chamaemoly, fin janvier, les plantes végétatives ou en fleurs ont été localisées et dénombrées annuellement sur chacune des placettes ainsi que sur une « zone tampon » d’un mètre les entourant, soit sur une surface totale de 75 m².
Dès 2010 et jusqu’en 2014, un suivi avait été mis en place sur neuf populations naturelles d’A. chamaemoly dans le cadre de mesures d’accompagnement liées à d’autres projets d’aménagements impactant cette espèce (conduites de gaz à Martigues, ligne grande vitesse Nîmes-Montpellier, contournement de Castries) (Gauthier et al., 2017). Ce suivi a été reconduit après 2014 sur quatre populations « de référence », deux localisées à moins de 5 km de la population de réintroduction (carte 2, c) et deux plus lointaines, l’une proche de l’autoroute et la dernière plus à l’intérieur des terres. Une cinquième population témoin, suivie depuis 2013 seulement, est localisée à une centaine de mètres de la zone de l’autoroute où les bulbes ont été exfiltrés avant destruction, et à moins de 5 km de la zone de réintroduction.
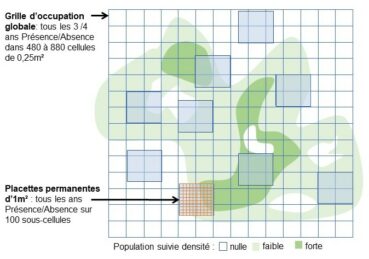
Pour cette espèce qui peut présenter des densités importantes et dont les individus peuvent, dans ce cas, être difficiles à distinguer, des suivis d’occupation en présence / absence ont été mis en place dans les cinq populations naturelles à deux échelles (figure 1) :
- un suivi annuel, à l’échelle de dix à quatorze placettes permanentes d’1 m² subdivisées en cent cellules et implantées sur une gamme de densités représentative des variations observées dans la population ;
- tous les trois-quatre ans (en 2010, 2014, 2017, 2021 et 2025), à l’échelle de « l’occupation globale » à l’aide d’une grille permanente avec des mailles de 0.25 m² recouvrant toute la population ou une partie représentative de celle-ci (120 à 220 m²) (Gauthier & Thompson, 2013 ; Gauthier et al., 2017, 2019b).
Pour analyser statistiquement les changements annuels (placettes) ou pluriannuels (occupation globale), nous avons utilisé le test du χ² de McNemar (1947). Ce test est adapté pour comparer, deux à deux, des données appariées (non indépendantes), ici des données de présence/absence d’A. chamaemoly dans 480 à 1 400 « cellules » par population lors de comptages successifs. Basé sur des données de transition, ce test ne prend en compte que les gains ou les pertes d’un comptage à l’autre et pas les « cellules » stables (présence ou absence aux deux dates). Sur la base de ce test, nous pouvons définir si les populations sont significativement en déclin, stables ou significativement en croissance.
4. Résultats
4.1. Renforcement de la population d’Iris xiphium
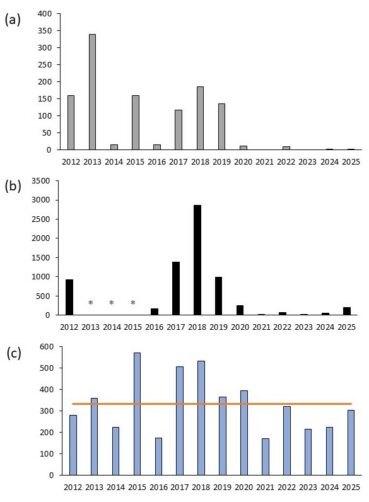
Le suivi des placettes permanentes dans les deux grandes sous-populations naturelles souligne les fortes fluctuations interannuelles de la floraison (figure 2, a). 2014 et 2016 comme toutes les années suivant 2019 sont très défavorables à la floraison, contrairement à 2013 et 2018 qui sont plutôt favorables. Les comptages de fleurs réalisés sur l’ensemble des sous-populations naturelles (grandes et petites taches) confirment la même variabilité interannuelle (figure 2, b) et les mêmes tendances annuelles. 2018 ressort comme une année de floraison exceptionnelle avec presque 3 000 fleurs comptées et confirme la représentativité de l’échantillonnage. Malheureusement ces comptages n’ont pas été réalisés de 2013 à 2015 alors que les floraisons sur les placettes permanentes étaient aussi très contrastées.
Figure 2. Variation du nombre de fleurs d’Iris xiphium : (a) dans 30 placettes permanentes dans les deux sous-populations naturelles principales et (b) dans les cinq sous-populations naturelles (* le comptage n’a pas été réalisé de 2013 à 2015) ; (c) cumul des pluies en millimètres de septembre (an-1) à mars (an 1) de 2012 à 2025 (colonnes bleus) et leur moyenne sur ces 14 années (rouge) pour la station météorologique de Béziers-Vias (34209002), https://meteo.data.gouv.fr/ ; P. Gauthier, CC-BY-NC-ND.
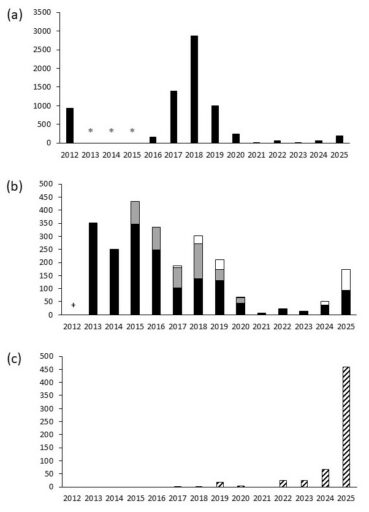
Les floraisons maximales des bulbes introduits sont observées de 2013 à 2016 (figure 3, b) pour les renforcements de 2012. Une première baisse est observée de 2017 à 2020, suivie d’une deuxième les années suivantes avec, à partir de 2021, quasiment aucune floraison dans les trois parcelles de renforcement installées en 2014. Cette diminution suit la même tendance que celle observée dans les sous-populations naturelles.
Un résultat important concerne l’apparition, en 2017, de six fleurs dans les placettes semées de graines dans trois des sept parcelles des renforcements de 2012. Cette floraison sur les placettes de semis varie d’une année sur l’autre, mais est proportionnelle au nombre de fleurs sur les placettes de renforcement de bulbes et sur les populations naturelles : de 37 en 2019, il tombe à 1 seule en 2021 pour finir à 79 en 2025. Parallèlement, dès 2017, une première tige florale apparait en dehors des placettes de translocation (figure 3, c). De 2022 à 2024, cette colonisation augmente progressivement jusqu’en 2025 avec 458 fleurs autour des placettes de renforcement pour seulement 171 fleurs à l’intérieur (92 sur les placettes de bulbes et 79 sur les placettes de graines). Cette colonisation a été observée dans six des dix parcelles de translocation avec la grande majorité autour de deux parcelles de 2012, n° 2 et n° 3 (carte 1, c), qui cumulent 389 des 458 fleurs.
Figure 3. Nombre de fleurs d’Iris xiphium observé chaque année : (a) dans les cinq sous-populations naturelles (* le comptage n’a pas été réalisé de 2013 à 2015), (b) dans les placettes de bulbes pour les sept renforcements de 2012 (noir), les trois renforcements de 2014 (gris) et les placettes de graines (blanc) (+ avant le premier renforcement) et (c) en colonisation à l’extérieur des placettes de renforcement ; P. Gauthier, CC-BY-NC-ND.
Les variations de floraison observées au niveau des taches naturelles pourraient être mises en parallèle avec la pluviométrie automnale /printanière (figure 2, c). Les années 2014, 2016 et 2021 avec une faible floraison présentaient aussi un cumul de pluie de septembre à mars très en dessous de la moyenne. Les années favorables à la floraison, sans doute avec une pluviométrie proche de la moyenne, comme en 2025, deviennent aussi de plus en plus rares.
4.2. Réintroduction d’une population d’Allium chamaemoly
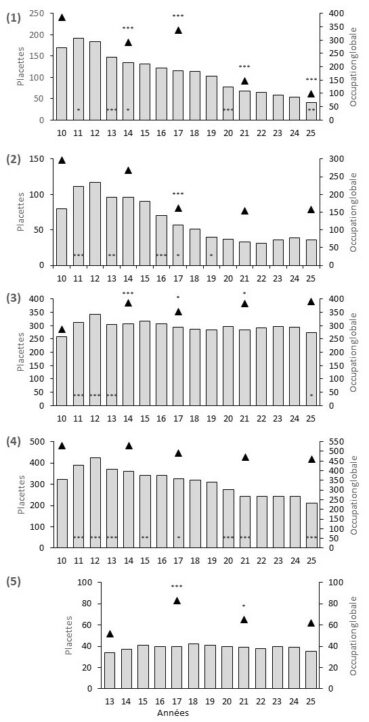
En ce qui concerne le suivi des populations naturelles de référence, pour les quatre populations suivies depuis 2010, si on compare l’occupation des placettes en 2010 et en 2025 (figure 4), la population 3 (Mèze) est stable et les trois autres diminuent (Saint-Jean-de-Védas, Maurin et Caux). Pour ces quatre populations, au cours des seize années de suivi, après une augmentation globale en 2011 et 2012, l’occupation chute en 2013. Les populations 1, 2 et 4 (Saint-Jean-de-Védas, Maurin et Caux) présentent aussi des baisses significatives d’occupation entre 2018 et 2021. Toutes les populations sont stables entre 2021 et 2024. Les populations 1, 3 et 4 (Saint-Jean-de-Védas, Mèze et Caux) baissent en 2025. La population 5 (Saint-Jean-de-Védas-Péage), suivie à partir de 2013, a une densité relativement faible et ne présente aucune variation significative d’occupation.
Figure 4. Changements annuels de l’occupation dans 10 à 14 placettes divisées en 100 cellules (histogrammes) et changement d’occupation globale (triangles noirs) dans les cinq populations naturelles d’Allium chamaemoly (1 - Saint-Jean-de-Védas, 2 - Maurin, 3 - Mèze, 4 - Caux, 5 - Saint-Jean-de-Védas-Péage.). Les changements significatifs sont : * p < 0.05, ** p<0.01, *** p<0.001 ; P. Gauthier, CC-BY-NC-ND.
À l’échelle de l’occupation globale des cinq populations, les tendances sont variables. Sur les quinze années d’étude, la population 3 (Mèze), seule stable à l’échelle des placettes, est aussi la seule qui présente une augmentation d’occupation à l’échelle globale. Pour la population 1 (Saint-Jean-de-Védas), le déclin continu observé à l’échelle des placettes se retrouve à l’échelle globale où, après un léger rebond en 2017, l’occupation baisse significativement en 2021 puis en 2025. Globalement en déclin sur l’ensemble de la période d’étude, l’occupation globale de la population 2 (Maurin) stagne suite à la forte baisse observée en 2017, alors que l’occupation des placettes continue de baisser. Pour la population 5 (Saint-Jean-de-Védas-Péage), l’occupation générale comme celle des placettes est relativement stable.
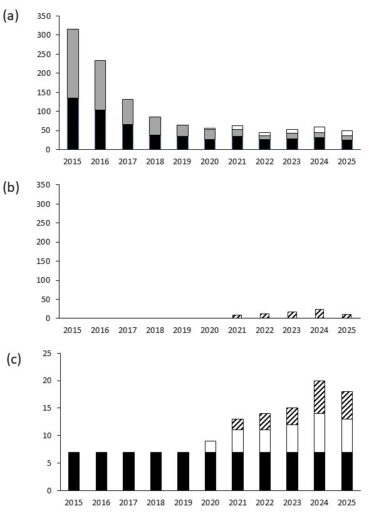
Le dénombrement des plantes en feuilles ou en fleurs sur les sept placettes de bulbes montre une chute rapide des plantes introduites de 2016 à 2019 (figure 5, a). Cette baisse ralentit à partir de 2019. En 2025, le taux d’occupation des 105 cellules où les bulbes avaient été plantés était de 26 % (27/105) et la survie des plantes introduites de 11.5 % (36/315). Les quatre placettes non protégées sont, chaque année, très perturbées par les sangliers et seulement douze plantes y ont été dénombrées en 2025 pour vingt-quatre sur les trois placettes protégées.
À partir de 2020, des plantes sont observées dans et autour des trois placettes de semis (figure 5, a) avec treize plantes dénombrées en 2025 et un maximum de seize plantes en 2024. La recherche de plantes dans une zone de 45 m² englobant les sept placettes de transplantation de bulbes met en évidence le début d’une colonisation « spontanée » à partir de 2021 : 23 plantes y ont été observées en 2024 et 10 en 2025 (figure 5, b).
En ce qui concerne la colonisation sur les 75 m² englobant les placettes de bulbes (figure 5, c) et de graines, A. chamaemoly se maintient jusqu’en 2025, malgré une très forte baisse de densité sur les sept m² où il a été réintroduit en 2015. Des plantes apparaissent à partir de 2020 sur et autour des placettes de semis et, à partir de 2021, autour des placettes des bulbes. La surface d’occupation augmente donc sur le site à partir de 2020. Elle atteint 20 m² en 2024 et retombe à 18 m² en 2025.
Figure 5. Nombre de plants d’Allium chamaemoly observé chaque année : (a) dans les trois placettes de réintroduction de bulbes protégées par une grille (noir), les quatre placettes de bulbes non protégées (gris) et les trois placettes de graines (blanc) ; (b) en colonisation à l’extérieur des placettes de réintroduction (rayé) ; (c) évolution de l’occupation (en m²) sur une surface de 75 m² englobant les zones de réintroduction de bulbes et de graines ; P. Gauthier, CC-BY-NC-ND.
5. Discussion et perspectives
Les résultats obtenus pour ces deux expérimentations indépendantes de translocation vont dans le même sens et sont particulièrement pertinents pour évaluer cette manière de contribuer à la préservation des populations des deux espèces.
5.1. Peut-on parler de succès ?
Godefroid et al. (2025) ont très récemment compilé les données disponibles à l’échelle mondiale et constaté un échec dans près de 50 % des translocations d’espèces végétales de leur analyse après cinq ans de suivi. Alors qu’une floraison a pu être observée dans la plupart des translocations étudiées, la reproduction a rarement été constatée. Ces auteurs concluent sans approfondir : « Cela soulève des questions quant à l’efficacité des approches actuelles en matière de translocation ». Force est donc de constater que les translocations comportent des risques considérables d’échec. Qu’en est-il de nos deux tentatives ?
Pour Iris xiphium, en 2017, cinq ans après la transplantation, des fleurs apparaissent dans les placettes de semis. Leur nombre varie d’une année sur l’autre, mais est proportionnel au nombre de fleurs sur les placettes de translocation de bulbes ainsi que sur les populations naturelles. Dès 2017, des fleurs en colonisation apparaissent aussi en dehors des placettes de renforcement. De 2022 à 2024, cette colonisation augmente progressivement jusqu’en 2025 avec 458 fleurs autour des placettes de renforcement pour seulement 171 fleurs à l’intérieur et seulement 194 fleurs dénombrées dans les taches naturelles. En ce qui concerne Allium chamaemoly, il se maintient et colonise spontanément les environs des zones de translocation même si le nombre de plantes comme les surfaces occupées restent très faibles.
Pour les deux espèces, le nombre de plantes qui fleurissent ou poussent à l’intérieur des placettes de translocation de bulbes diminue pendant que les espèces colonisent autour des placettes à partir de graines issues des plantes et des graines de la translocation. Cette colonisation se fait par une nouvelle génération de plantes issues des plantes d’origine et suggère, dès lors, un « succès », selon des critères de Drayton & Primack (2007, 2012) et Menges (2008). Même si la majorité des plantes transloquées a disparu (95 % des I. xiphium et 88 % des A. chamaemoly), ces expérimentations peuvent être considérées comme des succès en termes de dynamique d’une nouvelle génération. C’est particulièrement vrai pour I. xiphium, en 2025, où la nouvelle génération issue des renforcements représente 56 % des fleurs dénombrées pour seulement 23 % dans les populations naturelles et 21 % dans les placettes de renforcement.
Cependant, alors que le succès des translocations est évident, la colonisation des espaces contigus aux zones où les translocations ont été menées reste limitée. Une étape et un critère supplémentaires du succès de ces translocations seraient la dispersion de graines vers des zones plus éloignées pour la création de populations satellites, par exemple, dans les prés salés pour I xiphium.
5.2. L’importance des suivis à long terme avec témoins naturels
Depuis 2018 les translocations réalisées dans la cadre de la séquence ERC sont plutôt considérées comme des mesures d’accompagnement de la compensation que des mesures de réduction (voir les « lignes directrices pour la définition des mesures de compensation » du ministère de l’Écologie dans Alligrand et al., 2018 ; Diallo et al., 2023 ; Husse et al., 2025). Les translocations dont les résultats sont très incertains ne peuvent que compléter et renforcer d’autres mesures de compensation. Malgré cela, les translocations intègrent de plus en plus souvent les instructions dans la séquence ERC où elles devraient être conditionnées à la mise ne place d’un suivi à long terme. Notre étude montre qu’il est, en effet, fondamental d’intégrer des suivis à long terme pour évaluer le succès de ces opérations.
Tout d’abord, les deux espèces étudiées sont des géophytes. Même si elles sont très différentes, cette forme de vie avec un organe de réserve souterrain fait qu’elles peuvent se maintenir longtemps avant de péricliter. Il est donc nécessaire de prévoir un suivi à long terme (dix-vingt ans) pour conclure à leur maintien ou à leur disparition. Deuxièmement, dans le cas d’Iris xiphium les suivis reposent sur des dénombrements de fleurs : comme les plantes issues de graines peuvent mettre quatre-cinq ans à fleurir, leur installation indiquant la potentielle « réussite » d’un tel projet peut être longue à montrer. Idem, pour Allium chamaemoly, les individus juvéniles sont très difficiles à détecter et la colonisation n’a été observée qu’après cinq années de suivi. Enfin, des évènements extrêmes, comme l’augmentation en nombre et en intensité des périodes de sécheresse extrême, devraient se multiplier en raison du changement climatique (Thompson et al., 2026). Ces évènements peuvent avoir diverses conséquences sur ces espèces pérennes. Ils peuvent, par exemple, limiter leur floraison et faire conclure à tort à un échec des renforcements si seul ce paramètre est suivi.
Pour les deux espèces, le suivi simultané de populations de référence est fondamental. Le suivi réalisé dans ses taches naturelles montre qu’I. xiphium présente des variations interannuelles très importantes de floraison, de 11 fleurs en 2021 à 2746 fleurs en 2018, sans doute liées à la variation des pluies cumulées entre l’automne et le printemps. La variation d’abondance dans les parcelles de translocation suit étroitement celle des taches naturelles. Pour A. chamaemoly, depuis 2014, trois des cinq populations naturelles suivies montrent une décroissance pour l’occupation des quadrats, même si aucun évènement climatique extrême n’a été enregistré durant les hivers qui correspondent à la période de végétation des plantes. La baisse du nombre d’individus dans les translocations serait donc plus probablement liée à des changements environnementaux et à d’autres facteurs qui impacteraient négativement les populations (dégâts de sangliers, baisse du pâturage ovin et fermeture du milieu) qu’à un échec des translocations. Aucun froid extrême comme celui de février 2012 qui avait impacté les populations naturelles déjà suivies n’a été observé (Gauthier et al., 2017).
5.3. L’importance de translocations massives
Plusieurs synthèses (comme Godefroid et al., 2025) ont montré que le faible nombre de plantes (moins de cent) sur lequel reposent souvent les translocations fragilise, dès le départ, leur persistance à long terme. Ainsi, Silcock et al. (2019) préconisent l’utilisation d’au moins cinq cents individus pour augmenter la viabilité des populations dans les sites de translocation. Pour la région et la flore méditerranéenne, Thompson et al. (2026) insistent sur l’importance fondamentale d’utiliser de grands échantillons de juvéniles, bulbes et/ou graines dans les expérimentations de translocation. Pour ces auteurs, le renforcement de populations des espèces à distribution « ibéro-provençale », rares dans le sud de la France où elles sont en limite nord de leur aire de répartition mais abondantes dans la péninsule Ibérique, fait partie d’une nouvelle stratégie à mettre en place pour conserver la flore dans un climat changeant.
Une vaste expérimentation de renforcement / réintroduction a ainsi été menée, en 2019, dans le Parc national des Calanques à Marseille, sur Astragalus tragacantha L. dont les populations étaient en régression sur une aire de répartition restreinte (Affre et al., 2022). 4 532 plantules ont été transplantées sur douze sites doublant presque les effectifs naturels d’A. tragacantha. Après trois ans, en 2022, le taux de survie était de 32 % et six plantes fructifiaient. Plusieurs opérations de renforcement de Centaurea corymbosa Pourr. impliquant un nombre important d’akènes ont été menées sur le massif de la Clape (Aude) d’où l’espèce est endémique. 1 050 akènes en 1994 et 900 en 1995 (Colas et al., 2008), puis 10 000 de 2018 à 2022 (Imbert & Ducrettet, 2023) ont été utilisés afin d’essayer de « sauver génétiquement » les sous-populations naturelles.
Dans notre étude, les renforcements d’I. xiphium (1 850 bulbes et 12 250 graines) ont été réalisés dans un but explicite de conservation, à l’initiative d’une équipe de recherche et d’organismes de gestion. Ils répondent mieux aux critères de nombre que les réintroductions mises en place pour A. chamaemoly dans le cadre de mesures d’accompagnement d’un projet d’aménagement qui reposent sur un nombre plus restreint de propagules (350 bulbes et 1200 graines).
5.4. Semer des graines ou planter des bulbes ?
Dans une revue de plusieurs dizaines de translocations, Vaudey et al. (2011) ont trouvé plus de succès en termes de persistance d’une population dans les translocations menées avec des bulbes matures et des bulbes juvéniles qu’avec des graines. Pour les deux espèces de géophytes étudiées ici, les translocations ont combiné l’utilisation de graines et de bulbes. Les bulbes sont relativement faciles à manipuler et, en accumulant des réserves, permettent de résister lors d’années défavorables, contrairement aux plantules qui pourront mourir, par exemple lors de sécheresses ou de froids extrêmes. Dès la première année, une partie des bulbes des deux espèces a fleuri et produit des graines, ce qui constitue un avantage par rapport aux semis de graines qui vont mettre plusieurs années à fleurir et à fructifier.
En même temps, les graines sont faciles à manipuler (peu d’espace de conservation nécessaire) et à introduire (pour des plantes de parois ou de falaise, par exemple) mais nécessitent la maîtrise du taux de germination. Ces taux de germination ont, par exemple, été utilisés pour calibrer les expérimentations de renforcement de Centaurea corymbosa (Imbert & Ducrettet, 2023). De plus, les premiers stades suivant la germination sont généralement fragiles et peuvent nécessiter une gestion (arrosage, ouverture du milieu…). Pour Astraglus tragacantha, en raison du faible taux de germination des graines in natura, l’expérimentation s’est reportée sur l’utilisation de plantules issues de graines scarifiées et stratifiées (Affre et al., 2022). Pour I. xiphium (Max Debussche, comm. pers.) et A. chamaemolly (Perrine Gauthier, inédit), des expérimentations préalables avaient montré un taux de germination élevé sans levée de dormance nécessaire. En effet, pour les deux espèces, des plantes ont été observées sur les placettes de semis au bout de cinq années, temps nécessaire à I. xiphium pour fleurir et à A. chamaemoly pour que ses plants soient détectables. À long terme, les graines peuvent donc être bénéfiques pour l’installation d’une population viable.
En conclusion, les translocations de bulbes et de graines sont complémentaires lorsqu’elles permettent l’installation d’une population reproductrice sur le long terme
5.5. La gestion des placettes de translocation
Des variations importantes des taux de survie/floraison ont été constatées au niveau des différentes parcelles de renforcement d’I. xiphium. Elles indiquent une micro-niche plus ou moins favorable malgré les recherches approfondies préalables au choix de ces parcelles (Lorin, 2012). Dans l’éventualité de reconduire des expérimentations similaires, il faudrait travailler à une échelle encore plus fine, de l’ordre de la taille des placettes de renforcement (1 m²) pour choisir les zones les plus propices.
Les années favorables à la floraison, sans doute avec une pluviométrie proche de la moyenne, comme en 2025, deviennent aussi de plus en plus rares, d’où la nécessité de suivis à long terme. Les différences entre les deux taches naturelles pourraient aussi s’expliquer par des fonctionnements hydrologiques différents en termes des nappes d’eaux douces et salées. Une étude hydrologique/micro-topographique et de salinité des sols du site pourrait peut-être aider à comprendre les variations interannuelles et entre taches naturelles mises en évidence par le suivi. Sur ce point, on pourrait rappeler Flahault (1897) qui considérait que les zones littorales ne sont pas « vraiment » méditerranéennes, car déterminées plus par le sel que par le climat. Pour lui, I. xiphium (observé dans la Narbonnaise) figure parmi les espèces exigeant de l’eau (comme Schoenus nigricans, par exemple) et pour lesquelles « le sel paraît secondaire ».
Enfin, sur le site d’I. xiphium, le pastoralisme historiquement présent depuis plusieurs décennies a été abandonné au début des translocations. Remettre en place du pastoralisme en fin d’été et à l’automne, après la dissémination des graines, pourrait être intéressant afin de réduire la densité des plantes herbacées et des grandes graminées compétitrices sur le site.
Pour A. chamaemoly le déclin continu observé à l’échelle des placettes est probablement lié à l’activité des sangliers, dont le contrôle est un élément clé dans la gestion du site et la réussite de la réintroduction. Il existe un écart entre les placettes protégées et non protégées : huit individus d’A. chamaemoly ont été dénombrés en moyenne dans les premières et pour seulement trois en moyenne dans les secondes. Même si la végétation se densifie sous les grilles de protection qui empêchent le pâturage et complexifient les dénombrements, ces grilles ont un rôle de protection efficace.
Enfin, cette étude souligne la nécessité d’ouvrir le débat sur la migration assistée des espèces en dehors des limites de leur aire de répartition actuelle comme un élément de la stratégie de leur conservation. Cette pratique, très critiquée dans la littérature scientifique, pourrait néanmoins être employée afin d’aider de nombreuses espèces à coloniser des habitats qu’elles n’atteindraient pas par dispersion naturelle, notamment en raison de la fragmentation importante des habitats naturels.
Bibliographie
Affre L., Dumas E., Dupin A., Labat S., Miché L., Panzani L. & Ugo J., 2022. Guide de gestion des habitats littoraux et des espèces associées. LIFE16 NAT/FR/000593. Agence régionale pour la biodiversité et l’environnement Provence-Alpes-Côte d’Azur, 188 p.
Alligand G., Hubert S., Legendre T., Millard F. & Müller A., 2018. Évaluation environnementale. Guide d’aide à la définition des mesures ERC. Service de l’économie, de l’évaluation et de l’intégration du développement durable, 133 p., https://www.ecologie.gouv.fr/sites/default/files/publications.
Bolòs O. (de) & Vigo, J., 1984-2001. Flora del Països catalans (vol. 1-4). Barcino, Barcelona, 3 713 p.
Diallo M., Mayeur A., Vaissière A.-C. & Colas B., 2023. The relevance of plant translocation as a conservation tool in France. Plant Ecology 224 : 777-790, https://doi.org/10.1007/s11258-023-01295-4
Flahault C., 1897. La distribution géographique des végétaux dans la région méditerranéenne française. Lechevalier, Paris, 178 p.
Gauthier P. & Thompson J.D., 2013. C’est possible : suivre une population sans pouvoir identifier les individus. Espaces naturels 41 : 27.
Gauthier P., Pons V., Letourneau A., Papuga G. & Thompson J.D., 2017. Combining population trends with criteria for habitat vulnerability to assess the conservation status of populations of rare and endangered plants. Journal for Nature Conservation 37: 83-95, https://doi.org/10.1016/j.jnc.2017.03.005.
Gauthier P., Bernard C. & Thompson J.D., 2019a. Exploring vulnerability of listed Mediterranean plants in relation to risks of population loss. Journal for Nature Conservation 51 : article 125736, https://doi.org/10.1016/j.jnc.2019.125736.
Gauthier P., Pons V., Fisogni A., Murru V., Berjano R., Dessena S., Maccioni A., Chelo C., Doncieux A., Papuga G. & Thompson J.D., 2019b. Assessing vulnerability of listed Mediterranean plants based on population monitoring Journal for Nature Conservation 52 : article 125758, https://doi.org/10.1016/j.jnc.2019.125758.
Godefroid S., Piazza C., Rossi G., Buord S., Stevens A.-D., Aguraiuja R., Cowell C., Weekley C.W., Vogg G., Iriondo J.M., Johnson I., Dixon B., Gordon D, Magnanon S., Valentin B., Bjureke K., Koopman R., Vicens M., Virevaire M. & Vanderborght T., 2011. How successful are plant species reintroductions? Biological Conservation 144 : 672-682, https://doi.org/10.1016/j.biocon.2010.10.003.
Godefroid S., Lacquaye S., Ensslin A., Dalrymple S., Abeli T., Branwood H., Ferrando Pardo I., Ferrer Gallego P.P., Zippel E., Gouveia L., Lobo C.A., Fernandes F., Rasp M., Daco L., Séleck M., Frankard Ph., Fischer L.K., Koutsovoulou K., Finger A., Valkó O., Garfi G., Španiček B., Bürli S., Dickenmann R., Jones J., Guyonneau J., Papuga G., De Vitis M., Fenu G., Van Rossum F., Cogoni D., Foster G., Julien M., Piqueray J., Vít P., Bonnet V., Carta A., Descombes P., Lazarević M., Müller N., Orsenigo S., Ravera S., Sild M., Smyth S., Wagner T.C., Walisch T., Ballian D., Cambria V.E., Colas B., Dixon L., Draper D., Froidevaux V., Pagitz K., Pánková H., Pankhurst T., Preston J., Prunier P., Saura-Mas S., Sartori K., Socher S.A., Stanik N., Wunderli A., Nikowitz T. & White F.J., 2025. Current state of plant conservation translocations across Europe: motivations, challenges and outcomes. Biodiversity and Conservation 34 : 769-792, https://doi.org/10.1007/s10531-025-03013-0.
Husse S., Andrieu F. & Klesczewski M., 2025 Translocation de plantes vivaces protégées comme mesure compensatoire : deux retours d’expériences d’Occitanie. Carnets botaniques 273 : 1-15, https://doi.org/10.34971/K3N4-0A32.
Imbert E. & Ducrettet J., 2023. Projet RENPOP RENforcement des POPulations comme source de sauvetage évolutif, rapport final. OFB-Labex Cemeb, Montpellier, 39 p.
Lorin T., 2012. Renforcement et création de nouvelles populations sur le seul site connu d’Iris xiphium en France. L3 Biologie fondamentale, Ecole normale supérieure de Lyon.
McNemar Q., 1947 Note on the sampling error of the difference between correlated proportions or percentages. Psychometrika 12 : 153-157.
Médail F. & Diadema K., 2006. Biodiversité végétale méditerranéenne et anthropisation : approches macro et micro-régionales. Annales de Géographie 651 : 618-640, doi 10.3917/ag.651.0618.
Menges E.S., 2008. Restoration demography and genetics of plants: when is a translocation successful? Australian Journal of Botany 56 :187-196, https://doi.org/10.1071/BT07173.
Nervo L. (de), 2011. Renforcement, réintroduction ou introduction assisté : quelle méthodologie pour choisir des sites pour une véritable « compensation écologique » dans le cadre de la destruction de populations d’espèces végétales protégées ? M2 EBE, Université de Paris 11 et AgroParisTech.
Pavlik B.M., 1996. Defining and measuring success. In D.A. Falk, C.I. Millar & M. Olwell (eds), Restoring Diversity: Strategies for the Reintroduction of Endangered Plants, Island Press, Washington DC (USA) : 127-155.
Primack R.B. & Drayton B., 1997. The experimental ecology of reintroduction. Plant Talk 11 : 25-28.
Silcock J.L., Simmons C.L., Monks L., Dillon R., Reiter N., Jusaitis M., Vesk P.A., Byrne M. & Coates D.J., 2019. Threatened plant translocation in Australia: a review. Biological Conservation 236 : 211-222, https://doi.org/10.1016/j.biocon.2019.05.002.
Thompson J.D., 2020. Plant evolution in the Mediterranean. Insights for conservation. Oxford University Press, Oxford, 439 p.
Thompson J.D., Papuga G., Gauthier P. & Fauché M., 2026. Plant conservation in a changing Mediterranean world. Plants People Planet 8 : 49-72, https://doi.org/10.1002/ppp3.70036.
Vaudey V., Debussche M. & Thompson J.D., 2011. Renforcement ou création de nouvelles populations pour le sauvetage des espèces végétales : choix méthodologiques. In J.D. Thompson & P. Gauthier (eds), Activités humaines et dynamique de la biodiversité en région méditerranéenne. Problématique scientifique, enjeux de conservation, CEFE & MédiaTerra, Montpellier : 57-58.
Vellend M., Verheyen K., Jacquemyn H., Kolb A., Van Calster H., Peterken G. & Hermy M., 2006. Extinction debt of forest plants persists for more than a century following habitat fragmentation. Ecology 87 : 542-548, https://doi.org/10.1890/05-1182.
Zecchini A., 1998. La nature en sursis. Le Monde Diplomatique 28.
Remerciements
L’ensemble des travaux sur l’Iris d’Espagne a été réalisé en étroite collaboration avec les différents organismes de gestion intervenant sur le site : l’opérateur du site Natura 2000 (Communauté d’agglomération Hérault Méditerranée), le Conservatoire des espaces naturels Occitanie, le Conservatoire du littoral et le Conservatoire botanique national méditerranéen. Plusieurs opérations de sensibilisation du grand public ont été menées. De 2013 à 2016 puis en 2025, au mois de juin, les élèves de l’école primaire de Portiragnes nous ont rejoints sur le site pour réaliser le suivi annuel. Au printemps 2014, la classe a même participé à la deuxième série de renforcements. En 2014, un panneau de sensibilisation sur la vulnérabilité d’Iris xiphium a été réalisé et implanté jusqu’en 2020 près de la plus grande tache où les fleurs étaient régulièrement cueillies par les promeneurs.
Les réintroductions d’Allium chamaemoly ont été menées en collaboration avec le CEN-Occitanie et les Écologistes de l’Euzières et les suivis des populations naturelles ou de réintroduction ont été financés par différents programmes : programme « ITTECOP » du projet « INTERMOPES », GRT Gaz (contrat 048522), GPMM (contrat 060235) et Autoroutes du Sud de la France (contrat 093034).
Les auteurs remercient vivement Pauline Durbin, Pauline Bernard, Valentina Murru, Simone Dessena, Alfredo Maccioni, Thibaut Lorin et David Doblas pour leur aide précieuse sur le terrain.