La mousse de poche portuguaise (Fissidens curvatus Hornsch., 1841, Fissidentaceae) sur la marge orientale du Massif central (Auvergne-Rhône-Alpes, France)
Title
Portugese pocket moss (Fissidens curvatus Hornsch. 1841, Fissidentaceae) on the eastern Massif central margin
Résumé
Fissidens curvatus Hornsch., 1841 (Fissidentaceae) compte parmi les plus petites espèces de fissident d’Europe. Il est largement méconnu en France du fait de sa petite taille et de sa distribution limitée à une partie de la frange méditerranéo-océanique. C’est au cours de l’inventaire de l’espace naturel sensible nord-ardéchois des 3D, en 2022, que cette espèce fut découverte. Cette nouvelle localité apporte une perspective nouvelle dans l’appréhension de la chorologie de l’espèce en France métropolitaine, ce fissident ayant jusque-là toujours été observé à quelques dizaines de kilomètres des franges littorales. Les aspects nomenclaturaux d’une synonymie riche et complexe sont abordés. La singularité morphologique de ce fissident minuscule sont mis en exergue. Sa chorologie s’ensuit d’un historique détaillé des observations dans l’hexagone, puis d’une esquisse des contours de son enveloppe écologique. Enfin, les aspects climatiques, géologiques et topographiques du contexte cévenol favorables à l’espèce sont précisés.
Abstract
Fissidens curvatus Hornsch., 1841 (Fissidentaceae) is among the smaller European species. It’s unknown in France due to its very little size and its distribution limited to the edge Mediterranean and oceanic. In 2022, this species was discovered during the inventory of the natural space sensible called “3D” which is located in the north-east of Ardèche department. This new population give a new outlook in the way to analyze and explain its distribution in France. Indeed, this species has never been mentioned to more several ten kilometers from the coastline. Nomenclatural features of the rich and complex synonymy are detailed. The originality of morphological features of this tiny species are highlight. Its chorology is followed by a detailed historic of French observations, then by a description of its ecology. Finally, climatical, geological and topographical angles of the cévenol situation suitable to Fissidens curvatus are precised.
1. Introduction
Le Fissident courbé Fissidens curvatus Hornsch., 1841[1]– qui mesure tout au plus quelques millimètres de haut – compte parmi les plus petites espèces de fissidents d’Europe. Le nom anglais très imagé qui lui a été attribué insiste sur cette taille réduite : Portugese pocket moss, littéralement la mousse de poche portugaise.
En dépit de caractéristiques morphologiques univoques, cette espèce compte un assez faible nombre d’observations en France et dans les pays limitrophes. Nombre de mentions historiques n’ont pas été confirmées ces dernières décennies, que ce soit en France métropolitaine, au Royaume-Uni où seules quatorze mailles de présence parmi les dix-neuf existantes ont fait l’objet d’observations récentes, et ce malgré une pression d’observation conséquente (Blockeel et al., 2014). La grande discrétion de ce taxon réputé méditerranéo-océanique en Europe (Düll, 1984) ainsi que sa rareté, voire son absence dans un grand nombre de régions naturelles européennes, en font une espèce méconnue de la majorité des bryologues. Comme souvent en bryologie, pour trouver régulièrement une espèce, il faut a minima connaître son existence, quelques-unes de ses caractéristiques morphologiques et écologiques. Les trente-deux observations récentes de France métropolitaine proviennent de seulement sept observateurs et plus de la moitié des données sont méditerranéennes et issues de seulement deux observateurs. La pression d’observation est-elle trop faible dans les territoires favorables à l’espèce ? Ce fissident passe-t-il inaperçu à travers l’abondance d’autres espèces étant donné sa petite taille et une certaine difficulté dans le genre Fissidens ?
F. curvatus a été découvert en 2022 dans le département de l’Ardèche, suite à la collecte de substrat in situ pour une analyse au laboratoire plus approfondie sous forme d’un relevé bryosociologique. L’éloignement à la côte méditerranéenne de la population ardéchoise dénote vis-à-vis des autres localités françaises et européennes, elle apporte de nouvelles perspectives dans l’appréhension de la chorologie de l’espèce à l’échelle de la France.
Outre des rappels quant aux aspects nomenclaturaux, la morphologie de l’espèce, la chorologie et l’enveloppe écologique de l’espèce sont détaillées en Europe et plus spécialement en France.
2. Une synonymie riche et complexe
Fissidens curvatus est un élément du sous-genre Fissidens : il présente un péristome « de type bryoides », un nombre de cellules exothéciales à la périphérie de l’apex de la capsule supérieur à trente-deux et des cellules lisses pour la grande majorité des échantillons (Bruggeman-Nannenga & Pursell, 1995 ; Bruggeman-Nannenga, 2021). Dans le genre Fissidens, il compte parmi les espèces les plus largement répandues dans le monde : Afrique du Sud, Europe, Amérique du Sud, Amérique du Nord, Australie et Asie.
F. curvatus est une plante qui présente une grande variabilité morphologique et une large synonymie (Bruggeman-Nannenga, 1995), en partie induite par la distribution cosmopolite de l’espèce. Pas moins de cinquante-neuf synonymes sont actuellement reconnus (https://www.worldfloraonline.org/taxon/wfo-0001193312).
L’espèce apparaît à travers les publications historiques principalement sous le nom de Fissidens algarvicus Solms., 1868. En effet, cette espèce est décrite sur la base de matériel provenant de la région de l’Algarve, expliquant l’origine de l’épithète algarvicus et le nom anglais de mousse de poche portugaise. Hermann Maximilian Carl Ludwig Graf zu Solms Laubach (1842-1915), connu par ailleurs sous le nom de M. le Comte de Solms-Laubach (https://www.societe-botanique-alsace.org/botanistes-dalsace/solms-laubach/), professeur de botanique, spécialiste en systématique, en morphologie végétale et en paléontologie et éminent bryologue (photo 1), découvre Fissidens curvatus à l’oppidum de Silves, ville historique et ancienne capitale de l’Algarve, sur des argiles humides au pied d’un poirier, dans une tonsure de pelouse, associé à Ditrichum subulatum Hampe, 1867. L’espèce est décrite en mai 1868, dans le cadre de sa thèse Tentamen Bryo-Geographiae Algarviae regni Lusitani provinciae (Solms-Laubach, 1868) concrétisant son habilitation à la phytogéographie des mousses du Portugal. L’holotype est aujourd’hui conservé dans une collection entreposée à Lehmann (région de Brandebourg, Allemagne).
Par ailleurs, l’abbé Boulay et Pierre-Tranquille Husnot, dans leur bryoflore respectives (Boulay, 1884 ; Husnot, 1884) traitent tous deux Fissidens algarvicus comme une variété de F. pusillus [Fissidens pusillus var. algarvicus (Solms) Boulay ex Husn., Fissidens incurvus var. algarvicus (Solms) Husn.]. Ce dernier estime que ce taxon « tient de trop près des formes dioïques de Fissidens pusillus pour en être séparée spécifiquement ».
En 1995, Fissidens algarvicus Solms., 1868 est défini comme synonyme de F. curvatus (Bruggeman-Nannenga & Pursell, 1995), ce dernier décrit en 1827 dans Linnaea, 15 : 148, 1841 par l’illustre botaniste allemand Christian Friedrich Hornschuch (1793-1850). En l’absence d’un type associé à la description de l’espèce, un échantillon collecté le 24 octobre 1827 par Christian Friedrich Ecklon, « sur un mur du jardin de Monsieur Auret, sous le dos du lion » fut défini comme lectotype (Magill, 1981).
3. Un fissident singulier
C’est une espèce qui passe facilement inaperçue du fait de sa taille miniature et de son apparition régulière sous forme de populations réduites (Smith, 2004). Difficile à détecter sur le terrain, l’espèce peut aisément être confondue in situ et surtout passe inaperçue car apparaissant en une sous-strate d’autres fissidents terricoles communs comme Fissidens bryoides.
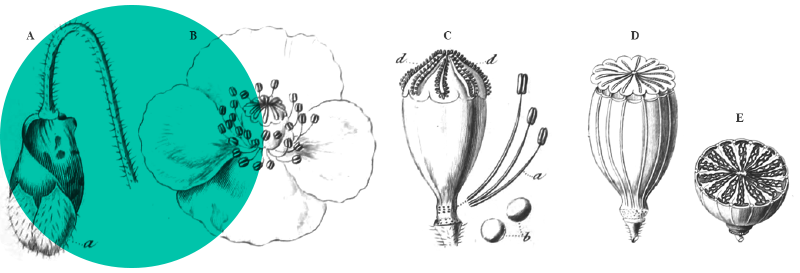
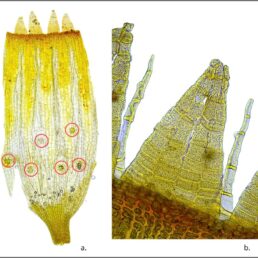
F. curvatus se distingue aisément des autres fissidents européens par sa singularité morphologique. En premier lieu, l’espèce présente une dimorphie patente entre individus stériles et fertiles, souvent associés dans une même touffe. Les individus feuillés stériles, qui sont beaucoup plus grands et densément feuillés que les individus fertiles, atteignent 4 mm de haut pour 0,6-1 mm de large et sont composés de 4-16 paires de feuilles, tandis que les individus fertiles atteignent tout au plus 1,5 mm de haut pour 0,8 mm de large et se composent de trois paires de feuilles (Xing-jiang, 2001) (planche 1 : 1). Les feuilles sont bordées d’un limbidium formant un bourrelet épais qui fusionne avec une nervure percurrente à ± longuement excurrente (planche 1 : 3, 4). L’abbé Boulay et Pierre-Tranquille Husnot (Boulay, 1884 ; Husnot, 1884) insistent à juste titre sur le caractère jaunâtre et épais du limbidium. Les feuilles sont, depuis le milieu du limbe, progressivement et longuement rétrécies en en apex aigu (Erzeberger, 2016), les supérieures se caractérisant par un acumen prononcé occupant 8-20 % de leur longueur totale (planche 1 : 5, 6, 7, 9, 11).
L’aréolation foliaire est constituée de cellules rectangulaires ou hexagonales au moins deux fois aussi longues que larges (planche 1 : 12, 13, 14) (Guerra & Brugués, 2015). Toutefois, la forme des cellules apparaît relativement variable (Magill, 1981). La description originelle de l’espèce indique des cellules munies de petites papilles espacées. Toutefois, ce trait dénote avec la majorité des échantillons en herbiers qui possèdent des cellules lisses (Erzberger, 2016).
En Europe, l’espèce a jusque-là toujours été observée sous une forme dioïque. Les capsules ne sont pas rares. Produites dans environ 50 % des populations (Erzberger, 2016), celles-ci sont matures dès l’hiver et jusqu’au début du printemps.
L’espèce se décline en deux variétés (https://www.anbg.gov.au/gardens/) : la variété curvatus se reconnaît à son limbidium complet – ou quasiment complet – sur toutes les feuilles, tandis que la variété inclinabilis (Müll. Hal. ex Dixon) J.E. Beever (mentionnée notamment en Australie) se différencie par son limbidium vestigial ou absent sur les lames dorsales et apicales. Les capsules sont généralement arquées, mais peuvent parfois être droites (Flora of North America editorial committee, 2007 ; Magill, 1981).
La forme du limbe, les caractéristiques du limbidium, l’aréolation foliaire et la taille de la plante permettent d’éviter toute confusion avec les deux autres fissidents terricoles à limbidium communs en Europe, à savoir Fissidens bryoides et F. viridulus. La vigilance est néanmoins de mise du fait de l’existence de formes aberrantes chez ces deux derniers taxons qui peuvent surprendre le bryologue.
4. Un élément des régions australe et tropicale…
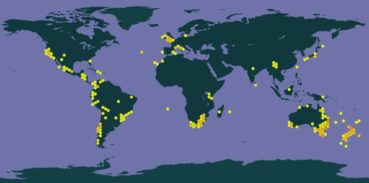
Fissidens curvatus est un élément appartenant aux régions australe – zone centrée sur la zone tempérée de l’hémisphère sud – tropicale et subméditerranéenne capable d’incursions en Europe tempérée de par son affinité (sub)-océanique (Dierßen, 2001). L’espèce est répertoriée dans les régions plus chaudes de l’Asie (Inde, Chine, Japon, Philippines), sur les continents américain (Californie, Antilles, Amérique centrale, Amérique du Sud) et africain (Maroc, Tunisie, Afrique du Sud), au Proche et Moyen-Orient (Turquie, Iran) mais aussi en Australie et Nouvelle-Zélande (carte 1).
Largement distribuée dans le monde, considérée comme appartenant aux éléments méditerranéo-océaniques à l’échelle européenne (Düll, 1984), Fissidens curvatus est relativement rare et localisée en Europe. On le retrouve en Macaronésie, en Afrique du Nord (Maroc, Tunisie), dans la péninsule Ibérique (Portugal au nord de Lisbonne, Espagne dans la région de Valence), dans le bassin méditerranéen de France métropolitaine, en Grèce (Crète), en Croatie, dans l’est de l’Europe (Slovaquie et Hongrie) et sur la frange atlantique (Bretagne et Normandie, sud-ouest de l’Irlande, de l’Angleterre et du Pays-de-Galles) (Blockeel et al., 2014).
Le genre Fissidens est cosmopolite à dominante tropicale et comporte 400 à 500 espèces dans le monde. Ainsi, le bryologue peut, pour l’identification des petits fissidents terricoles, se référer ponctuellement à des flores de territoires (sub-)tropicaux et tout particulièrement à celle d’Afrique du Sud. En effet, les différentes variantes du climat méditerranéen et la situation latitudinale d’Afrique du Sud sont propices à l’expression de ces petites acrocarpes. Par ailleurs, le genre Fissidens est particulièrement bien connu dans ce territoire puisqu’il est étudié de près par l’une des meilleures spécialistes mondiales. En Afrique du Sud, Fissidens curvatus peut être confondu avec d’autres espèces à lame engainante ouverte : F. beckettii, F. magnicellulatus, F. rufescens, F. pygmaeus.
5. …Disséminé dans le bassin méditerranéen et sur la façade océanique
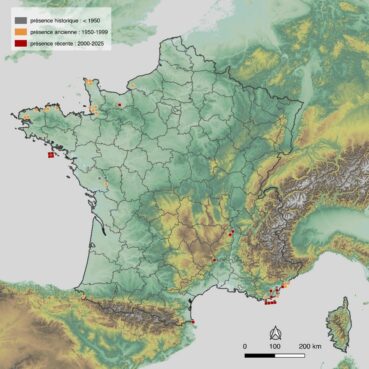
En France métropolitaine, Fissidens curvatus occupe le bassin méditerranéen et la frange océanique (carte 2). Au sud-ouest, l’espèce est uniquement mentionnée au début du xxe siècle dans les Pyrénées-Atlantiques, à Banca : tout d’abord en 1907 par Gabriel Dismier, puis en 1935 par Pierre Allorge, deux bryologues de renommée internationale.
Plus au nord le long de la façade atlantique, Joseph Charrier l’observe entre 1923 et 1958 au sein du Bocage vendéen et la Gâtine, dans les départements des Deux-Sèvres (Saint-Amand-sur-Sèvre) et de la Vendée (Saint-Hilaire-de-Voust, Montournais, Monsireigne) (Charrier, 1958). Tandis que Belle-Île-en-Mer dans le Morbihan accueille les trois seules « populations » récemment observées en Bretagne (Durfort et al., 2021), les côtes nord de la pointe bretonne enregistrent six localités historiques réparties dans les départements du Finistère (Brest, Guipavas, Saint-Pol-de-Léon) et des Côtes-d’Armor (Lannion, Saint-Michel-en-Grève) (Gaume, 1956). En Normandie, l’espèce a principalement été observée, entre 1889 et 1938, aux extrémités nord et sud du département de la Manche (Cherbourg-Octeville, Gavray-sur-Sienne, Martinvast, Le Mesnil-Garnier, Saint-Pair-sur-Mer, Saint-Senier-sous-Avranches, Sartilly-Baie-Bocage) (Potier de la Varde, 1923, 1938 ; Frémy & Meslin, 1927 ; Corbière, 1889). En 2016, l’espèce est récemment découverte par Julien Lagrandie dans le département du Calvados, à Soumont-Saint-Quentin (Durfort et al., 2017). Enfin, en 1900, Irénée Thériot, grand nom de la bryologie française, mentionne Fissidens curvatus dans la commune seinomarine d’Épretot (Thériot, 1890).
C’est le bassin méditerranéen qui abrite aujourd’hui le plus grand nombre de populations de l’espèce et, contrairement au domaine atlantique, il s’agit là de mentions majoritairement récentes. À l’ouest du bassin méditerranéen, dans les Pyrénées-Orientales, deux localités sont signalées. Adolphe-Henri Duterte, en 1886, situe l’espèce à Amélie-les-Bains-Palalda (Duterte, 1887). Puis dans la seconde moitié du xxe siècle, l’espèce est observée en plusieurs emplacements de Banyuls-sur-Mer (Allorge, 1958 ; Zanten & During, 1974) avant d’être confirmée plus récemment en 2004 (Aicardi, 2005). Il faut se déplacer quelques centaines de kilomètres plus à l’est, dans les Bouches-du-Rhône, pour trouver une autre population de Fissidens curvatus, celle-ci découverte en 2007 par Jean-Pierre Hébrard, à Arles, près de la bergerie de Négueiron (Hébrard, 2009). La grande majorité des observations françaises de l’espèce se cantonnent au littoral varois : l’espèce est respectivement observée durant la première moitié du xxe siècle à Hyères, Saint-Raphaël, la Croix-Valmer, Le Muy, Roquebrune-sur-Argens et Ramatuelle (Corbière & Jahandiez, 1921 ; Dismier, 1920 ; Squivet d Carondelet, 1961 ; Crundwell & Whitehouse, 1976 ; Hébrard, 1978). En 2005, l’espèce est retrouvée en différents emplacements de l’île de Porquerolles (Hugonnot, 2007a). Puis, l’aire de répartition de l’espèce s’affine dans le Midi avec des observations au Cannet-des-Maures (Hugonnot, 2007b), au Lavandou (Skrzypczak, 2009) ainsi qu’à Bormes-les-Mimosas et Sainte-Maxime (inventaires menés par l’Office national des forêts et le Conservatoire botanique méditerranéen de Porquerolles). Notons également deux populations maralpines mentionnées en 1917 par Gabriel Dismier dans les communes de Cannes et de Mandelieu-la-Napoule (Dismier, 1920). Enfin, Fissidens curvatus est observée en trois localités du littoral de Haute-Corse : Calvi, Olmeta-di-Capocorso, Osani (Hébrard, 1988 ; Sotiaux et al., 2007).
Parmi les soixante-quatre planches d’herbier accessibles depuis l’interface e-recolnat (https://explore.recolnat.org) sous les identités de Fissidens curvatus et F. algarvicus, trente-sept étaient associées à des observations européennes dont vingt-cinq issues de France métropolitaine, provenant très majoritairement de l’herbier Louis Corbière (Normandie, Bretagne). La vérification de parts d’herbiers provenant de l’île de Madère a montré l’existence d’une confusion en contexte macaronésien avec deux autres fissidents : F. sublineaefolius et F. coacervatus (Lobo et al., 2011). Aucune part d’herbier n’a été vérifiée dans le cadre du présent travail. Bien qu’aucune mention française ne semble irréaliste, des erreurs d’identification peuvent bien évidemment exister.
6. Une espèce pionnière des sols argileux
En Europe, et en particulier en France, Fissidens curvatus est très majoritairement observé à l’étage planitaire (étage mésoméditerranéen et méditerranéen inférieur en région méditerranéenne), à une altitude de 40-290 m (Blockeel et al., 2014), jusqu’à 1 000 m sur l’île macaronésienne de Madère (Lobo et al., 2011), sur des substrats géologiques de natures variées : gneiss, granite, grès, rhyolite, schistes, calcaires.
Cette plante pionnière est une subneutrophyte (pH 5.7–7.0), mésotrophile à mésoeutrophile (Dierßen, 2001), et semble préférer les situations semi-ombragées à ombragées. Elle investit les terres nues, à dominante argileuse.
Les localités situées à l’extérieur du bassin méditerranéen sont presque systématiquement associées à une exposition sud. Elle est très souvent détectée dans les tonsures des végétations herbacées parmi les chênaies pubescentes, yeuseraies ou pinèdes relevant des Quercetea ilicis et parfois dans les maquis littoraux relevant des Cisto-Lavanduletea, que ce soit en Europe, mais également en Australie ou en Nouvelle-Zélande dans des habitatshomologues (Flora of North America editorial committee, 2007).
Noter que les observations se rapportent très majoritairement à des situations anthropiques : talus en bord de route ou de sentier et plus rarement fossés, murets comportant des anfractuosités terreuses dans les villages (Lobo et al., 2011 ; Blockeel et al., 2014). En se comportant en tant que pionnière terricole thermophile et hygrophile temporaire, fréquemment citée en compagnie d’autres terricoles pionnières telles que Epipterygium tozeri, Fissidens viridulus et Weissia controversa (Blockeel et al., 2014), elle s’intègre dans des communautés qui sont à rapprocher du Fissidenti serrulati-Fossombronienion angulosae[2] Marstaller 1993 (communautés des sols limono-argileux mésoxéroclines caractérisées par la présence d’Epipterygium tozeri, Fossombronia angulosa, Fissidens serrulatus, Scapania compacta, Scleropodium touretii et Cephaloziella turneri ; Dierßen, 2001 ; Bardat & Hauguel, 2002) et du Mannion androgynae Ros & Guerra 1987 (communautés méditerranéennes à développement printanier des replats à inondation hivernale, caractérisée par la présence de Mannia androgyna, Riccia nigrella, R. gougetiana, Targionia hypophylla, Oxymitra incrassata ; Marstaller, 2006).
La présence d’espèces d’affinités méditerranéennes et hygrophiles temporaires ou adaptées à des microhabitats confinés comme Cephaloziella turneri, Epipterygium ssp., Fossombronia angulosa, Heterocladium heteropterum, Riccia nigrella et Scleropodium touretii laisse présager la possibilité de découvrir Fissidens curvatus.
On la retrouve parfois dans un groupement halophile rare à Fissidens curvatus et Tortella flavovirens (Hugonnot, 2018a) apparenté au Tortellion flavovirentis Guerra ex Guerra & Puche 1984 (communautés terricoles des substrats à granulométrie assez fine des marges océaniques et principalement composées d’acrocarpes).
7. Un contexte cévenol favorable
Si l’on analyse la situation géographique de la quasi-totalité des mentions européennes, on remarque que l’espèce ne s’éloigne qu’exceptionnellement de plus de 15 km de la Méditerranée et de l’océan Atlantique. Toutefois, ce patron de répartition souffre de quelques exceptions :
- Amélie-les-Bains-Palalda (66) : 32 km ;
- Soumont-Saint-Quentin en Normandie à Ouistreham (14) : 35 km ;
- Banca (64) : 40 km ;
- Penybont (Pays de Galles) : 40 km ;
- mentions des Deux-Sèvres et de la Vendée : 45 à 65 km ;
- Berga (Catalogne, Espagne) : 85 km.
En 2022, dans le cadre de l’expertise de l’espace naturel sensible dit des 3D (ENS des gorges du Doux, de la Daronne et du Duzon ; Labroche, 2022), Fissidens curvatus est découvert dans la région naturelle des Boutières, au sein de la commune ardéchoise de Lemps, au lieu-dit « Gouny » (figure 5, figure 6).
Le socle rocheux de l’ENS est fortement entaillé par une multitude de ruisselets qui alimentent les trois rivières principales. L’hydrographie très prégnante est à l’origine de nombreuses zones de sources et ruisselets dans des contextes variés : adrets, ubacs, vallons très étroits et confinés sur de fortes pentes. La densité à la fois de l’hydrographie, mais aussi localement des végétations arbustives et arborées sont de nature à favoriser une hygrométrie atmosphérique relativement élevée. Le fissident a été observé à proximité d’une sente peu empruntée, dans une tonsure argileuse ensoleillée et temporairement suintante, en situation d’adret, sur gneiss à sillimanite-biotite (pente moyenne du versant avoisinant 35°, pente du substrat d’environ 10°), accompagnée de Riccia nigrella et Weissia controversa var. controversa (planche 2).
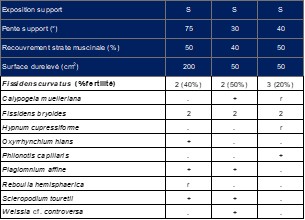
Deux autres localités ont été découvertes dans un contexte similaire (V. Hugonnot, comm. pers.). La première, en 2018, à seulement 10 km au nord de l’ENS des 3D et dans le même contexte (également dans la région naturelle des Boutières), à Sarras, dans les gorges de l’Ay (290 m d’altitude), sur un talus semi-ombragé au sein d’un versant pentu (pente avoisinant 45°) boisé d’exposition sud, sur des leptynites granitoïdes (planche 3). En écrivant ces lignes, une visite du site improvisée en avril 2025 a permis de retrouver assez aisément l’espèce tout en restant sur le sentier. Fissidens curvatus y a été observé sur des placages argileux brun-noirâtre (teneur en humus notoire), en bordure immédiate d’un ruisselet temporaire et du sentier, au sein d’une chênaie pubescente dense à Buis et Fragon. L’espèce y trouve à la fois la chaleur procurée par le versant sud très incliné et la fraicheur engendrée par la proximité immédiate du ruisseau temporaire associée au recouvrement dense de la végétation forestière. Le fissident occupe (tout du moins au niveau de la zone découverte en 2025) une surface de 200 cm2 répartie en quatre patchs espacés les uns des autres d’environ deux mètres. Les communautés bryophytiques ont été décrites sus la forme de relevés bryosociologiques présentés dans le tableau 1. D’autres bryophytes jouxtent les zones relevées mais à des niveaux topographiques et dans des microhabitats différents : Atrichum angustatum, Cirriphyllum crassinervium, Grimmia hartmanii, Heterocladium heteropterum, Isothecium alopecuroides, Lejeunea cavifolia, Plagiomnium rostratum, P. undulatum, Ptychostomum donianum, Rhynchostegium riparioides, Sciurohypnum populeum.
La seconde localité découverte par Vincent Hugonnot en 2015 se situe dans les Cévennes sud, sur une dalle rocheuse de gneiss amygdalaires de la Cézarenque, en exposition est/sud-est, à proximité d’un ruisseau temporaire, à environ 430 m d’altitude (photo 3).
Ces trois sites découverts récemment montrent la capacité de Fissidens curvatus à coloniser des territoires « plus continentaux ». On note à l’échelle mondiale une forte corrélation de l’espèce avec les zones à climats subtropicaux (à la fois les déclinaisons humides là où les étés sont humides, mais également les déclinaisons sèches, là où les étés sont secs, correspondant au climat méditerranéen).
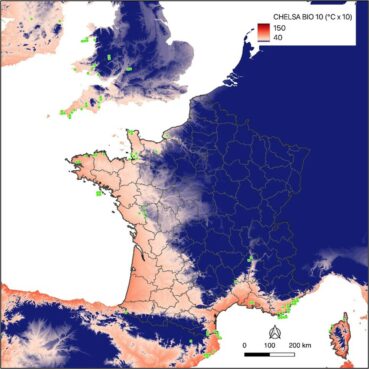
L’analyse des données climatiques issues de Chelsa (Climatologies at high resolution for the earth’s land surface areas ; Karger et al., 2021) par le prisme du BET (Bryophytes of Europe Traits dataset [3] ; Van Zuiken et al., 2023 ; Bardet et al., 2023) est à même de mettre en exergue les paramètres climatiques qui semblent les plus déterminants pour Fissidens curvatus, comparativement aux autres espèces du genre Fissidens :
- la température moyenne journalière du quart le plus chaud ;
- la température moyenne journalière du quart le plus froid (carte 3) ;
- la saisonnalité des précipitations.
L’enveloppe climatique optimale de ce fissident miniature requiert une température moyenne journalière élevée durant le quart le plus chaud (d’où la plus forte fréquence présumée de l’espèce dans le bassin méditerranéen), une température moyenne journalière relativement élevée durant le quart le plus froid (les températures négatives doivent être exceptionnelles, espèce de climat subtropical) et une saisonnalité des précipitations prégnante (précipitations très irrégulières intra et inter-annuellement, longues périodes de sécheresse relativement fréquentes).
Outre des conditions climatiques favorables, l’installation de Fissidens curvatus en situation « plus continentale », a fortiori lorsque l’altitude s’élève, nécessite de fortes pentes dans des vallées très encaissées sur un socle cristallin en situations d’adret (ou tout du moins, en exposition est/sud-est dominante), situation favorisant un contexte microclimatique favorable (hygrométrie atmosphérique suffisante et relativement constante, températures minimales réhaussées, forte chaleur en période estivale).
Les Cévennes, en particulier dans sa partie la plus méridionale, ainsi que la région naturelle des Boutières et ses nombreux vallons orientés est-ouest et au contact de la vallée du Rhône et des irradiations méditerranéennes offrent à l’espèce de vastes zones hautement favorables à son installation. D’autres régions naturelles en France présentent des conditions d’accueil intéressantes pour l’espèce parmi lesquelles la vallée de la Garonne et ses affluents, la région limousine (grès de Brive-la-Gaillarde, etc.), la vallée de la Seine…
8. Perspectives
Bien que l’espèce ne soit pas rare en Provence siliceuse, en particulier dans le Var (Hugonnot, 2018b), elle présente localement un intérêt patrimonial fort comme sur l’île de Porquerolles (Hugonnot, 2018a).
Au vu de l’état actuel des connaissances, l’espèce est rare dans le reste de la métropole (avec un statut de menace qui n’a jusque-là jamais été évaluée à l’échelle régionale). Fissidens curvatus a été observé à cinquante-six reprises avant 2015 (les données sont majoritairement anciennes, antérieures à 1950) contre seulement neuf fois durant la période 2015-2024 (pour une zone d’occupation nationale équivalente à 65 km2). Ce fissident a très peu été mentionné dans d’autres territoires européens, que ce soit en Italie, au Portugal et en Espagne… A contrario, sur l’île de Madère, l’espèce figure parmi les espèces à préoccupation mineure (Sérgio et al., 1992), tout comme en Grande-Bretagne (Callaghan, 2022). En Europe, l’espèce est considérée comme « data deficient (DD) » (Hodgetts, 2019).
Enfin, il ne faut pas sous-estimer la méconnaissance de cette espèce minuscule qui ne semble faire son apparition que par petits patchs et qui passera inaperçu à moins de connaitre l’espèce, sa taille et son écologie.
Évoquer un présumé déclin de l’espèce sur la base des données disponibles en France métropolitaine serait hasardeux. Néanmoins, un certain nombre de localités sont potentiellement menacées par la destruction des habitats, a fortiori sur les littoraux (urbanisation, carrières, aménagement du territoire dans des sites accessibles) ou par l’abandon du pâturage (Lobo et al., 2011 ; Blockeel et al., 2014). Au contraire, les populations découvertes dans le Massif central sont, au moins à court et moyen termes, à l’abri de destruction d‘habitats compte tenu de leur faible accessibilité et de la forte naturalité des sites connus.
Le maintien de cette espèce pionnière sur un site requiert l’existence d’un régime de perturbation régulier : retournement du sol par les sangliers, présence de lapins, éboulis sur les sites rocheux les plus pentus, érosion et dépôts d’alluvions par les ruisseaux temporaires, gestion des bermes, maintien d’un pâturage… Les perturbations, qui permettent la mise à nu du sol, induisent une évolution spatiale permanente des microhabitats favorables à l’espèce. De fait, comme beaucoup d’espèces pionnières à développement cyclique (apparition fugace et aléatoire), les localités sont régulièrement vouées à disparaître assez rapidement sous l’apparition et le développement rapide de pleurocarpes robustes et sociales compétitives. C’est d’ailleurs ce qui explique en partie que l’espèce n’ait pas été retrouvée dans la majorité des localités européennes historiques, et ce malgré une recherche active et ciblée (Lobo et al., 2011 ; Blockeel et al., 2014).
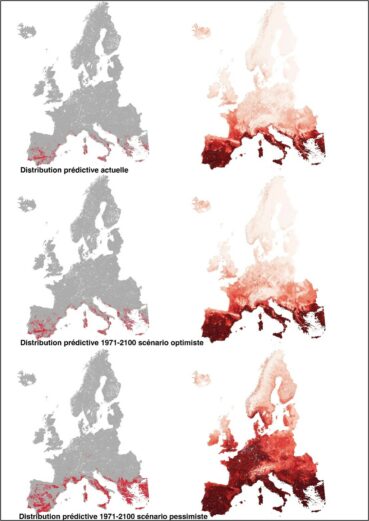
L’espèce est-elle installée dans le Massif central depuis une période lointaine ? Ou l’espèce connaît-elle une extension récente de sa distribution favorisée par le changement climatique ? Les populations des îles macaronésiennes – bastion présumé de l’espèce en Europe – jouent-elle un rôle de réservoir pour les populations de l’Europe occidentales ? Quoi qu’il en soit, les éléments biogéographiques de type méditerranéen connaissent une progression notoire de leurs habitats favorables, au contraire des espèces arctico-alpines (Zanatta et al., 2020). Les niches favorables semblent relativement répandues, au moins dans le bassin méditerranéen et au sud-est du Massif central, où la continuité des espaces favorables à l’espèce – particulièrement dans les Cévennes – est notoire ! Mais encore faut-il que l’espèce soit capable de coloniser ces nouvelles niches, d’en avoir les caractéristiques biologiques, morphologiques. Pionnière, capable de se maintenir jusqu’à plusieurs années (Dierßen, 2001), la dissémination de l’espèce ne semble reposer que sur la dispersion des spores. Cependant, la part des individus portant des sporophytes se trouve limitée par son caractère dioïque. Les spores nombreuses, de petite taille (entre 9 à 17,5 µm) comme celles de Fissidens curvatus, sont facilement emportées par les vents, même d’intensité modérée. D’autres vecteurs jouent probablement un rôle dans la dispersion de l’espèce : espèces animales (mammifères), ruissellement, sentier de randonnée. On peut se demander quel modèle de dispersion principal suit l’espèce, une dispersion à courte distance – distance-dépendant – ou une dispersion à longue distance – indépendant de la distance ? Seule une attention croissante des bryologues pour ce fissident permettra de renforcer la connaissance de l’espèce, de mieux appréhender son écologie, de préciser sa distribution en France métropolitaine et de tenter d’évaluer la dynamique de ses populations.
[1] La nomenclature des taxons cités dans ce document suit le référentiel taxonomique Lobelia, basé sur TaxRef v. 17 (CBN, 2024). Afin de ne pas alourdir la lecture du document, les noms des espèces sont indiqués sans leurs autorités.
[2] La nomenclature des syntaxons bryophytiques cités dans ce document suit le catalogue des communautés muscinales d’Europe et des régions voisines (Marstaller, 2006), celle des syntaxons trachéophytiques suit le référentiel taxonomique Lobelia, basé sur TaxRef v. 17 (CBN, 2024). Afin de ne pas alourdir la lecture du document, les noms des syntaxons sont indiqués sans leurs autorités.
[3] Dans le BET, pour chaque espèce, des valeurs moyennes calculées sur la base des cellules abritant les populations à l’échelle de l’Europe sont disponibles pour les paramètres de Chelsa.
Bibliographie
Aicardi O., 2005. Contribution à l’inventaire de la bryoflore française (année 2004). Bulletin de la Société botanique du Centre-Ouest, n. s., 36 : 531-538.
Allorge V., 1958. Deux espèces de mousses nouvelles pour la France. Revue bryologique et lichénologique 27 (3-4) : 188-190.
Australian National Botanical gardens, monographie de Fissidens curvatus, https://www.anbg.gov.au/abrs/
Mosses_online/FISSIDENS/000_Fissidens%20curvatus%20V2.pdf [15/12/2024].
Bardet O., Labroche A. & Legland T. (coord.), 2023. Base de traits des bryophytes de France. Correspondance entre le bet dataset (Van Zuijlen K. et al. 2023) et TaxRef v.16. Groupe de Travail Bryophytes des Conservatoires botaniques nationaux.
Biographie du Comte de Solms-Laubach, https://www.societe-botanique-alsace.org/botanistes-dalsace/solms-laubach/ [08/12/2024].
Blockeel T.L., Bosanquet S.D.S., Hill M.O. & Preston C.D., 2014. Atlas of british & irish bryophytes. The distribution and habitat of mosses and liverworts in Britain and Ireland. British Bryological Society, 652 p.
Boulay J.N., 1884. Muscinées de la France, première partie : mousses. F. Savy, Paris, 800 p.
Bruggeman-Nannenga M.A., 2013. Subgenus Fissidens in tropical eastern Africa with emphasis on the Tanzanian collections by Tamás Pócs. Polish botanical journal 58 : 369-417.
Bruggemann-Nannega M.A., 2021. Fissidens subgenus Aloma, the scariosus and bryoides types of peristome in the light of the phylogenetic tree by Suzuki et al. Lindbergia 2021 : 1-8.
Bruggeman-Nannenga M.A. & Pursell R.-A., 1995. Notes on Fissidens, V. Lindbergia 20 : 49-55.
Callaghan D. A., 2022. A new IUCN red list of the bryophytes of Britain, 2023. Journal of bryology 44 (4) : 271-389.
Charrier J., 1958. Catalogue des muscinées du département de la Vendée. Annales de la Société des sciences naturelles de la Charente-Maritime 4 (1) : 1-56.
Corbière l. & Jahandiez E., 1921. Muscinées du département du Var. Annales de la Société d’histoire naturelle de Toulon 6 (suppl. au t. 4) : 1-63.
Corbière l., 1889. Muscinées du département de la Manche. Mémoires de la Société nationale des sciences naturelles et mathématiques de Cherbourg 26 : 195-368.
Crundwell A.C. & Whitehouse H.L.K,1976. Tortula bolanderi (Lesq. & James) howe in France, new to Europe. Journal of bryology 9 : 13-15.
Dierßen K., 2001. Distribution, ecological amplitude and phytosociological characterization of European bryophytes. Cramer, Berlin, 289 p.
Dismier G., 1920. Additions à la flore bryologique des Alpes-Maritimes et du Var. Bulletin de la Société botanique de France 67(1) : 35-47 et 113-120.
Düll R., 1984. Distribution of the European and Macaronesian mosses (Bryophytina). Bryologische Beiträge 4 : 1-114.
Durfort J., Lagrandie J., Le Bail J. & Stauth S., 2017. Découvertes récentes concernant les bryophytes du Massif armoricain et de ses marges. E.R.I.C.A. 31 : 117-122.
Dufort J., Le Bail J. & Stauth S., 2021. Bilan des découvertes 2020 concernant les bryophytes du massif armoricain et de ses marges. E.R.I.C.A 35 : 97-106.
Duterte H., 1887. Notes bryologiques sur Amélie-les-Bains et ses environs. Revue bryologique 13 (1) : 6-8.
Editorial committee, 2007. Volume 28. Fissidens. Eds. 1993 +. Flora of North America north of Mexico [online].
Erzberger P., 2016. The genus Fissidens (Fissidentaceae, Bryophyta) in Hungary. Studia botanica Hungarica 47 (1) : 41-139.
Frémy P. (abbé) & Meslin R., 1927. Herborisations aux environs de Gavray (Manche). Bulletin de la Société linnéenne de Normandie 7 (9) : 146-183.
Gaume R., 1956. Catalogue des muscinées de Bretagne d’après les documents du Dr F. Camus. Revue bryologique et lichénologique 25 (1-2) : 1-115.
GBIF occurrence download, http://gbif.org, https://doi.org/10.15468/dl.s7c7vk [03/02/2025].
Guerra J. & Brugués M., 2015. Flora briofítica ibérica, II – Archidiales, Dicranales, Fissidentales, Seligeriales & Grimmiales. Universidad de Murcia, 356 p.
Hébrard J.-P., 1978. Contribution à l’étude de la flore et de la végétation muscinale du Parc national de Port-Cros (Var). Scientific reports of Port-Cros National Park 4 : 9-68.
Hébrard J.-P. 1988. Contribution à l’étude des bryophytes de la Réserve naturelle de la presqu’ile de Scandola (Corse). Candollea 43 : 189-197.
Hébrard J.-P., 2009. Bryophytes méconnues, rares ou signalées pour la première fois dans les Alpes-de-Haute-Provence, les Alpes-Maritimes, les Bouches-du-Rhône et le Var. Bulletin de la Société linnéenne de Provence 60 : 99-111.
Hodgetts N., 2019. A miniature world in decline: European Red List of Mosses, Liverworts and Hornworts. UICN, 88 p.
Hotermans A., Albertos B., Bisang I., Blockeel T.L., Calleja J.A., Campisi P., Celle J., Cogoni A., Draper I., Garcia N., Garilleti R., Hedenäs L., Hodgetts N., Hugonnot V., Karger D., Kiebacher T., Kučera J., Lara F., Lembrechts J., Lenoir J., Mežaka A., Natcheva R., Papp B., Sparrius L., Zechmeister H., Vanderpoorten A. Collart, F., in prep. Impacts of climate change on bryophyte distribution: a comprehensive assessment at fine spatial resolution across Europe.
Hugonnot V., 2007a. Les bryophytes de l’ile de Porquerolles (Hyères, Var, France) : inventaire, atlas, groupements bryophytiques et intérêt patrimonial. Scientific reports of Port-Cros National Park 22 : 67-194.
Hugonnot V., 2007b. Aperçu de la flore et de la végétation bryophytiques des sites de Saint-Daumas, du bois du Rouquan et du vallon de Sauronne. Leur place dans le contexte du massif des Maures. WWF/CEEP, 101 p.
Husnot P.-T., 1884. Muscologia gallica. Description & figures des mousses de France et des contrées voisines. Première partie : Acrocarpes. Editions Husnot – Savy, Paris, 284 p.
Karger D.N., Conrad O., Böhner J., Kawohl T., Kreft H. Soria-Auza R.W. Zimmermann N.E. Linder H.P. & Kessler M., 2017. Climatologies at high resolution for the earth’s land surface areas. Scientific data 4.
Labroche A., 2022. Expertise de la bryoflore de l’ENS « Gorges du Doux, du Duzon et de la Daronne » (Ardèche). Conservatoire botanique national du Massif central, Pélussin, 42 p.
Lobo C., Sim-Sim M., Luís l. & Stech M., 2011. Chorological data and threat status evaluation of Fissidens species (Fissidentaceae, Bryophyta) on Madeira archipelago. Nova Hedwigia 92 : 121-131.
Magill R.E., 1981. Bryophyta. 1 – Mosses (1) – Sphagnaceae to Grimmiaceae, Flora of Southern Africa, Botanical research institute, Pretoria.
Marstaller R., 2006. Syntaxonomischer Konspekt der Moosgesllschaften Europas und angrenzender Gebiete. Haussknechtia 13 : 1-192.
The Plantlist, theplantlist.org [08/12/2025].
Potier de la Varde R., 1923. Contribution à la flore bryologique du département de la Manche. Bulletin de la Société linnéenne de Normandie 7 (5) : 61-68.
Potier de la Varde R., 1938. Le genre Fissidens dans la Manche. Notices, mémoires et documents de la Société d’agriculture, d’archéologie et d’histoire naturelle du département de la Manche (Saint-Lô) 49 : 139-168.
Sérgio C., Schumacker R., Fontinha S. & Sim-Sim. M., 1992. Evaluation of the status of the bryophyte flora of Madeira with reference to endemic and threatened European species. Biological Conservation 59 (2–3) : 223-231.
Skrzypczak R., 2009. Didymodon bistratosus J.-P. Hébrard & R.-B. Pierrot en France. Bulletin de la Société botanique du Centre-Ouest, n. s., 40 : 549-560.
Smith A.J.E., 2004. The moss flora of Britain. Cambridge University Press, Cambridge, 1 012 p.
Solms-Laubach H., 1868. Tentamen bryo-geographiae algarviae regni lusitani provinciae. 43 p.
Sotiaux A., Pioli A., Royaud A., Schumacker R. & Vanderpoorten A., 2007. A checklist of the bryophytes of Corsica (France): new records and a review of the literature. Journal of bryology 29 : 41-53
Spécimens de Fissidens curvatus sous e-recoltnat, https://explore.recolnat.org/search/botanique/
simplequery=fissidens%2520algarvicus [12/12/2024].
Squivet de Carondelet J., 1961. Mousses de Montpellier et contributions diverses à la bryologie du sud-est de la France (plaines et basses montagnes). Naturalia monspeliensia, série botanique, 13 : 71-188.
Thériot I., 1890. Herborisations dans les vallées de Saint-Aubin-Routot et d’Oudalle. Bulletin de la Société́ linnéenne de Normandie 4 (4) : 95-101.
Van Zuijlen K., Nobis M.P., Hedenäs L., Hodgetts N., Calleja Alarcón J. A., Albertos B., Bernhardt-Römermann M., Gabriel G., Garilleti R., Lara F., Preston C.D., Simmel J., Urmi E., Bisang I. & Bergamini A., 2023. Bryophytes of Europe traits (bet) data set: a fundamental tool for ecological studies. Journal of Vegetation Science 34 (2) : DOI: 10.1111/jvs.13179, 7 p.
The World Flora Online, https://www.worldfloraonline.org/taxon/wfo-0001193312 [15/12/2024].
Xing-jiang l., 2001. Moss flora of China, 2 – Fissidentaceae-Ptychomitriaceae. Missouri Botanical Garden Press, 283 p.
Zanatta F., Engler R., Collart F., Broennimann O., Mateo R., Papp B., Muñoz J., Baurain D., Guisan A. & Vanderpoorten A., 2020. Bryophytes are predicted to lag behind future climate change despite their high dispersal capacities. Nature communications 11. 9 p.
Zanten B.O. & During H.J., 1974. Contribution to the mossflora of the departments Pyrénées-orientales and Aude. Revue bryologique et lichénologique 40 (3) : 203-217.
Remerciements
Je remercie ARCHE Agglo (Communauté d’agglomération d’Ardèche en Hermitage) et le Département de l’Ardèche pour avoir confié au CBN Massif central la réalisation de l’expertise bryologique de l’ENS des 3D. Par ailleurs, je tiens à exprimer ma reconnaissance à toutes les personnes qui ont contribué à l’élaboration de cet article, à savoir Rosa María Ros (Université de Murcie) pour la confirmation de l’identification de l’espèce, Virgile Noble et Julie-Anne Burkhart (Conservatoire botanique national méditerranéen de Porquerolles), Paol Kerinec (Conservatoire botanique national de Brest),Timothée Prey (Conservatoire botanique de Normandie), Jean-Christophe Hauguel (Conservatoire botanique national de Bailleul), Sabrina Borgomano (Conservatoire botanique national de Corse), Vincent Hugonnot (bureau d’études Pépin-Hugonnot) pour le partage de données, Maria Bruggeman-Nannega pour le partage de publications scientifiques, Olivier Bardet, Nicolas Bianchin et Émeric Sulmont pour leur relecture attentive et minutieuse, Marco Bastianelli pour son appui technique dans l’appréhension du jeu de données climatiques Chelsa, Adèle Hotermans et Alain Vanderpoorten pour la transmission des cartes de distribution prédictives, Pierre Boudier pour la réalisation de la planche photographique de l’espèce.