Contribution à une synthèse de la classe des Juncetea maritimi
Title
Contribution to a synthesis of Juncetea maritimi
Résumé
Sur la base de tableaux par alliance et d’un large tableau synthétique, l’auteur propose une synthèse de la végétation des prés halophiles vivaces (Juncetea maritimi), incluant la végétation subarctique et la végétation pannonique ; sept ordres et vingt-quatre alliances (dont trois nouvelles) sont reconnus.
Abstract
Based on tables by alliance and a large synthetic table, the author offers a synthesis of the vegetation of perennial halophilous meadows (Juncetea maritimi), including subarctic and Pannonic vegetation; seven orders and twenty-four alliances (including three new ones) are recognized.
À la suite de la synthèse récente des Sarcocornietea fruticosae, classe de végétation halophile chaméphytique (de Foucault, 2021b), on propose ici celle des Juncetea maritimi, classe de végétation halophile hémicryptophyto-géophytique. On renvoie à la première synthèse pour les méthodes et les limites de cet exercice.
La nomenclature suivie est celle de Flora Gallica (Tison & de Foucault, 2014) pour les taxons présents en France (à l’exception des Spergula halophiles dénommés ici sous Spergularia), celle de Euro+Med PlantBase ou à défaut Catalogue of life pour le reste de l’aire couverte. Pour alléger le texte, les noms des sous-espèces autonymes, c’est-à-dire ayant le même nom que l’espèce, seront réduits à leur initiale. Pour alléger les tableaux et les relevés isolés, le signe * y remplacera ‘subsp.’ ou ‘var.’. Les thérophytes (dont Spergularia marina) ne sont pas considérés comme caractérisant la végétation synthétisée ici.
1. Déclinaison des Juncetea maritimi
JUNCETEA MARITIMI Tüxen & Oberd. 1958 (Veröff. Geobot. Inst. Rübel Zürich 32 (2) : 98) [syn. : Juncetea maritimi Braun-Blanq., Roussine & Nègre 1952 (Les groupements végétaux de la France méditerranéenne : 114, note de bas de page considérée ici comme invalide ; incl. Asteretea tripolii V. Westh. & Beeftink in Beeftink 1962 (Biol. Jaarb. 30), Spartinetea glabrae Tüxen in Beeftink 1962 (Biol. Jaarb. 30), Festuco-Puccinellietea Soó 1968].
Typus classis : Juncetalia maritimi Braun-Blanq. ex Horvatić 1934 (Prirod. Istraž. Kral. Jugosl. 19 : 269).
Prés halophiles vivaces méditerranéo-atlantiques à irradiations arctiques et pannoniques caractérisés par Juncus gerardii, Tripolium pannonicum, auxquels on peut ajouter Carex extensa (photo 1) et Juncus maritimus qui manquent toutefois dans les Puccinellietalia phryganodis et une bonne partie des Lysimachio-Puccinellietalia maritimae. Parmi les taxons compagnes, relevons Halimione portulacoides dont l’optimum se situe plutôt dans les Sarcocornietea fruticosae, Phragmites australis, Bolboschoenus maritimus ; un contact spatial (mosaïques biologiques) existe avec des classes thérophytiques, notamment les Thero-Suaedetea splendentis et les Saginetea maritimae.
En termes systémiques, des relations biotiques peuvent relier les Sarcocornietea fruticosae et les Juncetea maritimi. En effet le pâturage-piétinement tend à limiter les chaméphytes, plus fragiles, et alors à favoriser les cryptophytes, moins sensibles ; on a par exemple (Géhu et al., 1976 : 210) :
Halimionetum portulacoidis – » →Halimiono portulacoidis-Puccinellietum maritimae (cf. infra, syntaxon Pm2)
où » désigne cette influence biotique. On note une relation équivalente entre l’Eleocharitetum parvulae Gillner 1960 et des roselières halophiles soumises au pâturage (Géhu, 1973b, sub Eleocharetum parvulae) ; mais ces deux types de communautés ne relèvent pas des Juncetea maritimi. Cet Eleocharitetum apparaît comme l’homologue des communautés amphibies non ou peu halophiles piétinées de bas niveau topographique à Eleocharis palustris.
Il peut paraître paradoxal d’évoquer maintenant une dynamique des prés salés vers des bas-marais oligotrophiles tant ces deux types de communautés végétales paraissent irréductibles. Et pourtant, quelques rares exemples en sont connus. Un premier exemple est rapporté par Franck et al. (1982) de la côte nord-bretonne. Il s’agit d’une série dynamique sur un substrat géologique homogène (arènes granitiques non calcarifères, plus ou moins mêlées d’éléments fins), menant de prés salés (1 – Halimiono portulacoidis-Puccinellietum maritimae, 2 – Cochleario anglicae-Plantaginetum maritimae, 3 – Junco maritimi-Caricetum extensae) à des bas-marais basiphiles (4-5 – Junco maritimi-Schoenetum nigricantis et gr. à Eleocharis quinqueflora) puis acidiphile (6 – Caro verticillati- Molinietum caeruleae), enfin à des landes de l’Ulicion minoris (7) avec des espèces plus ou moins halophiles relictuelles dans les deux derniers stades. L’étude corrélative des sols donne la série éaphique suivante pour ces sept communautés :
1 : tangue sableuse humide indifférenciée
2 : id. plus évoluée à horizon organique marqué
3 : sol à gley sulfureux et horizon organique plus ou moins épais
4-5 : sol organique à gley sulfureux
6 : gley à humus brut
7 : gley podzolique à humus brut
Au cours de cette série édaphique, on note une baisse de NaCl, de l’indice de sodicité (rapport Na/somme cations), de la somme des bases échangeables, un lessivage des cations, une augmentation de la matière organique, du carbone, du rapport Ca/somme des bases échangeables traduisant un entraînement par drainage vertical des cations alcalins. Cette dynamique semble exister aussi dans quelques salines continentales, comme le montrent certaines associations étudiées en ex-Tchécoslovaquie par Vicherek (1973, alliance de l’Halo–Trichophorion pumili, mieux placé dans les Scheuchzerio palustris-Caricetea nigrae que dans les Juncetea maritimi où la place son auteur) ou des salines littorales subboréales étudiées en Suède par Tyler (1980).
Le tableau 1 dresse la synthèse globale de cette classe.
Ordre 1. Puccinellietalia phryganodis Hadač 1946 (Studia Bot. Čechica 7, non consulté), incl. Lysimachio maritimae-Puccinellietalia pumilae A. Miyaw. & Ohba 1965 (Sci. Rep. Yokohama Natl. Univ., sect. II, 12 : 18, sub Glauco maritimae-Puccinellietalia kurilensis) prov. ? ; tableau 1 : colonnes Pph à SPd
[syn. : Carici-Puccinellietalia phryganodis Beeftink & V. Westh. in Beeftink 1962 (Biol. Jaarb. 30) nom. illeg. (art. 22)]
Typus ordinis : Puccinellion phryganodis Hadač 1946 (Studia Bot. Čechica 7).
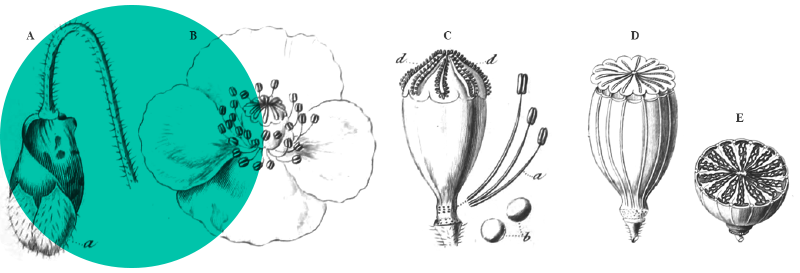
Prés halophiles (circum)arctiques caractérisés par Anserina anserina subsp. egedei, Carex subspathacea (planche 1 : 1), Stellaria humifusa (planche 1 : 2), pouvant se rattacher aux Juncetea maritimi surtout par Triglochin maritima, Plantago maritima subsp. m. et Lysimachia maritima. Bosseaux (1965) puis Muller & Etcheberry (2006) citent aussi des végétations de cet ordre pour le littoral de l’archipel Saint-Pierre-et-Miquelon, avec Puccinellia pumila, Juncus gerardii, Carex paleacea, Lysimachia maritima, Triglochin maritima.
Alliance Pph. Puccinellion phryganodis Hadač 1946 (Studia Bot. Čechica 7, non consulté) ; tableau 1 : colonne Pph ; tableau 2
[syn. : Puccinellion phryganodis Nordh. 1954 (Vegetatio 5 : 384) nom. illeg. (art. 22)]
Lectotypus nominis hoc loco : Puccinellietum phryganodis Hadač 1946 (Studia Bot. Čechica 7 : 142).
Prés halophiles de marais côtiers boréo-arctiques de bas niveau à Puccinellia phryganodes (planche 1 : 3), P. nutkaensis, Cochlearia officinalis, Carex ursina (planche 1 : 4) et, en commun avec l’alliance suivante, Carex glareosa (planche 1 : 5) ; sur ces associations, voir aussi Thannheiser (1975) et Lepping & Daniëls (2006).
Pph1. Puccinellietum phryganodis Hadač 1946 (Hofmann, 1969, tableau p. 226) ; renommé Puccinellietum vilfoideae par Hadač (1989 : 136) ; voir aussi Thannheiser & Hofmann (1977, tableau 1).
Pph2. Puccinellietum phryganodis arcticum (Thannheiser, 1974, tableau p. 152).
Pph3. Caricetum subspathaceae Hadač 1946 ; a – race norvégienne (Ibid., tableau p. 153) ; b – race russe (rivages de la mer de Barents ; Lavrinenko & Lavrinenko, 2018, tableau 1 : relevés 7 à 26) ; voir aussi Hadač (1989, tableau 2).
Pph4. Caricetum ursinae Hadač 1946 (Thannheiser & Hofmann, 1977, tableau 2 ; Lepping & Daniëls, 2006, tableau 3 : relevés 14 à 18) ; voir aussi Hadač (1989, tableau 3).
Pph5. Puccinellietum nutkaensis Nordh. 1954 (Nordhagen, 1954, tableau 2 : colonnes 7 et 8, sub Puccinellietum retroflexae ; de Molenaar, 1974, tableau I : relevés 8 à 10, sub Puccinellietum coarctatae).
Pph6. Sagino nivalis-Phippsietum algidae Molenaar 1974 prov. (de Molenaar, 1974, tableau III, sub Sagino intermediae-Phippsietum algidae) (Phippsia algida illustré planche 1 : 6).
Alliance Cg. Caricion glareosae Nordh. 1954 (Vegetatio 5 : 386) ; tableau 1 : colonne Cg ; tableau 3
Lectotypus nominis hoc loco : Festuco littoralis-Caricetum glareosae Nordh. 1954 (Vegetatio 5 : 384).
Prairies de marais côtiers salés boréo-arctiques de niveau supérieur (Atlantique-Nord et océan Arctique) à Carex salina, C. mackenziei, Calamagrostis deschampsioides, Festuca rubra subsp. littoralis.
Cg1. Festuco littoralis-Caricetum glareosae Nordh. 1954 (Dítě et al., 2019, tableau 1 : colonne 2).
Cg2. Caricetum mackenziei Nordh. 1954 (Ibid., tableau 1 : colonne 3) ; le Caricetum mackenziei sensu Gillner (1960, tableau 10) ne correspond pas à cette association.
Cg3. Caricetum salinae Nordh. 1954 (Ibid., tableau 1 : colonne 4).
Cg4. Juncetum gerardii subarcticum Nordh. 1954 (Nordhagen, 1954, tableau 3 : colonnes 12 et 13) ; nom illégitime (art. 34), qui peut être renommé (art. 39) Stellario humifusae-Juncetum gerardii (Nordh. 1954) nom. nov. hoc loco, typus nominis hoc loco : relevé décrit par la colonne 13 du tableau 3 in Nordhagen (1954, Vegetatio 5 : 384).
Cg5. Thannheiser (1987, tableau 10 et figure 10) mentionne le Festucetum littoralis Corill. 1953 jusque sur les côtes islandaises, ce qui paraît excessif ; d’ailleurs, dans les sept relevés de son tableau 10, Carex glareosa apparaît deux fois, on peut définir nouvellement un Carici glareosae-Plantaginetum maritimae (Thannheiser 1987) B. Foucault & Thannheiser nom. nov. hoc loco, typus nominis hoc loco : relevé 6 du tableau 10 in Thannheiser (1987, Acta Bot. Islandica 9 : 53), synthétisé ici dans la colonne Cg5.
Cg6. Caricetum glareosae sensu Lavrinenko & Lavrinenko 2018 (Lavrinenko & Lavrinenko, 2018, tableau 2 : relevés 1 à 23) ; cette association russe est bien distincte de l’association scandinave (Cg8) et peut être distinguée sous le nom de Arctanthemo arctici-Caricetum glareosae (Lavrinenko & Lavrinenko 2018) nom. nov. hoc loco, typus nominis hoc loco : relevé 1 du tableau 2 in Lavrinenko & Lavrinenko (2018, Phytodiversity of eastern Europe XII (3) : 94).
Cg7. Stellario crassifoliae-Caricetum salinae Lavrinenko & Lavrinenko 2018 (Lavrinenko & Lavrinenko, 2018, tableau 3) ; paraît mieux placé dans le Caricion glareosae que dans le Dupontion fisheri où ses auteurs le rangent.
Cg8. Caricetum glareosae Molenaar 1974 (de Molenaar, 1974, tableau 4 : relevés 1 à 25).
Cg9. Argentino egedei–Caricetum rariflorae Molenaar 1974 (Ibid., tableau 4 : relevés 26 à 30, sub Potentillo–Caricetum rariflorae).
Alliance Ppu. Puccinellion pumilae A. Miyaw. & Ohba 1965 (Sci. Rep. Yokohama Natl. Univ., sect. II, 12 : 18, sub Puccinellion kurilensis) ; tableau 1 : colonne Ppu ; tableau 4 : syntaxons en Ppu
Prairies de marais côtiers salés de Hokkaido (Japon septentrional) à Puccinellia pumila, Juncus gracillimus, Carex ramenskii ; alliance placée par ses auteurs dans les Lysimachio maritimae-Puccinellietalia pumilae A. Miyaw. & Ohba 1965 prov. (Sci. Rep. Yokohama Natl. Univ., sect. II, 12 : 18, sub Glauco maritimae Puccinellietalia kurilensis) mais sans doute à rattacher plutôt aux Puccinellietalia phryganodis.
Ppu1. Puccinellio pumilae-Caricetum subspathaceae A. Miyaw. & Ohba 1965 (Miyawaki & Ohba, 1965, tableau 6, sub Puccinellio kurilensis-Caricetum subspathaceae).
Ppu2. Juncetum gracillimi A. Miyaw. & Ohba 1965 (Ibid., tableau 5).
Ppu3. Puccinellietum pumilae A. Miyaw. & Ohba 1965 (Ibid., tableau 4, sub Puccinellietum kurilensis).
Ppu4. Caricetum ramenskii A. Miyaw. & Ohba 1965 (Ibid., tableau 8).
Plus au sud du Japon, donc à Honshu, Shikoku et Kyushu, une ou plusieurs classes différentes prennent le relais (Miyawaki & Ohba, 1969).
Pour éviter l’homonymie avec d’autres Puccinellieta distantis antérieurs (par exemple ceux de Feekes 1934, de Soó 1937), le Puccinellietum distantis Nordh. 1954 (Thannheiser, 1987, tableau 7, sub Puccinellietum retroflexae) peut être renommé (art. 39) Stellario humifusae-Puccinellietum distantis (Nordh. 1954) nom. nov. hoc loco, typus nominis hoc loco : relevé 10 du tableau 7 in Thannheiser (1987, Acta Bot. Islandica 9 : 48), dans la colonne SPd de notre tableau 1, non encore rattaché à une alliance précise.
On ne possède par ailleurs qu’assez peu d’informations sur le Dupontion fischeri Hadač 1946 (Studia Bot. Čechica 7, non consulté) qui rassemblerait des prés littoraux oligohalophiles turficoles sur sol argileux. Il est cependant sans doute possible d’y rattacher le Calamagrostio deschampsioidis-Caricetum subspathaceae Bournérias 1976 (Bournérias, 1976, tableau p. 161). En outre, de la Russie arctique, Sergienko (2013) publie une liste de taxons paraissant s’y rattacher. Ces deux données sont synthétisées respectivement dans les colonnes Df et Serg. du tableau 4. De l’Alaska, Taylor (1981) évoque aussi des prés salés à Dupontia fisheri.
Il est probable que les prés salés du Canada oriental relèvent encore de cet ordre, avec Argentina anserina subsp. egedei, Stellaria humifusa, Lysimachia maritima, Triglochin maritima, Juncus gerardii, Puccinellia phryganodes (incl. P. ambigua), Carex mackenziei, C. salina, bien que Géhu et Géhu-Franck (1992a) créent pour eux les Plantagini maritimae-Triglochinetea maritimae et les Junco-Spartinetalia patentis.
Dans ses tableaux 4 et 5 (Plantaginetum maritimae et Puccinellietum ambiguae), Grandtner (1984) livre deux faciès d’un même Puccinellietum phryganodis homonyme illégitime (art. 31) du Puccinellietum phryganodis Hadač 1946, d’où la proposition (art. 34) du Limonio caroliniani-Puccinellietum phryganodis (Grandtner 1984) nom. nov. hoc loco, typus nominis hoc loco : relevé 4 du tableau 5 in Grandtner (1984, Doc. Phytosoc., NS, VIII : 10), association typus nominis hoc loco du Limonio caroliniani-Puccinellion phryganodis all. nov. hoc loco, alliance caractérisée par Puccinellia phryganodes, Limonium carolinianum, Plantago maritima subsp. m., Lysimachia maritima, Sporobolus pumilus (= Spartina patens) synthétisé dans la colonne LPp de notre tableau 4. Quoiqu’encore pourvu de L. carolinianum, le Distichlidetum spicatae de Conard (1935 : 458) pourrait relever d’une unité plus méridionale.
De leur côté, pour le littoral de l’Alaska, Peinado et al. (1995, figure 1) évoquent les Carici-Puccinellietea phryganodis, d’après Knapp (1976). Barbour et Billings (1988) confirment cette végétation pour l’Amérique septentrionale arctique, tout en relevant l’absence de chaméphytes et de représentants de la famille des Amaranthaceae.
Finalement, de Hokkaido à la Sibérie, puis la Scandinvie et l’Amérique du Nord orientale et occidentale, il se pourrait qu’il faille définir plutôt une unique classe circum-arctique, celle des Carici-Puccinellietea phryganodis Knapp 1976, mais ce nom est invalide (nomen nudum, art. 2b). Selon les régions, elle pourrait alors accueillir des taxons transgressifs de classes plus méridionales, dont les Juncetea maritimi. D’un autre côté, sur la base de leurs observations sur un estuaire du Québec, on a déjà cité le fait que Géhu et Géhu-Franck (1992a) définissent une classe nouvelle, les Plantagini maritimae-Triglochinetea maritimae, selon eux à répartition holarctique ; dans la mesure où ils y incluent les Glauco-Puccinellietalia maritimae (holotype des Plantagini-Triglochinetea maritimae) et les Juncetalia maritimi (holotype des Juncetea maritimi), il n’y a aucune raison de substituer ce nouveau nom au classique Juncetea maritimi.
Ordre 2. Spartinetalia alterniflorae Conard 1935 (Amer. Midl. Naturalist 16 (4) : 507, sub Spartinetalia glabrae) ; tableau 1 : colonne Sa
Typus ordinis : Spartinion alterniflorae Conard 1935 (Amer. Midl. Naturalist 16 (4) : 507).
Prés halophiles des slikkes européennes à ouest-nord-américaines (au moins) souvent placés dans une classe à part, les Spartinetea glabrae, pouvant cependant se rattacher aux Juncetea maritimi comme fin de classe (Julve, 1993). Voir aussi Géhu (1973a). Malgré sa large extension, il ne paraît pas utile de distinguer plus d’une alliance.
Alliance Sa. Spartinion alterniflorae Conard 1935 (Amer. Midl. Naturalist 16 (4) : 507, sub Spartinion glabrae) ; tableau 1 : colonne Sa ; tableau 5
[syn. : Spartinion anglicae Géhu in Bardat, Bioret, Botineau, Boullet, Delpech, Géhu, Haury, Lacoste, Rameau, J.-M. Royer, G. Roux & Touffet 2004 (Patrimoines naturels 61 : 97) nom. illeg.]
Typus allianciae : Spartinetum alterniflorae Conard 1935 (Amer. Midl. Naturalist 16 (4) : 455, sub Spartinetum glabrae).
* Associations amphi-atlantiques
Sa1. Spartinetum maritimae Corill. 1953 (Beeftink & Géhu, 1973, tableau p. 8) ; la première mention de cette végétation revient semble-t-il à Emberger & Régnier (1926 : 78, où Spartina maritima est dénommé S. stricta), mais sans relevé (nomen nudum).
Sa2. Spartinetum alterniflorae Conard 1935 (Conard, 1935, tableau p. 455), nord-américain.
Sa3. Spartinetum alterniflorae Corill. 1953 (Beeftink & Géhu, 1973, tableau p. 20), homonyme postérieur du Spartinetum alterniflorae Conard 1935, donc à renommer : Tripolio pannonici–Spartinetum alterniflorae (Corill. 1953) nom. nov. hoc loco, typus nominis hoc loco : relevé 3 du tableau 5 in Géhu & Delzenne (1976, Colloq. Phytosoc. IV : 239).
Sa4. Spartinetum anglicae Corill. 1953 corr. Géhu & Géhu-Franck 1984 (Ibid., tableau p. 25, sub Spartinetum townsendii) ; photo 2.
* Associations méditerranéennes à Limonium narbonense, Sarcocornia fruticosa
Sa5. Limonio narbonensis–Spartinetum maritimae (Pignatti 1966) Beeftink & Géhu 1973 ; a – d’après Géhu, Scoppola et al. (1984, tableau 14) ; b – d’après Beeftink & Géhu (1973, tableau p. 17).
Sa6. Spartinetum densiflorae Rivas Mart., M.J. Costa, Castrov. & Valdés Berm. 1980 (Rivas-Martínez et al., 1980, tableau 22).
Sa7. Spartinetum densiflorae sensu Costa et al. 1997 (Costa et al., 1997, tableau 3) ; assez différent du précédent dont il est homonyme, renommé ici Halimiono portulacoidis-Spartinetum densiflorae (J.C. Costa, Lousã & Espírito-Santo 1997) nom. nov. hoc loco, typus nominis hoc loco : relevé 6 du tableau 3 in Costa et al. (1997, Studia Bot. 15 : 88).
Ordre 2. Lysimachio maritimae-Puccinellietalia maritimae Beeftink & V. Westh. in Beeftink 1962 (Biol. Jaarb. 30, non consulté, sub Glauco maritimae-Puccinellietalia maritimae) ; tableau 1 : colonnes Pm à SPm
Lectotypus nominis hoc loco : Puccinellion maritimae W.F. Christ. 1927 (Föhrer Heimatbücher 16, non consulté).
Prés halophiles atlantico-baltiques à Puccinellia maritima (photo 3), Lysimachia maritima, Spergularia media, Limonium vulgare, Armeria maritima (présent aussi dans les pelouses aérohalophiles des Armerio-Festucetea pruinosae et dans des pelouses sur sols calaminaires des Violetea calaminariae), Blysmus rufus (absent de France) ; en commun avec au moins une partie de l’ordre précédent : Triglochin maritima, Plantago maritima subsp. m., Festuca rubra subsp. littoralis.
Alliance Pm. Puccinellion maritimae W.F. Christ. 1927 (Föhrer Heimatbücher 16, non consulté) ; tableau 1 : colonne Pm ; tableau 6
Lectotypus nominis hoc loco : Puccinellietum maritimae W.F. Christ. 1927 (Föhrer Heimatbücher 16, non consulté).
Prés halophiles des schorres inférieurs, entrant en contact avec les slikkes à Spartina ; alliance centrale de l’ordre, guère différenciée positivement.
* Groupe de syntaxons à Spergularia media
Pm1. Puccinellietum maritimae W.F. Christ. 1927 ; a – race boréo-atlantique (Enggravslia et al., 1985, tableau 2 : colonne 8 ; Vevle, 1985, tableau 2 : colonnes 8 à 11) ; b – race suédoise intermédiaire (Gillner, 1960, tableau 13) ; c – race nord-atlantique (irlando-écossaise) à Armeria maritima et Spergularia media (Braun-Blanquet & Tüxen, 1952, tableau 25 ; Birse, 1980, tableau p. 13) ; cité d’Estonie par Korotkov et al. (1991) ; voir aussi Menke (1969).
Pm2. Halimiono portulacoidis-Puccinellietum maritimae Géhu 1976 (Géhu, 1976, tableau 16) ; = Puccinellietum maritimae sensu Tüxen (1937 : 47), se différenciant du précédent surtout par Halimione portulacoides et Limonum vulgare ; photo 4.
Pm3. Triglochino maritimae-Limonietum humilis Annezo, Bioret & Géhu 1991 (Annezo et al. 1991, tableau 2) ; Birse (1980 : 15, un seul relevé) évoque un groupement à Limonium humile nord-atlantique distinct de celui-ci qu’il rapporte à tort au Plantagini maritimae-Limonietum vulgaris.
* Groupe de syntaxons à Festuca rubra subsp. littoralis
Pm4. Juncetum gerardii ‘Warming 1906’ ; a – race boréo-atlantique (Enggravslia et al., 1985, tableau 2 : colonnes 9 et 11) ; voir aussi Vevle (1985, tableau 2 : colonne 13) ; b – race nord-atlantique (écossaise) à Armeria maritima, Cochlearia officinalis et Festuca rubra (subsp. littoralis ?) (Birse, 1980, tableau p. 16) ; voir aussi Menke (1969). Le tableau de Juncetum gerardii des côtes sud-occidentales suédoises (Gillner, 1960, tableaux 7 et 15) montre une timide apparition d’Armeria maritima ; voir aussi Jeckel (1977, tableau 3). L’autorité de « Warming 1906 » ne peut être conservée (art. 2a), il faudrait donc préciser une autorité postérieure à 1910 : Jeckel (1977) puis Korotkov et al. (1991) citent ‘Nordhagen 1923’, à identifier et à vérifier (la source possible est précisée en bibliographie).
Pm5. Caricetum rectae Gillner 1960 (Gillner, 1960, tableau 8).
* Autre syntaxon
Pm6. Puccinellietum fasciculatae Beeftink 1965 (Géhu, 1976, tableau 17) ; souvent cité dans l’alliance suivante où cependant il n’est pas mieux placé.
On n’a pas repris ici le Blysmetum rufi Gillner 1960 placé dans le Loto glabri-Trifolion fragiferi dans notre synthèse antérieure (de Foucault & Catteau, 2012).
Alliance PSs. Puccinellio maritimae-Spergularion marinae Beeftink 1965 (De zoutvegetatie van ZW-Nederland… : 113, sub Puccinellio maritimae-Spergularion salinae) ; tableau 1 : colonne PSs ; tableau 7
[syn. : Puccinellion distantis Géhu & Rivas Mart. in Choisnet, C. Roux, Cordonnier, Hugonnot & Bioret 2020 (BIOM 1 : 86) nom. illeg., non Puccinellion distantis (Soó 1933) Wendelb. 1943 ; corresp. syntax. : Puccinellio maritimae-Spergularienion marinae (Beeftink 1965) Géhu & Géhu-Franck 1984 (Doc. Phytosoc., NS, VIII : 55, sub Puccinellio maritimae-Spergularienion salinae)]
Lectotypus nominis hoc loco : Spergulario salinae–Puccinellietum distantis Feekes ex Vlieger 1938 (Ned. Kruidk. Arch., serie 3, 48).
Prés oligohalophiles des sites continentaux ou en voie de continentalisation, optimum de Puccinellia distans au sein de l’ordre, remplaçant ici Puccinellia maritima.
PSs1. Spergulario marinae–Puccinellietum distantis Feekes ex Vlieger 1938 ; a – d’après Feekes (1943, tableau III) ; b – d’après Dangien et al. (1974, tableau 3bis), Géhu et al. (1976, tableau 10), Frileux & Géhu (1976, tableau IX), Celinski & Wika (1976, tableau 1) ; voir aussi Gillner (1960, tableau 14) et Jeckel (1977, tableau 1).
PSs2. Spergulario mediae-Puccinellietum distantis B. Foucault 2018 (de Foucault, 2018, tableau 1 : relevés 1 à 3, sub Spergulo mediae-Puccinellietum distantis) ; se distingue de PSs1 notamment par l’absence de taxons littoraux tels que Tripolium pannonicum et Puccinellia maritima.
PSs3. Groupement à Spergularia marina (Tüxen, 1937 : 47).
PSs4. Juncetum gerardii sensu Celinski & Wika 1976 (Celinski & Wika, 1976, tableau 1).
PSs5. Plantagini maritimae-Puccinellietum fontanae Choisnet, C. Roux, Cordonnier, Hugonnot & Bioret 2020 (Choisnet et al., 2020, tableau 2 : relevés D1 à D39 et C1 à C19) ; photo 5.
PSs6 et PSs7. Du sud du delta du Danube, Géhu et al. (1994) définissent les Tripolio pannonici-Juncetum gerardii Géhu, Roman & Boullet 1994 (leur tableau 10, sub Astero pannonici-Juncetum gerardii, en PSs6) et Tripolio pannonici-Puccinellietum distantis Géhu, Roman & Boullet 1994 (leur tableau 11, sub Astero pannonici-Puccinellietum distantis, en PSs7) qu’ils rangent dans le Juncion gerardii Wendelb. 1943 ; par la forte présence de Puccinellia distans, ils rappellent cependant beaucoup le Puccinellio maritimae-Spergularion marinae, à part l’absence des taxons caractérisant les Lysimachio-Puccinellietalia maritimae.
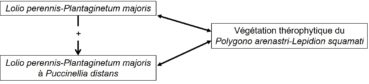
Une salinisation intervenant localement dans certaines régions non littorales, soit par dépôt de sel (sur les routes en hiver ; Géhu, 1983), soit par réaction chimique aboutissant à une libération de Na2CO3 (Matysiak, 1993), se traduit sur le plan phytosociologique par l’apparition d’espèces oligohalophiles telles que Puccinellia distans au sein d’une végétation initiale glycophile. Les observations de Vanden Berghen (1994) précisent quelque peu cette dynamique dans le cas de mosaïques de communautés fortement piétinées, selon le schéma systémique de la figure 1 déduit de son tableau I :
avec les flèches systémiques suivantes :
flèche spatiale de superposition en mosaïque ↔
flèche temporelle d’évolution →
alcalinisation édaphique : +.
On remarque que la salinisation n’a guère d’effet sensible sur la végétation thérophytique, aucun taxon indicateur n’y apparaissant.
Alliance Am. Armerion maritimae Braun-Blanq. & De Leeuw 1936 (Ned. Kruidk. Arch. 46 : 373) ; tableau 1 : colonne Am ; tableau 8
Typus allianciae : Armerio maritimae-Festucetum arenariae Braun-Blanq. & De Leeuw 1936 (Ned. Kruidk. Arch. 46 : 374).
Prés halophiles des schorres supérieurs à Armeria maritima, Artemisia maritima subsp. m. (photo 5), Festuca rubra subsp. littoralis, Frankenia laevis, Cochlearia anglica, Limonium dodartii. Deux sous-alliances bien confirmées par le tableau 8.
Sous-alliance Eu-Armerienion maritimae
[syn. : Festucenion littoralis Géhu 1976 (Colloq. Phytosoc. IV : 431), Limonio vulgaris-Plantaginenion maritimae Géhu & Géhu-Franck 1984 (Doc. Phytosoc., NS, VIII : 56)]
Prés halophiles développés sur des substrats plutôt limoneux ou limono-sableux différenciés par Lysimachia maritima, Triglochin maritima, Juncus gerardii, Agrostis stolonifera s. l.
Am1. Plantagini maritimae-Limonietum vulgaris V. Westh. & Segal 1961 (Géhu, 1976, tableau 18) ; photo 6.
Am2. Cochleario anglicae-Plantaginetum maritimae Géhu 1976 (Ibid., tableau 19) ; photo 8.
Am3. Festucetum littoralis Corill. 1953 (Ibid., tableau 20).
Am4. Juncetum gerardii sensu Géhu 1976 (Ibid., tableau 21) ; ce syntaxon est un homonyme plus récent du Juncetum gerardii boréal (cf. supra, syntaxon Pm4), il devrait donc être renommé. La comparaison entre les colonnes Am4 et Am5 montre toutefois son inclusion possible dans le suivant.
Am5. Festuco littoralis-Juncetum gerardii Géhu in Géhu & Géhu-Franck 1982 (Géhu & Géhu-Franck, 1982, tableau 55).
Am6. Juncetum gerardii sensu Braun-Blanq. & Tüxen 1952 (Braun-Blanquet & Tüxen, 1952, tableau 26 : Juncetum gerardii).
Am7. Artemisietum maritimae Hocquette 1927 ; a – race franco-atlantique (Géhu, 1976, tableau 26) ; b – race nord-est-atlantique (Braun-Blanquet & De Leeuw, 1936 : 383 ; Festuca arenaria est sans doute une erreur pour F. rubra subsp. littoralis) ; c – race boréo-atlantique (Suède ; Gillner, 1960, tableau 16) ; Catteau et al. (2021 : 364) synonymisent ce nom avec le Festucetum littoralis (cf. Am3), ce que le tableau 8 ne confirme pas. Ce nom est un homonyme contemporaison de l’Artemisietum maritimae Soó 1927 (cf. syntaxon Fp3), homonymie régie par l’article 33 : on propose de conserver le nom de Soó et de renommer celui de Hocquette en Festuco littoralis-Artemisietum maritimae (Hocquette 1927) nom. nov. hoc loco, typus nominis hoc loco : relevé 6 du tableau 14 in Géhu, Caron & Bon (1976, Colloq. Phytosoc. IV : 214).
Am8. Armerio maritimae-Festucetum arenariae Braun-Blanq. & De Leeuw 1936 (Braun-Blanquet & De Leeuw, 1936, tableau 5).
Sous-alliance Frankenio laevis-Armerienion maritimae Géhu & Géhu-Franck in Géhu 1976 (Colloq. Phytosoc. IV : 431)
Lectotypus nominis hoc loco : Cochleario anglicae-Frankenietum laevis Géhu 1976 (Colloq. Phytosoc. IV : 446).
Prés halophiles développés sur des substrats plutôt sableux et à plus forte dessiccation estivale, différenciés par Frankenia laevis (photo 9), Limonium auriculiursifolium.
Am9. Frankenio laevis-Limonietum auriculiursifolii (Meslin 1936) G. Lemée 1952, incl. Frankenio laevis-Limonietum normannici Géhu & Bioret 1992 (Géhu, 1976, tableau 23, sub Frankenio laevis-Limonietum lychnidifolii) ; voir aussi Géhu & Bioret (1992) ; photo 10.
Am10. Cochleario anglicae-Frankenietum laevis Géhu 1976 (Ibid., tableau 24).
Am11. Limonio vulgaris-Frankenietum laevis Géhu & Delzenne 1976 (Géhu & Delzenne, 1976, tableau 14).
Am12. Limonietum lychnidifolio-dodartii Géhu & Géhu-Franck 1974 (Géhu, 1976, tableau 25).
Am13. Frankenio laevis-Limonietum binervosi Bioret & Lahondère 2010 (Bioret & Lahondère, 2010, tableau 2, sub Frankenio laevis-Limonietum occidentalis).
Am14. Frankenio laevis-Limonietum auriculiursifolii sensu Bioret & Lahondère 2010 (Ibid., tableau 3) ; cette association est assez différente de Am9, dont il constitue un homonyme illégitime (présence significative de Suaeda vera subsp. v., Limonium dodartii, Sarcocornia fruticosa, Juncus maritimus ; absence ou rareté de Festuca rubra subsp. littoralis, Armeria maritima, Elytrigia acuta) : Halimiono portulacoidis-Limonietum auriculiursifolii (Bioret & Lahondère 2010) B. Foucault, Bioret & Lahondère nom. nov. hoc loco, typus nominis hoc loco : relevé 2 du tableau 3 in Bioret & Lahondère (2010, Braun-Blanquetia 46 : 132).
Am15. Frankenio laevis-Limonietum ovalifolii Bioret & Lahondère 2010 (Ibid., tableau 4).
Alliance LJm. Lysimachio maritimae-Juncion maritimi Géhu & Géhu-Franck ex Géhu in Bardat, Bioret, Botineau, Boullet, Delpech, Géhu, Haury, Lacoste, Rameau, J.-M. Royer, G. Roux & Touffet 2004 (Patrimoines naturels 61 : 27, sub Glauco maritimae-Juncion maritimi) ; tableau 1 : colonne LJm ; tableau 9
[corresp. syntax. : Junco maritimi-Caricenion extensae Géhu 1976 (Colloq. Phytosoc. IV : 431)]
Typus allianciae : Junco maritimi-Caricetum extensae (Corill. 1953) Parriaud in Géhu 1976 (Colloq. Phytosoc. IV : 444) désigné par Géhu in Bardat et al. (2004, Patrimoines naturels 61 : 27).
Prés halophiles des schorres soumis à des infiltrations d’eaux douces d’origine continentale à Juncus maritimus, Carex extensa (deux taxons fort peu fréquents ailleurs dans cet ordre), Juncus anceps, Triglochin palustris.
LJm1. Oenantho lachenalii-Juncetum maritimi Tüxen 1937 (Tüxen, 1937 : 67).
LJm2. Junco maritimi-Caricetum extensae (Corill. 1953) Parriaud in Géhu 1976 (Géhu, 1976, tableau 22).
LJm3. Junco ancipitis-Caricetum extensae Braun-Blanq. & De Leeuw 1936 (Braun-Blanquet & De Leeuw, 1936 : 381).
LJm4. Carici punctatae-Plantaginetum maritimae Glemarec & Wattez 2019 (Glemarec & Wattez, 2019, tableau 2).
LJm5. Juncetum gerardii sensu Castrov. 1975 (Castroviejo, 1975, tableau 3).
LJm6. Sarcocornio perennis-Limonietum vulgaris Bueno Sánchez & Fern. Prieto in Bueno Sánchez 1997 (Bueno Sánchez, 1997, tableau 16).
Alliance SPm. Spergulario mediae-Plantaginion maritimae all. nov. hoc loco ; tableau 1 : colonne SPm ; tableau 10
Typus nominis hoc loco : Artemisio gargantae-Puccinellietum pungentis Barrera & Cirujano 1986 (Trab. Dep. Botánica 13 : 112, sub Artemisio gallicae-Puccinellietum pungentis).
Prés halophiles centre- à nord-ibériques sous influence atlantique assez distincts de ceux du Juncion maritimi où ils ont été souvent placés et paraissant mieux à leur place dans les Lysimachio-Puccinellietalia maritimae (présence de Plantago maritima subsp. m., Puccinellia maritima, rareté des taxons caractérisant les Juncetalia maritimae).
SPm1. Elytrigio curvifoliae-Iridetum reichenbachianae (Rivas Mart. in Rivas Mart. & M.J. Costa 1976) Cirujano 1981 (Rivas-Martínez & Costa, 1976, tableau 1, sub Irido spuriae-Juncetum maritimi), = Elymo curvifolii-Juncetum maritimi Rivas Mart. 1984 (Rivas-Martínez, 1984 : 10).
SPm2. Agrostio stoloniferae-Juncetum maritimi Izco, P. Guitián & J.M. Sánchez 1993 (Izco et al., 1993, tableau 3).
SPm3. Limonio binervosi-Frankenietum laevis Izco & Sánchez 1997 (Izco & Sánchez, 1997, tableau X).
méditSPm4. Puccinellio maritimae-Juncetum maritimi Bueno & Fern. Prieto in Bueno 1997 (Bueno Sánchez, 1997, tableau 12).
SPm5. Artemisio gargantae-Puccinellietum pungentis Barrera & Cirujano 1986 corr. Rivas Mart. et al. 2002 (Barrera & Cirujano, 1986, tableau 1, sub Artemisio gallicae-Puccinellietum pungentis).
SPm6. Plantagini maritimae-Camphorosmetum monspeliacae Ladero, Navarro, C. Valle, Marcos, Ruiz & M.T. Santos 1984 (Ladero et al., 1984, tableau 12).
Ordre 3. Juncetalia maritimi Braun-Blanq. ex Horvatić 1934 (Prirod. Istraž. Kral. Jugosl. 19 : 269) ; tableau 1 : colonnes Jm à SJa
[syn. : Juncetalia maritimi Braun-Blanq. 1931 (Comm. SIGMA 9 : 39) nom. inval. (art. 2b)]
Typus allianciae : Juncion maritimi Braun-Blanq. ex Horvatić 1934 (Prirod. Istraž. Kral. Jugosl. 19 : 270).
Prés halophiles méditerranéens à Limonium narbonense (photo 11), Puccinellia festuciformis subsp. f. (photo 12), Limbarda crithmoides subsp. longifolia, Aeluropus littoralis (photo 13), Juncus acutus subsp. a., Sonchus maritimus, S. crassifolius, Elytrigia elongata subsp. e., E. curvifolia, Scorzonera parviflora, Plantago cornutii ; optimum de Juncus maritimus et Carex extensa au sein de la classe.
Alliance Jm. Juncion maritimi Braun-Blanq. ex Horvatić 1934 (Prirod. Istraž. Kral. Jugosl. 19 : 270), incl. Puccinellion festuciformis Géhu & Scoppola in Géhu, Scoppola, Caniglia, Marchiori & Géhu-Franck 1984 (Doc. Phytosoc., NS, VIII : 493) nom. inval. et illeg. (art. 2d, 3o, 5, 31) non Puccinellion festuciformis Micevski 1965) ; tableau 1 : colonne Jm ; tableau 11
[syn. : Juncion maritimi Braun-Blanq. 1931 (Comm. SIGMA 9 : 39) nom. inval. (art. 2b)]
Lectotypus nominis hoc loco : Juncetum maritimo-acuti Horvatić 1934 (Prirod. Istraž. Kral. Jugosl. 19 : 272).
Prés halophiles fortement hygrophiles ; cœur de l’ordre sans différenciation floristique particulière.
* Groupe de syntaxons à Sarcocornia fruticosa, Puccinellia festuciformis subsp. f., Juncus subulatus…
Jm1. Elytrigio elongatae-Limbardetum longifoliae Braun-Blanq. in Braun-Blanq., Roussine & Nègre 1952 (Braun-Blanquet et al., 1952 : 108, sub Agropyro-Inuletum crithmoidis).
Jm2. Junco gerardii-Triglochinetum maritimae Braun-Blanq. ex Braun-Blanq., Roussine & Nègre 1952 (Ibid. : 115).
Jm3. Caricetum divisae Braun-Blanq. ex Braun-Blanq., Roussine & Nègre 1952 (Ibid. : 117) ; décrits dans le même document, Jm2 et Jm3 sont très proches l’un de l’autre et pourraient être interprétés comme deux variations de la même association à définir.
Jm4. Puccinellio festuciformis-Aeluropodetum littoralis Géhu & M.J. Costa in Géhu, M.J. Costa, Scoppola, Biondi, Marchiori, Peris, Géhu-Franck, Caniglia & Veri 1984 ; a – selon Géhu, Costa et al. (1984a, tableau 21) : b – selon Noble & Baret (Noble & Baret, 2021, tableau 6 : colonne 3).
Jm5. Bolboschoeno maritimi-Juncetum subulati Géhu, Biondi, Géhu-Franck & M.J. Costa 1992 ; a – selon Noble & Baret (2021, tableau 6 : colonne 4) ; b – selon Géhu, Biondi et al. (1992, tableau 20, sub Scirpo-Juncetum subulati). Présent dans l’Aude :
Narbonne, « Le Cercle », bord d’un chemin rural, N 43° 09’ 11,5’’, E 3° 01’ 16,9’’, le 19/07/2020, 90 %, 25 m², 7 taxons
Juncus subulatus 4, Phragmites australis 3, Agrostis stolonifera 2, Bolboschoenus maritimus *m. 1, Limonium narbonense 1, Symphyotrichum squamatum 1, Paspalum distichum 1.
Jm6. Aeluropodo littoralis-Juncetum maritimi Bouabdallah & B. Foucault ass. nov. hoc loco [syn. : Juncetum maritimi Bouabdallah 1992 (La végétation steppique sur sols salés… : 106) nom. ined.] (Bouabdallah, 1992, tableau II.10), typus nominis hoc loco : relevé 8 du tableau II.10 in Bouabdallah 1992 (La végétation steppique sur sols salés… : 106) publié ci-dessous :
Algérie méridionale, 7 taxons
- JUNCETEA MARITIMI: Juncus maritimus 1, Limonium delicatulum 3, Frankenia thymifolia 3, Aeluropus littoralis 3,
- autres taxons : Arthrocnemum macrostachyum +, Phragmites australis +, Sarcocornia fruticosa +.
Jm7. Puccinellio festuciformis-Juncetum maritimi Géhu in Géhu, M.J. Costa, Scoppola, Biondi, Marchiori, Peris, Géhu-Franck, Caniglia & Veri 1984 ; a – selon Géhu, Costa et al. (1984a, tableau 22) ; b – selon Noble & Baret (2021, tableau 6 : colonne 6) ; c – selon Géhu & Biondi (1994, tableau 31).
Jm8. Juncetum acuti Molin. & Tallon 1969 ; a – selon Noble & Baret (2021, tableau 6 : colonne 7) ; b – selon Géhu, Biondi et al. (1992, tableau19).
Jm9. Limonio narbonensis-Caricetum extensae Géhu & Biondi 1994 (Géhu & Biondi, 1994, tableau 32).
Jm10. Limonio narbonensis-Puccinellietum festuciformis Géhu & Scoppola in Géhu, Scoppola, Caniglia, Marchiori & Géhu-Franck 1984 (Géhu et al., 1984, tableau 15, sub Limonio-Puccinellietum palustris).
Jm11. Polygono equisetiformis-Juncetum maritimi J.C. Costa in J.C. Costa, Lousã & Espírito-Santo 1997 (Costa et al., 1997, tableau 14).
Jm12. Elytrigio elongatae-Juncetum maritimi Alcaraz, Garre, Peinado & Martínez-Parras 1986 (Sivim, extrait le 08/03/2021, sub Elymo elongati-Juncetum maritimi).
Jm13. Juncetum maritimo-subulati Alcaraz 1984 corr. Alcaraz, P. Sánchez, De la Torre, Ríos & J. Alvarez 1991 (Sivim, extrait le 08/03/2021).
Jm14. Spartino versicoloris-Juncetum maritimi O. Bolòs 1962 (Sivim, extrait le 08/03/2021) ; Biondi (1992b) décrit sous le même nom (Junco maritimi-Spartinetum junceae) une association du nord de la Sardaigne qu’il considère comme nouvelle et qui cependant n’en diffère guère ; voir aussi Filigheddu et al. (2000, tableau 12) et Bertacchi et al. (2021, tableau 10).
Jm15. Caro foetidi-Juncetum maritimi Esteve & Varo 1975 (Sivim, extrait le 08/03/2021).
Jm16. Puccinellio festuciformis-Juncetum subulati Géhu, Biondi, Géhu-Franck & Arnold 1986 (Géhu et al., 1986, tableau 12).
Jm17. Centaureo dracunculifoliae-Lotetum jordanii Esteve & Varo 1975 (Sivim, extrait le 08/03/2021, sub Centaureo dracunculifoliae-Dorycnietum gracilis).
* Groupe de syntaxons à Arthrocnemum macrostachyum
Jm18. Limonio narbonensis-Juncetum gerardii Géhu & Biondi 1994 (Géhu & Biondi, 1994, tableau 33).
Jm19. Frankenio hirsutae-Juncetum maritimi Bartolo, Brullo, De Marco, Dinelli, Signorello & Spampinato 1992 (Bartolo et al., 1992, tableau 11, sub Frankenio hirsuti-Juncetum maritimi).
Jm20. Limonio retiramei-Juncetum acuti Bartolo, Brullo, De Marco, Dinelli, Signorello & Spampinato 1992 (Bartolo et al., 1992, tableau 10, sub Limonio dictyocladi-Juncetum acuti).
* Groupe de syntaxons à Samolus valerandi
Jm21. Limonio narbonensis-Juncetum maritimi Teles in P. Silva & Teles 1972 corr. Rivas Mart. et al. 1980 (Izco et al., 1993, tableau 2, sub Limonio serotini-Juncetum maritimi).
Jm22. Juncetum maritimo-acuti Horvatić 1934 (Horvatić, 1934, tableau XVI ; Horvatić, 1939, tableau X).
Jm23. Scorzonero humilis–Juncetum maritimi Horvatić 1934 (Horvatić, 1934, tableau XVIII, sub Junco-Scorzoneretum candollei).
* Autres syntaxons
Jm24. Cuscuto cesatianae-Phyletum nodiflorae Stešević, Küzmič, Milanović, Stanišić-Vujačić & Šilc 2019 (Stešević et al., 2019, tableau 2).
Jm25. Dittrichio viscosae-Juncetum acuti Bacchetta, Casti & Zavattero 2007 (Bacchetta et al., 2007, tableau 4).
On ne retient pas ici l’Oenantho fistulosae-Lotetum glabri Mercadal 2020, prairie oligohalophile de bas niveau topographique mieux à sa place dans le Ranunculo ophioglossifolii-Oenanthion fistulosae B. Foucault in B. Foucault & Catteau 2012 (Mercadal, 2019, tableau 122, 2020), malgré l’absence du premier taxon éponyme d’alliance.
Le Suaedo verae-Limonietum delicatuli Quézel 1965 semble pouvoir se rattacher aussi à cette alliance (Quézel, 1965, tableau 10, sub Suaedo longifoliae-Limonietum delicatuli). Une composante thérophytique à Frankenia pulverulenta, Sphenopus divaricatus, Hornungia procumbens, Spergularia marina, Polypogon monspeliensis s’y infiltre (surtout au niveau du relevé 4 ; Frankenietalia pulverulentae, Saginetea maritimae). Les autres groupements halophiles décrits par cet auteur ne sont pas repris ici, étant plutôt chaméphytiques et riches en Amaranthaceae.
Du désert tunisien, a été évoqué un pré halophile hygrophile à Limonum tunetanum, Juncus maritimus, Carex extensa, Elytrigia elongata, Limbarda crithmoides subsp. longifolia, Sonchus maritimus (de Foucault, 2013).
Malgré l’éloignement géographique, il semble bien que le Juncetum subulati décrit des environs d’Aboukir (côte égyptienne) par Géhu, Arnold et al. (1992, tableau 23) relève aussi de cette alliance.
Alliance Pca. Puccinellion caespitosae Rivas Mart. in Rivas Mart. & M.J. Costa 1976 (Colloq. Phytosoc. IV : 82, sub Puccinellion fasciculatae), incl. Soncho crassifolii-Juncenion maritimi Rivas Mart. 1984 (Stvdia Bot. 3 : 11), typifié par le Schoeno nigricantis-Plantaginetum maritimae Rivas Mart. 1984 ; tableau 1 : colonne Pca ; tableau 12
Lectotypus nominis hoc loco : Aeluropodo littoralis-Puccinellietum caespitosae (Rivas Goday 1956) Rivas Mart. & M.J. Costa 1976 (Colloq. Phytosoc. IV : 84).
Prés halophiles ibériques à Puccinellia caespitosa, Juncus subulatus, Plantago crassifolia.
Pca1. Limbardo crithmoidis-Juncetum subulati Rivas Mart., Báscones, T.E. Díaz, Fern.Gonz. & Loidi 1991 (Sivim, le 08/03/2021).
Pca2. Aeluropodo littoralis-Juncetum subulati Cirujano 1981 (Cirujano, 1981, tableau 17).
Pca3. Aeluropodo littoralis-Puccinellietum caespitosae (Rivas Goday 1956) Rivas Mart. & M.J. Costa 1976 (Rivas-Martínez & Costa, 1976, tableau 4, sub Aeluropo littoralis-Puccinellietum fasciculatae).
Pca4. « Bupleuro tenuissimi-Juncetum gerardii Rivas Mart. in Rivas Mart. & M.J. Costa 1976 » (Rivas-Martínez & Costa, 1976, tableau 5) ; on pourrait mettre à part la composante thérophytique à Bupleurum tenuissimum (V sur sept relevés), Hordeum marinum (III), Plantago coronopus subsp. c. (II), Atriplex patula (II), à rattacher aux Frankenietalia pulverulentae, dans les Saginetea maritimae.
Pca5. Puccinellio caespitosae-Artemisietum gallicae Cirujano 1981 corr. Rivas Mart. et al. 2002 (Cirujano, 1981, tableau 20, sub Puccinellio fasciculatae-Artemisietum gallicae).
Pca6. Schoeno nigricantis-Plantaginetum maritimae Rivas Mart. 1984 (Cirujano, 1981, tableau 16, sub Schoeno nigricantis-Plantaginetum crassifoliae) nom. illeg. (non Schoeno nigricantis-Plantaginetum maritimae Horvatić 1934), renommé (art. 39) ici Lino maritimi–Plantaginetum maritimae (Rivas Mart. 1984) nom. nov. hoc loco, typus nominis hoc loco : relevé 4 du tableau 16 in Cirujano (1981, Anales Jard. Bot. Madrid 38 (1) : 214).
Pca7. Puccinellietum caespitosae Rivas Goday 1956 corr. Rivas Mart. et al. 2002 (Rivas Goday, 1955, tableau 24, sub Puccinellietum convolutae).
Pca8. Soncho crassifolii-Juncetum maritimi Braun-Blanq. & O. Bolòs 1957 (Braun-Blanquet & de Bolòs 1957, tableau 24).
Pca9. Aeluropodo littoralis-Elytrigietum acutae Corbetta & Pirone in Corbetta, Gratani, Moriconi & Pirone 1992 (Corbetta et al., 1992, tableau 22, sub Aeluropo littoralis-Agropyretum pungentis).
Alliance Pf. Puccinellion festuciformis Micevski 1965 (Acta Mus. Maced. Sci. Nat. 10, non consulté, sub Puccinellion convolutae) ; tableau 1 : colonne Pf ; tableau 13
Lectotypus nominis hoc loco : Puccinellietum festuciformis Micevski 1965 (Acta Mus. Maced. Sci. Nat. 10, non consulté, sub Puccinellietum convolutae).
Prés halophiles centre- et sud-est-européens, différenciés négativement par l’absence d’un bon nombre de taxons caractérisant l’ordre et la classe, plus positivement par Limonium gmelinii, L. bellidifolium, Juncus littoralis, Halimione verrucifera, Artemisia santonicum ; Spergularia media, taxon plutôt inféodé aux Lysimachio-Puccinellietalia maritimae, y est aussi bien représenté. Plusieurs associations ont notamment été décrites, quoique souvent sur un faible nombre de relevés, par Géhu et al. (1994).
Pf1. Puccinellio festuciformis-Limonietum bellidifolii Géhu, Roman & Boullet 1994 (Géhu et al., 1994, tableau 4, sub Puccinellio convolutae-Limonietum danubialis).
Pf2. Puccinellio festuciformis-Halimionetum verruciferae Géhu, Roman & Boullet 1994 (Ibid., tableau 6, sub Puccinellio convolutae-Halimionetum verruciferae).
Pf3. « Halimiono pedunculatae-Juncetum maritimi » Géhu, Roman & Boullet 1994 (Ibid., tableau 5), présentant une composante thérophytique à Halimione pedunculata.
Pf4. Limonio gmelinii-Artemisietum santonici (Tzopa 1939) Géhu, Roman & Boullet 1994 (Ibid., tableau 7).
Pf5. Artemisio santonici-Juncetum littoralis (Popescu & Santa 1976) Géhu, Roman & Boullet 1994 (Ibid., tableau 8).
Pf6. Juncetum littoralis Popescu & Sanda 1976 (Zamfirescu, 2011, tableau I : relevés 6 à 10).
Pf7. Juncetum maritimi sensu Zamfirescu 2011 (Ibid., tableau I : relevés 1 à 5).
Pf8. Juncetum maritimi sensu Tzonev, Lysenko, Gussev & Zhelev 2008 (Tzonev et al., 2008, tableau 2 : « Juncetum maritimae »).
Pf9. Diantho pallidiflori-Puccinellietum festuciformis Tzonev, Lysenko, Gussev & Zhelev 2008 (Ibid., tableau 3, sub Diantho pallidiflori-Puccinellietum convolutae) ; les relevés 1 à 4, 7 à 11, 48, 54 et 58 à 55 revèlent une communauté thérophytique associée combinant (présences sur treize relevés) Polygonum arenarium subsp. pulchellum V, Hordeum geniculatum III, Atriplex tatarica II, Bupleurum tenuissimum II, Schenkia spicata I, Spergularia marina +, Suaeda maritima +, Hordeo geniculati-Polygonetum pulchelli ass. nov. hoc loco, typus nominis hoc loco : composante thérophytique du relevé 48 du tableau 3 in Tzonev et al. (2008, Hacquetia 7 (2) : 118) :
Atolovo village (Yambol district), 9 m², 6 taxons
Polygonum arenarium subsp. pulchellum 1, Hordeum geniculatum 1, Atriplex tatarica 2a, Bupleurum tenuissimum +, Spergularia marina 2a, Suaeda maritima +.
Pf10. Groupement à Artemisia santonicum (Ibid., tableau 5).
Pf11. Elytrigietum elongatae Şerbănescu 1968 (Zamfirescu, 2011, tableau II).
Pf12. Limonio gmelinii-Juncetum gerardii Géhu & Uslu 1989 (Géhu & Uslu, 1989, tableau 23 : relevés 1 à 3 ; Géhu et al., 1994, tableau 9).
Pf13. Limonio gmelinii-Spergularietum nicaeensis Babalonas & Papastergiadou 1990 (Babalonas & Papastergiadou, 1990, tableau 1 : syntaxon e).
Pf14. Limonio gmelinii-Aerulopodetum littoralis (Babalonas 1979) Géhu, Biondi, Géhu-Franck & Arnold 1986 (Géhu, Biondi et al., 1986, tableau 13 : relevés 1 et 2).
Pf15. Puccinellio festuciformis-Caricetum extensae Géhu & Uslu 1989 (Géhu & Uslu, 1989, tableau 23 : relevé 4).
Pf16. Halimiono portulacoidis-Artemisietum santonici Géhu & Uslu 1989 (Ibid., tableau 22).
Pf17. « Halimiono pedunculatae-Aerulopodetum littoralis » Géhu, Roman & Boullet 1994 (Géhu, Roman & Boullet, 1994, tableau 12, ‘…-Aerulopetum…’, art. 41b), présentant une composante thérophytique à Halimione pedunculata, Salicornia perennans subsp. p. (sub S. patula) et Suaeda maritima (Thero-Suaedetea splendentis).
Pf18. Aeluropodetum littoralis sensu Tzonev, Lysenko, Gussev & Zhelev 2008 (Tzonev et al., 2008, tableau 2 : « Aeluropetum littoralis »).
Pf19. « Bupleuro tenuissimi-Camphorosmetum monspeliacae Tzonev, Lysenko, Gussev & Zhelev 2008 » (Tzonev et al., 2008, tableau 4). La présence de la thérophyte Bupleurum tenuissimum incite à définir un groupement thérophytique caractérisé par la flore suivante (synthèse de la composante thérophytique des relevés 20, 23 à 25, 53, 56, soit six relevés) : B. tenuissimum V, Pholiurus pannonicus IV, Polygonum arenarium subsp. pulchellum IV, Bromus scoparius II et, de présence I, Lepidium ruderale, Polygonum aviculare subsp. arenastrum, Portulaca oleracea, Heliotropium supinum, Hordeum geniculatum : Pholiuro pannonici-Bupleuretum tenuissimi ass. nov. hoc loco, typus nominis hoc loco : composante thérophytique du relevé 23 du tableau 4 in Tzonev et al. (2008, Hacquetia 7 (2) : 120)
Bikovo village (Sliven district), 25 m², 4 taxons
Bupleurum tenuissimum +, Pholiurus pannonicus 1, Polygonum arenarium subsp. pulchellum +, Bromus scoparius +.
Pf20. Elytrigietum elongatae Babalonas & Papastergiadou 1990 nom. illeg. (non Elytrigietum elongatae Şerbănescu 1968, cf. Pf11) (Babalonas & Papastergiadou, 1990, tableau 1 : syntaxon f), renommé (art. 39) ici Carici divisae–Elytrigietum elongatae (Babalonas & Papastergiadou 1990) nom. nov. hoc loco, typus nominis hoc loco : relevé 37 du tableau 1 in Babalonas & Papastergiadou (1990, Tuexenia 10 : 118).
Pf21. Puccinellietum festuciformis Micevski 1965 (Ibid., tableau 1 : syntaxon g, sub Puccinellietum convolutae).
Alliance Pcr. Plantaginion crassifoliae Braun-Blanq. ex Braun-Blanq., Roussine & Nègre 1952 (Les groupements végétaux de la France méditerranéenne : 118) ; tableau 1 : colonne Pcr ; tableau 14
[syn. : Plantaginion crassifoliae Braun-Blanq. 1931 (Comm. SIGMA 9 : 39) nom. inval. (art. 2b)]
Lectotypus nominis hoc loco : Schoeno nigricantis-Plantaginetum crassifoliae Braun-Blanq. ex Braun-Blanq., Roussine & Nègre 1952 (Les groupements végétaux de la France méditerranéenne : 118).
Prés halophiles de transition vers la végétation dunaire sur sols sablo-graveleux enrichis en matières organiques et à fortes variations d’humidité, caractérisés par Plantago crassifolia, Schoenus nigricans, Linum maritimum, Lotus jordanii, Oenanthe lachenalii, Scirpoides holoschoenus subsp. australis.
Mercadal (2019, 2020) propose de subdiviser cette alliance en deux sous-alliances.
* Eu-Plantaginenion crassifoliae
Pcr1. Schoeno nigricantis-Plantaginetum crassifoliae Braun-Blanq. ex Braun-Blanq., Roussine & Nègre 1952 [syn. : Schoeno nigricantis-Plantaginetum crassifoliae Braun-Blanq. 1931 (Comm. SIGMA 9 : 39) nom. inval. (art. 2b)] (Braun-Blanquet et al., 1952 : 118) ; photo 14.
Pcr2. Schoeno nigricantis-Plantaginetum maritimae Horvatić 1934 (Horvatić, 1934, tableau XXII) ; deux relevés ont aussi été publiés publiés ultérieurement par le même auteur (1939, tableau p. 48).
Pcr3. Junco acuti-Schoenetum nigricantis Géhu, Biondi, Géhu-Franck & Taffetani 1987 (Géhu, Biondi et al., 1987, tableau 9) ; initialement décrite du littoral oriental de la Corse, cette association se retrouve au niveau de l’archipel de la Maddalena, au nord de la Sardaigne (Biondi, 1992b, tableau 15).
Pcr4. Anacamptido palustris–Centaureetum dracunculifoliae Curcó 2001 (Mercadal, 2019, tableau 127 : colonne OC, sub Orchido–Centaureetum dracunculifoliae).
Pcr5. Scirpoidetum australis Braun-Blanq. ex Braun-Blanq. in Braun-Blanq., Roussine & Nègre 1952 (Braun-Blanquet et al., 1952 : 120, sub Holoschoenetum romani).
Pcr6. Artemisio gallicae-Juncetum acuti Boira 1992 (Sivim, extrait le 08/03/2021).
Pcr7. Plantagini crassifoliae-Caricetum extensae Géhu & Biondi 1988 (Géhu & Biondi, 1988, tableau 15).
Pcr8. Groupement à Plantago crassifolia-Schoenus nigricans (Géhu, Costa et al., 1984b, tableau 11), assez différent de Pcr1.
Pcr9. Centaureo dracunculifoliae-Lotetum jordanii Esteve & Varo 1976 (Mercadal, 2019, tableau 127 : colonne CD, sub Centaureo dracunculifoliae-Dorycnietum gracilis).
* Limonio virgati-Plantaginenion crassifoliae Mercadal 2020 (Acta Bot. Malac. 45 : 110)
Typus suballianciae : Limonio virgati-Plantaginetum crassifoliae Gesti & Vilar ex Mercadal 2020 (Acta Bot. Malac. 45 : 110)
Pcr10. Limonio virgati-Plantaginetum crassifoliae Mercadal 2020 (Mercadal, 2019, tableau 134).
Pcr11. Trifolio squamosi-Plantaginetum crassifoliae Mercadal 2020 (Mercadal, 2019, tableau 136).
* Autre syntaxon
Pcr12. Junco rigidi-Schoenetum nigricantis Tadros 1954 (Tadros, 1953-54, tableau II : relevés 1 à 12). Les relevés 13 à 17 de ce tableau, décrivant le Schoenetum aegyptiacum Tadros 1954 nom. illeg. (art. 34), peuvent être interprétés comme le typicum de cette association [lectotypus nominis hoc loco : relevé 17 du tableau II in Tadros (1953-54, Vegetatio IV : 108)], par opposition au limoniastretosum monopetali subass. nov. hoc loco, typus nominis hoc loco : relevé 6 du tableau II in Tadros (1953-54, Vegetatio IV : 108). Comme le montre le tableau 14, cette association est assez marginale au sein de cette alliance, elle mériterait peut-être d’être placée dans une autre unité.
On ne retient pas dans cette alliance l’Anacamptido palustris-Schedonoretum arundinacei Mercadal 2020 (Mercadal, 2019, tableau 131 sub Orchido palustris-Festucetum arundinaceae, 2020), une prairie plutôt oligohalophile.
Alliance SJa. Schizigyno sericeae-Juncion acuti all. nov. hoc loco ; tableau 1 : colonne SJa
Typus nominis hoc loco : Schizogyno sericeae-Juncetum acuti Esteve 1968 (Collect. Bot. (Barcelona) 7 : 319).
Prés halophiles canariens à Schizogyne sericea, Juncus acutus, Limonium tuberculatum, Salsola vermiculata, un peu éloignés du cœur de l’ordre. Il faut noter qu’aucun syntaxon relevant des Juncetea maritimi n’est cité de Ténérife par Rivas-Martínez et al. (1993).
SJa. Schizogyno sericeae-Juncetum acuti Esteve 1968 (Esteve, 1968, tableau p. 319) dans la colonne SJa du tableau 1.
Ordre 4. Festuco-Puccinellietalia Soó 1968, incl. Artemisio-Festucetalia pseudovinae Soó 1968 ; tableau 1 : colonnes Pd à LgJm
Typus ordinis : ?
Prés halophiles surtout pannoniques à Plantago maritima subsp ciliata, Cerastium dubium, Taraxacum besarabicum.
On ne considèrera pas ici les Scorzonero parviflorae-Juncetalia gerardii Vicherek 1973 (Vegetace ČSSR A 5 : 79) et le Scorzonero parviflorae-Juncion gerardii (Wendelb. 1943) Vicherek 1973 (Vegetace ČSSR A 5 : 80), ce dernier synonyme illégitime du Juncion gerardii Wendelb. 1943 (Wiener Bot. Z. 92 : 144), placé plutôt dans les unités supérieures subhalophiles des Agrostietea stoloniferae (de Foucault & Catteau, 2012).
Alliance Pd. Puccinellion distantis (Soó 1933) Wendelb. 1943 (Wiener Bot. Z. 92 : 131, sub Puccinellion limosae) ; tableau 1 : colonne Pd ; tableau 15 : syntaxons en Pd
Lectotypus nominis hoc loco : Puccinellietum distantis (Rapaics 1927) Soó 1930 (Magyar Biol. Kutatóint. Munkái 3, non consulté).
Prés halophiles pannoniques à Puccinellia distans, Spergularia media, Lepidium cartilagineum, Cerastium dubium.
Pd1. Puccinellietum distantis (Rapaics 1927) Soó 1930 (Vicherek, 1973, tableau 13, sub Puccinellietum limosae).
Pd2. Tripolio pannonici-Plantaginetum ciliatae (Rapaics 1927) Soó 1930 (Slavnić, 1948 : 20, sub Astero-Plantaginetum maritimae).
Le Pholiuro pannonici-Plantaginetum tenuiflorae Rapaics ex Wendelb. 1943 est surtout une association thérophytique rappelant plutôt la végétation des Saginetea maritimae ; sa variation myosuretosum minimi est totalement thérophytique, alors que sa variation puccinellietosum limosae est une mosaïque entre cette végétation thérophytique et une composante hémicryptophyto-géophytique à Puccinellia distans (présence V sur 10 relevés), Tripolium pannonicum (V), Plantago maritima subsp. ciliata (II), Artemisia maritima subsp. m. (II), sans doute à interpréter comme une forme appauvrie d’un pré halophile de la présente alliance.
Alliance Pi. Puccinellion intermediae Wendelb. 1943 (Wiener Bot. Z. 92 : 131, sub Puccinellion salinariae) ; tableau 1 : colonne Pi ; tableau 15 : syntaxons en Pi
[syn. : Puccinellion peisonis Soó 1957 (Acta Bot. Acad. Sci. Hung. 3, non consulté]
Prés halophiles à Puccinellia intermedia et Carex secalina.
Pi1. Carici secalinae-Puccinellietum intermediae Slavnić 1948 (Slavnić, 1948 : 21).
Pi2. Tripolio pannonici-Puccinellietum intermediae Slavnić 1948 (Wendelberger, 1943 : 130, sub Astero pannonici-Puccinellietum salinariae).
Pi3. Lepidio cartilaginei-Puccinellietum intermediae Slavnić 1948 (Wendelberger, 1943 : 130, sub Lepidio cartilaginei-Puccinellietum salinariae).
Alliance Fp. Festucion pseudovinae Soó in Máthé 1933 (Bot. Közl. XXX, non consulté) ; tableau 1 : colonne Fp ; tableau 15 : syntaxons en Fp
Prés halophiles à Festuca pseudovina, Artemisia maritima subsp. m., Podospermum canum, Limonium hungaricum, Achillea setacea, Artemisia santonicum subsp. patens, Ranunculus pedatus.
Fp1. Limonio hungarici-Artemisietum maritimae (Rapaics 1916) E. Ţopa 1939 (Vicherek, 1973, tableau 15, sub Statico hungarici-Artemisietum monogynae).
Fp2. Triglochino maritimae-Tripolietum pannonici Soó 1927 (Soó, 1927 : 100).
Fp3. Artemisietum maritimae Soó 1927 (Soó, 1927 : 101, sub Artemisietum salinae) ; ce nom est un homonyme contemporain de l’Artemisietum maritimae Hocquette 1927, homonymie régie par l’article 33 : on a proposé plus haut de conserver ce nom de Soó et de renommer celui de Hocquette (cf. syntaxon Am7).
Fp4. Artemisio santonici-Festucetum pseudovinae Soó in Máthé 1933 ; a – selon Dítě et al. (2010, tableau 1) ; b – selon Šmarda (1952, tableau p. 101).
Fp5. Limonio hungarici–Artemisietum santonici E. Ţopa 1939 (Ştefan et al., 2008, tableau 1, sub Statico-Artemisietum santonici).
Fp6. Achilleo setaceae-Festucetum pseudovinae Soó 1947 (Czirjak, 2010, tableau 1) ; très proche du précédent ; l’interprétation de Czirjak est-elle correcte ?
Alliance LgJm. Limonio gmelinii-Juncion maritimi Golub & Solomacha ex Dubyna & Neuhäuslová 2000 (Acta Bot. Croatica 59 (1) : 169) ; tableau 1 : colonne LgJm ; tableau 16, syntaxons en LgJm
[syn. : Limonio gmelinii-Juncion maritimi Golub & Solomacha 1988 (Byull. Moskovsk. Obshch. Isp. Prir., Otd. Biol., 93 (6) non consulté, invalidité à vérifier)]
Typus allianciae : Plantagini ciliatae-Juncetum maritimi Šeljag-Sosonko & Solomacha 1987 (Ukrayins’k. Bot. Zhurn. 44 (6), sub Plantagini salsae-Juncetum maritimi, non consulté) désigné par Dubyna & Neuhäuslová (2000, Acta Bot. Croatica 59 (1) : 169).
Prés halophiles prolongeant les halipèdes pannoniques vers les environs de la mer d’Azov (Ukraine) à Puccinellia gigantea, Limonium meyeri, Agrostis gigantea subsp. maeotica, Lysimachia maritima (optimal dans les Lysimachio-Puccinellietalia maritimae).
LgJm1. Artemisio santonici-Juncetum maritimi Šeljag-Sosonko, Neuhäuslova & Dubyna in Dubyna & Neuhäuslova 2000 (Dubyna & Neuhäuslova, 2000, tableau 1).
LgJm2. Plantagini ciliatae-Juncetum maritimi Šeljag-Sosonko & Solomacha 1987 (Ibid., tableau 2, sub Plantagini salsae-Juncetum maritimi) ; cité aussi par Korotkov et al. (1991).
LgJm3. Tripolio pannonici-Caricetum extensae Dubyna & Neuhäuslova 2000 (Ibid., tableau 3).
Des lacs salés de l’Iran sont frangés de prés halophiles à Aeluropus littoralis, Puccinellia distans… La partie droite du tableau 16 synthétise les quatre syntaxons suivants :
I-A. Halimionetum verruciferae Atri, Asri & Ghorbanli 1995 nom. inval. (art. 2b, 3o, 5) (Asri et al., 1995, tableau hors texte : relevés n° 36 à n° 38 ; Atri et al., 1995, tableau 2 : relevés 38 à 54).
I-B. Juncetum heldreichiani (Asri et al., 1995, tableau hors texte : relevés n° 24 à n° 18 ; pas d’auteur indiqué).
I-C. Puccinellietum distantis nom. illeg. (art. 22) (Asri et al., 1995, tableau hors texte : relevés n° 47 à n° 46) ; à renommer.
I-D. Puccinellio bulbosae-Aeluropodetum littoralis Atri, Asri & Ghorbanli 1995 nom. inval. (art. 3o, 5) (Atri et al., 1995, tableau 2 : relevés 55 à 61).
Ils présentent des liens avec le Limonio gmelinii-Juncion maritimi, mais la flore y est globalement assez différente, avec des taxons vicariants de ceux connus ici (dont Puccinellia bulbosa), d’autres en commun avec le Puccinellion festuciformis (cf. supra, alliance Pf), dont Halimione verrucifera (Asri et al., 1995 ; Atri et al., 1995). De manière invalide (art. 2b, 3o, 5), Atri et al. (1995) rangent le premier et le dernier de ces quatre syntaxons respectivement dans leurs Halimionion verruciferae et Puccinellion bulbosae. Ces unités, qui restent à confirmer et valider plus strictement, pourraient se ranger à la limite dans les Juncetea maritimi et les Juncetalia maritimi par Aeluropus littoralis et de rares autres taxons.
Plusieurs auteurs d’Europe centrale considèrent encore bien d’autres associations au sein de cet ordre des Festuco-Puccinellietalia, mais plusieurs d’entre elles possèdent une forte composante thérophytique, dont les Matricario-Plantaginetum tenuiflorae (Soó 1933) Borhidi 1996, Hordeo-Trifolietum parviflori Micevski 1965, Puccinellio convolutae-Hordeetum hystricis Eliáš et al. 2013 prov., Hordeetum hystricis Wendelb. 1943, Artemisio-Petrosimonietum triandrae Soó 1927, Camphorosmetum annuae Rapaics ex Soó 1933, Petrosimonio brachyatae-Puccinellietum convolutae Tzonev et al. 2008. Leur interprétation devrait être revue.
Ordre 5. Tripidietalia ravennae Biondi, Blasi & Casavecchia in Biondi, Allegrezza, Casavecchia, Galdenzi, Gasparri, Pesaresi, Vagge & Blasi 2014 (Pl. Biosyst. 148 (2) : 327, sub Saccharetalia ravennae) ; tableau 1 : colonne ITr
Typus ordinis : Imperato cylindricae-Tripidion ravennae Braun-Blanq. & O. Bolòs 1957 (Anales Est. Exp. Aula Dei 5 (1-4) : 199).
Alliance ITr. Imperato cylindricae-Tripidion ravennae Braun-Blanq. & O. Bolòs 1957 (Anales Est. Exp. Aula Dei 5 (1-4) : 199, sub Imperato cylindricae-Erianthion ravennae) ; tableau 1 : colonne ITr ; tableau 17
[syn. : Holoschoenion romani Molin. & Tallon 1965 (La Terre et la Vie 19 : 54) nom. illeg. (art. 22).]
Hautes prairies oligohalophiles méditerranéennes à Imperata cylindrica (photo 15) et Tripidium ravennae (photo 16), plus Scirpoides holoschoenus subsp. australis, Dittrichia viscosa subsp. v. dont c’est certainement l’une des stations primaires ; des taxons halophiles à oligohalophiles sont fréquemment présents : Plantago crassifolia, Juncus acutus. Elles ont un peu l’aspect de roselières et d’ailleurs des Typha et Phragmites australis peuvent s’y rencontrer. Elles ont été classiquement placées parmi les végétations nanophanérophytiques des Nerio oleandri-Tamaricetea africanae.
Typus allianciae : Equiseto ramosissimi-Tripidietum ravennae Braun-Blanq. & O. Bolòs 1957 (Anales Est. Exp. Aula Dei 5 (1-4) : 200).
ITr1. Equiseto ramosissimi-Tripidietum ravennae Braun-Blanq. & O. Bolòs 1957 (Braun-Blanquet & de Bolòs, 1957, tableau 41, sub Equiseto ramosissimi-Erianthetum ravennae).
ITr2. Imperato cylindricae-Tripidietum ravennae Molin. & Tallon 1965 (Molinier & Tallon, 1965 : 56, sub Imperato cylindricae-Erianthetum ravennae).
ITr3. Gr. à Imperata cylindrica-Scirpoides holoschoenus subsp. australis (Noble & Baret, 2021, tableau 6 : colonne 10).
ITr4. Tripidio ravennae-Schoenetum nigricantis Géhu in Géhu, Costa, Scoppola, Biondi, Marchiori, Peris, Géhu-Franck, Caniglia & Veri 1984 (Géhu, Costa et al., 1984a, tableau 9, sub Eriantho ravennae-Schoenetum nigricantis) ; cité aussi par Géhu, Biondi et al. (1992, tableau 8), Biondi (1992a, tableau 5), Géhu, Uslu et al. (1992, tableau15).
ITr5. Tripidio ravennae-Scirpoidetum australis O. Bolòs 1962 (de Bolòs, 1962, tableau 52, sub Eriantho ravennae-Holoschoenetum australis).
ITr6. Imperato cylindricae-Juncetum littoralis Brullo & Furnari 1976 (Brullo & Furnari, 1976 : 31, sub Imperato cylindricae-Juncetum tommasinii).
ITr7. Scirpoidetum globiferi Pirola 1959 (Brullo & Furnari, 1976 : 30, sub Holoschoenetum globiferi).
ITr8. Carici distantis-Schoenetum nigricantis Géhu, Biondi, Géhu-Franck & Arnold 1986 prov. (Géhu et al., 1986, tableau 6).
ITr9. Calamagrostio epigeji-Tripidietum ravennae Taffetani & Biondi 1992 (Taffetani & Biondi, 1992, tableau 4, sub Calamagrostio epigeji-Erianthetum ravennae).
ITr10. Tripidio ravennae-Desmostachyetum bipinnatae (Quézel 1965) B. Foucault 2020 (de Foucault, 2020 : 66).
On n’a pas retenu ici le Panico repentis-Imperatetum cylindricae M.B. Crespo 1989 dont les liens avec l’alliance se réduisent à la présence d’Imperata cylindrica.
Ordre 6. Elytrigietalia acutae Géhu 1968 (Bull. Soc. Bot. N. Fance XXL (2) : 76, sub Agropyretalia pungentis)
Typus ordinis : Elytrigion acutae Géhu 1968 (Bull. Soc. Bot. N. Fance XXL (2) : 76, sub Agropyrion pungentis) nom. illeg. (art. 22).
Végétation halonitrophile des bordures estuariennes à Elytrigia acuta, Suaeda vera subsp. v., Beta vulgaris subsp. maritima.
Alliance EPm. Elytrigio acutae-Plantaginion maritimae Horvatić 1934 (Prirod. Istraž. Kral. Jugosl. 19 : 281, sub Agropyro-Plantaginion maritimae) ; tableau 1 : colonne EPm ; tableau 18
[syn. : Elytrigion acutae Géhu 1968 (Bull. Soc Bot. N. Fance XXL (2) : 76, sub Agropyrion pungentis) nom. illeg. (art. 22)]
Alliance unique.
EPm1. Beto maritimae-Elytrigietum acutae (Arènes 1933) Corill. 1953 ; a – d’après Géhu (1976, tableau 27) ; b – d’après Beeftink (1965, tableau 14 : colonnes 1 et 2, sub Atriplici-Elytrigietum acutae Beeftink & V. Westh. 1962).
EPm2. Elytrigio acutae-Althaeetum officinalis Géhu & Géhu-Franck 1976 (Géhu & Géhu-Franck, 1976 : 310).
EPm3. Braun-Blanquet et al. (1952, Les groupements végétaux de la France méditerranéenne : 121) valident le Trifolion maritimi Braun-Blanq. 1931 nom. nud. en publiant leur Elytrigio acutae-Trifolietum squamosi (sub Agropyro-Trifolietum maritimi). À côté d’une imposante composante thérophytique (Bromus hordeaceus s. l., Trigonella indica, Podospermum laciniatum, Vicia lutea, Ervum tetraspermum, Sonchus asper, Medicago scutellata, Hordeum marinum, Polypogon maritimus, Sagina maritima, des Parapholis, dont des taxons caractérisant les Saginetea maritimae), la composante vivace est synthétisée en EPm3. En commun avec les prairies subhalophiles de l’Alopecurion rendlei Zeidler 1954, alliance placée dans les Agrostietea stoloniferae (de Foucault & Catteau, 2012), on relève Trifolium squamosum V, Alopecurus bulbosus III, Hordeum secalinum II, Carex divisa II, alors qu’il manque de très nombreux taxons prairiaux caractérisant les Agrostietea stoloniferae. On ne peut donc pas suivre Mucina et al. (2016) puis des auteurs ultérieurs pour préférer le Trifolion squamosi à l’Alopecurion rendlei dans les Agrostietea stoloniferae.
EPm4. Elytrigio acutae-Suaedetum verae Géhu 1975 ex 1976 (Géhu, 1976, tableau 15, sub Agropyro littoralis-Suaedetum verae).
EPm5. Groupement à Elytrigia acuta-Juncus maritimus (Noble & Baret, 2021, tableau 6 : colonne 2).
EPm6. « Monermo cylindricae-Agropyretum littoralis Horvatić 1934 » (Horvatić, 1934, tableau XIX) ; cette association biologiquement complexe peut être subdivisée en une composante vivace, le Podospermo cani-Elytrigietum acutae (Horvatić 1934) ass. nov. hoc loco, typus nominis hoc loco : composante vivace du relevé 14 du tableau XIX in Horvatić (1934, Prirod. Istraž. Kral. Jugosl. 19 hors texte)
Livadno područje, 10 taxons
- combinaison caractéristique : Elytrigia acuta1, Podospermum canum +.2, Plantago maritima *m. 1-2.3, Centaurea jacea *pagensis +.1,
- autres taxons : Cynodon dactylon2, Cichorium intybus +.1, Agrostis stolonifera 1-2.2, Phleum nodosum +.1, Lotus glaber +.1, Trifolium pratense +.1
et une composante thérophytique, l’Hainardio cylindricae-Centaurietum tenuiflori (Horvatić 1934) ass. nov. hoc loco, typus nominis hoc loco : composante thérophytique du relevé 14 du tableau XIX in Horvatić (1934, Prirod. Istraž. Kral. Jugosl. 19 hors texte)
Livadno područje, 6 taxons
- combinaison caractéristique : Hainardia cylindrica2-3, Centaurium tenuiflorum 1-2.1, Schenkia spicata +.1, Ranunculus sardous +.1,
- autres taxons : Helminthotheca echioides +.1, Lolium rigidum 1-2.1,
association à rapprocher du Centaurio pulchelli-Blackstonion perfoliatae dans la classe des Juncetea bufonii.
Le Sarcocornio fruticosae-Suaedetum verae Géhu 1976 (Géhu, 1976, tableau 15bis, sub Arthrocnemo-Suaedetum verae) comporte un ‘Agropyron sp.’, on ne peut donc affirmer que ce syntaxon relève de la présente alliance. L’Elytrigio acutae-Limbardetum crithmoidis Géhu 1979 (sub Agropyro pungentis-Inuletum crithmoidis) a été publié dans un document ministériel difficile à consulter.
Enfin le tableau 19 synthétise quatre syntaxons de prés halophiles substeppiques décrits de l’Égypte et du Sud tunisien à Juncus rigidus, Aeluropus lagopoides, Limonium menigense, Tetraena alba dont les liens avec les Juncetea maritimi sont pratiquement réduits à Plantago crassifolia et Limonium virgatum ; ils seront à comparer avec d’autres associations affines (voir Zahran et al., 2016, qui ne décrivent toutefois pas d’associations). Quoi qu’il en soit, on peut les rapprocher dans une alliance originale non définie par les auteurs de ces associations, qui les rattachent souvent au Plantaginion crassifoliae, l’Aeluropodo lagopoidis-Juncion rigidi all. nov. hoc loco, typus nominis hoc loco : Aeluropodo lagopoidis-Juncetum rigidi (Vanden Berghen 1979) Géhu & Géhu-Franck 1992 (Colloq. Phytosoc. XIX : 691). Ce sont :
AJr1. Phragmito australis-Juncetum rigidi (Danin 1983) Géhu, Arnold, Géhu-Franck & Apostolidès 1992 (Géhu, Arnold et al., 1992, tableau 24, sub Phragmito australis-Juncetum arabici).
AJr2. Aeluropodetum lagopoidis (Vanden Berghen 1979) Géhu & Géhu-Franck 1992 (Géhu & Géhu-Franck, 1992b, tableau 20, sub Aeluropetum lagopoidis).
AJr3. Aeluropodo lagopoidis-Juncetum rigidi (Vanden Berghen 1979) Géhu & Géhu-Franck 1992 (Ibid., tableau 21, sub Aeluropo lagopoidis-Juncetum arabici).
AJr4. Aeluropodo lagopoidis-Schoenetum nigricantis (Vanden Berghen 1979) Géhu & Géhu-Franck 1992 (Ibid., tableau 22, sub Aeluropo lagopoidis- Schoenetum nigricantis).
3. La végétation à Cressa cretica
Dans cette synthèse, l’halophyte vivace Cressa cretica (photo 17) apparaît très rarement. Ce taxon est d’ailleurs souvent considéré comme caractérisant la végétation thérophytique des Frankenietalia pulverulentae.
Son comportement paraît effectivement bien être celui d’un taxon résistant peu à la concurrence et à l’ombrage des autres taxons, préférant des perturbations d’origine biotique ouvrant le tapis végétal (Lorenzoni & Paradis, 1994 ; Paradis & Lorenzoni, 1999 ; Tison & de Foucault, 2014 ; photo 18) ; c’est largement aussi le comportement des thérophytes, ce qui explique son association fréquente avec ceux-ci. Pourtant, son statut biologique de vivace est un peu en contradiction avec cette position. Pour mieux comprendre la sociologie de cette Convolvulacée, le tableau 20 synthétise les données suivantes :
Cc1. Cresso creticae-Hordeetum marini Géhu, Uslu & M.J. Costa 1992 (Géhu, Uslu & Costa, 1992, tableau 22), de Turquie.
Cc2. Cresso creticae-Crypsietum aculeatae Géhu, M.J. Costa & Uslu 1990 (Géhu, Costa & Uslu, 1990, tableau 26) de Chypre.
Cc3. Cresso creticae-Eleocharitetum palustris Géhu, M.J. Costa & Uslu 1990 (Géhu, Costa & Uslu, 1990, tableau 27) de Chypre.
Cc4. Cressetum creticae Brullo & Furnari 1970 sicilien (Brullo & Furnari, 1976, tableau p. 11).
Cc5. Cressetum creticae Martinez Parras 1984 andalou (non Brullo & Furnari 1976 ; Martinez Parras, 1984, tableau 7).
Cc6. Cressetum creticae algérien (non Brullo & Furnari 1970 ; Géhu, Kaabèche & Gharzouli, 1994, tableau 7 : relevés 10 à 19).
Cc7. Groupement adriatique à Cressa cretica (Jasprica et al., 2015, tableau 1 : relevés 11 à 14 et 18 à 21).
Cc8. Groupement corse à Limonium narbonense-Cressa cretica (Paradis & Lorenzoni, 1999, tableau 1, syntaxons A, D à G, I).
Cc9. Autre groupement corse à Cressa cretica (Paradis & Lorenzoni, 1999, tableau 1, syntaxons B, C, H).
Cc10. Cressetum creticae Brullo & Furnari 1970 ibérique (Sivim, extrait le 17/04/2021).
Cc11. Autre Cressetum creticae Brullo & Furnari 1970 ibérique (Sivim, extrait le 17/04/2021, sub Cressetum villosae Rothm. 1943).
Cc12. Cressetum villosae Rothm. 1943 (Reyes-Betancort et al., 2009, tableau 1 : relevés 13 à 16).
Laissant de côté les syntaxons Cc5, Cc6, Cc9 à Cc11 peu caractérisés et dont les descriptions sont à approfondir, on voit que les autres sont assez diversifiés. Cc1, Cc2 et Cc3, est-méditerranéens, se différencient par Aeluropus littoralis : Aeluropodo littoralis-Cressetum creticae ass. nov. hoc loco, typus nominis hoc loco : composante vivace du relevé 3 du tableau 22 in Géhu, Uslu & Costa (1992, Colloq. Phytosoc. XIX : 619)
Demre (Turquie), 10 m², 2 taxons
Cressa cretica 11, Aeluropus littoralis +,
avec une sous-association à Eleocharis palustris en Cc3 ; cette association pourrait cependant être présente aussi en Catalogne (Blanché & Ladero, 1986, tableau 4). Cc4 est le plus ancien décrit, sous le nom de Cressetum creticae Brullo & Furnari 1970, se différenciant des autres par Aeluropus lagopoides subsp. repens et Sarcocornia alpini ; lui seul doit donc garder le nom de Cressetum creticae. Le syntaxon adriatique Cc7 est bien caractérisé et statistiquement bien défini : Puccinellio festuciformis-Cressetum creticae (Jasprica, Milović & Romić 2015) nom. nov. hoc loco, typus nominis hoc loco : composante vivace du relevé 11 du tableau 1 in Jasprica et al. (2015, Hacquetia 14 (2) : 275)
Blato, littoral est-adriatique (Croatie), 25 m², 6 taxons
- combinaison caractéristique : Cressa cretica 1, Juncus maritimus 4, Puccinellia festuciformis +, Limonium narbonense +, Elytrigia elongata +,
- autre taxon : Sarcocornia fruticosa 2 ;
ce syntaxon est plus ou moins confirmé par Milović & Marković (2003, tableau 1, surtout relevé 3). Le syntaxon corse Cc8 est proche du précédent, mais plus pauvre en taxons : Triglochino barrelieri-Cressetum creticae ass. nov. hoc loco, typus nominis hoc loco : composante vivace du relevé 14 du tableau 1 in Paradis & Lorenzoni (1999, J. Bot. Soc. Bot. France 9 : 32)
San Giovanni, baie de Figari (Corse-du-Sud), 4 m², 5 taxons
- combinaison caractéristique : Cressa cretica 2b, Triglochin barrelieri 2a, Limonium narbonense 2a,
- autres taxons : Bolboschoenus maritimus 2a, Sarcocornia fruticosa
L’association languedocienne (photo 18) reste à préciser. Enfin, le syntaxon Cc12 est nommé d’après Cressa cretica var. villosa, qui n’est plus reconnu actuellement ; c’est donc un Cressetum creticae des Canaries à renommer, avec Frankenia boissieri : Frankenio boissieri-Cressetum creticae (Rothm. 1943) nom. nov. hoc loco, typus nominis hoc loco : composante vivace du relevé 13 du tableau 1 in Reyes-Betancort et al. (2009, Lazaroa 30 : 67).
Juncalillo del Sur, Gran Canaria (Espagne), 1 m², 2 taxons
Cressa cretica 3, Frankenia boissieri +.
Où placer toutes ces associations méditerranéennes ? Le lien avec les Sarcocornietea fruticosae est trop mince pour envisager un tel rattachement. On retient donc leur intégration aux Juncetea maritimi et aux Juncetalia maritimi ; au niveau alliance, les caractères écologiques particuliers de C. cretica, notamment son comportement pionnier et sa faible résistance à la concurrence, associés à la faible représentation des taxons caractéristiques de classe et d’ordre, justifient l’identification d’une alliance particulière au sein des Juncetalia maritimi, le Cression creticae all. nov. hoc loco, caractérisée surtout par Cressa cretica, avec un lien spatial (mosaïque) privilégié avec les Saginetea maritimae, typus nominis hoc loco : Puccinellio festuciformis-Cressetum creticae (Jasprica, Milović & Romić 2015) B. Foucault.
3. Quelques aspects de la structure systématique associée aux Juncetea maritimi
Pour la végétation basse halophile, dans un essai antérieur (de Foucault, 1987), on avait reconnu des structures systématiques originales, c’est-à-dire des catégories phytosociologiques caractérisées par une combinaison originale de familles, la S(Chenopodiaceae) et la S(Plumbaginaceae-Poaceae), celle-ci plus riche en taxons que celle-là. On propose de reprendre ici cet essai en suivant la délimitation et la nomenclature des familles selon APG IV (Angiosperm Phylogeny Group, 2016) et en s’appuyant sur le tableau synthétique 1 (à l’exception des colonnes LHs et HTp assez marginales). On a donc « lissé » dans ce tableau les genres et espèces au niveau familial pour obtenir le tableau 21.
La catégorie optimale est formée par l’ensemble des colonnes Sa à Cc, caractérisé par la combinaison des Asteraceae, Fabaceae, Frankeniaceae, Apiaceae, Plumbaginaceae et Amaranthaceae, alors que d’autres familles surtout herbacées sont bien représentées : Poaceae, Juncaceae, Plantaginaceae, Cyperaceae, Caryophyllaceae. On confirme ainsi la S(Plumbaginaceae-Poaceae) reconnue en 1987. Les quatre premières colonnes (Pph à SPd), correspondant aux Puccinellietalia phryganodis, apparaissent comme bien appauvries par rapport à l’ensemble optimal, avec cependant l’arrivée des Rosaceae (représentées par Argentina anserina subsp. egedei). Les Juncaginaceae (par Triglochin maritima) relient ces deux ensembles.
À l’extrême droite, la colonne AJr se sépare du reste par l’apparition des Zygophyllaceae et la disparition de plusieurs des familles citées à propos des ensembles précédents, amorce probable d’une structure systématique originale à définir dans l’avenir [S(Zygophyllaceae-Juncaceae) prov.].
Le tableau 22 permet de comparer les F-structures reconnues lors de ces deux synthèses de classes de végétation halophiles, Juncetea maritimi et Sarcocornietea fruticosae.
4. Conclusion
Sur la base d’une assez large synthèse, quoique pas parfaite pour des raisons de disponibiité de la ressource bibliographique (de Foucault, 2021b), on est parvenu au schéma synsystémique suivant, avec sept ordres et vingt-quatre alliances (les syntaxons en grisé sont présents en France) :
JUNCETEA MARITIMI Tüxen & Oberd. 1958
Puccinellietalia phryganodis Hadač 1946
Puccinellion phryganodis Hadač 1946 (tableau 2)
Caricion glareosae Nordh. 1954 (tableau 3)
Puccinellion pumilae A. Miyaw. & Ohba 1965 (tableau 4)
Dupontion fischeri Hadač 1946 (tableau 4)
Limonio caroliniani-Puccinellion phryganodis B. Foucault (tableau 4)
Spartinetalia alterniflorae Conard 1935
Spartinion alterniflorae Conard 1935 (tableau 5)
Lysimachio maritimae-Puccinellietalia maritimae Beeftink & V. Westh. in Beeftink 1962
Puccinellion maritimae W.F. Christ. 1927 (tableau 6)
Puccinellio maritimae-Spergularion marinae Beeftink 1965 (tableau 7)
Armerion maritimae Braun-Blanq. & De Leeuw 1936 (tableau 8)
Eu-Armerienion maritimae
Frankenio laevis-Armerienion maritimae Géhu & Géhu-Franck in Géhu 1976
Lysimachio maritimae-Juncion maritimi Géhu & Géhu-Franck ex Géhu in Bardat et al. 2004 (tableau 9)
Spergulario mediae-Plantaginion maritimae B. Foucault (tableau 10)
Juncetalia maritimi Braun-Blanq. ex Horvatić 1934
Juncion maritimi Braun-Blanq. ex Horvatić 1934 (tableau 11)
Puccinellion caespitosae Rivas Mart. in Rivas Mart. & M.J. Costa 1976 (tableau 12)
Puccinellion festuciformis Micevski 1965 (tableau 13)
Plantaginion crassifoliae Braun-Blanq. ex Braun-Blanq., Roussine & Nègre 1952 (tableau 14)
Eu-Plantaginion crassifoliae
Limonio virgati-Plantaginenion crassifoliae Mercadal 2020
Schizogyno sericeae-Juncion acuti B. Foucault (tableau 1)
Cression creticae B. Foucault (tableau 20)
Festuco-Puccinellietalia Soó 1968
Puccinellion distantis (Soó 1933) Wendelb. 1943 (tableau 15)
Puccinellion intermediae Wendelb. 1943 (tableau 15)
Festucion pseudovinae Soó in Máthé 1933 (tableau 15)
Limonio gmelinii-Juncion maritimi Golub & Solomacha ex Dubyna & Neuhäuslová 2000 (tableau 16)
Tripidietalia ravennae Biondi, Blasi & Casavecchia in Biondi et al. 2014
Imperato cylindricae-Tripidion ravennae Braun-Blanq. & O. Bolòs 1958 (tableau 17)
Elytrigietalia acutae Géhu 1968
Elytrigio acutae-Plantaginion maritimae Horvatić 1934 (tableau 18)
À plusieurs reprises, tant dans les Juncetea maritimi que dans les Sarcocornietea fruticosae, on a mis en évidence la présence de pelouses thérophytiques associées ; ce sont pour la première classe les Pholiuro pannonici-Bupleuretum tenuissimi, l’Hordeo geniculati-Polygonetum pulchelli, assez proches l’une de l’autre, et l’Hainardio cylindricae-Centaurietum tenuiflori, pour la seconde (de Foucault, 2021b) les Frankenio pulverulentae-Psylliostachyetum leptostachyae et Frankenietum florido-pulverulentae, certaines pouvant se placer dans les Saginetea maritimae et les Frankenietalia pulverulentae, l’Hainardio cylindricae-Centaurietum tenuiflori étant plutôt à ranger dans les Juncetea bufonii et le Centaurio pulchelli-Blackstonion perfoliatae. Plus particulièrement, dans la quatrième association, on peut insister sur la présence du genre annuel Psylliostachys, le type biologique thérophyte étant assez peu fréquent chez les Plumbaginaceae (Kubitzki, 1993) : on connaît quelques Limonium, dont L. echioides, taxon apparaissant dans certaines associations du Sileno sedoidis-Catapodion marini (de Foucault & Bioret, 2010, sub Sileno sedoidis-Catapodion loliacei) au sein des Saginetalia maritimae et des Saginetea maritimae, apparaissant donc comme homologue des Psylliostachys. Akhani et Ghorbanli (1993) citent deux autres Psylliostachys, P. spicata et P. beludshistanica, en association avec Frankenia pulverulenta, diverses Amaranthaceae annuelles (Bienertia cycloptera, genres Atriplex, Bassia, Climacoptera, Halanthium, Halocharis, Halimocnemis, Suaeda…), Hordeum marinum, Polypogon maritimum.
On espère que cet essai stimulera de nouvelles recherches pour en combler les lacunes, mais aussi pour développer la connaissance des steppes salées du centre et du sud-est de l’Europe, voire aussi d’Afrique du Nord, où la végétation halophile hémicryptophyto-géophytique reste encore assez mal connue, au contraire de la végétation halophile chaméphytique à nanophanérophytique des Sarcocornietea fruticosae.
Bibliographie
Akhani H. & Ghorbanli M., 1993. A contribution to the halophytic vegetation and flora of Iran. In H. Lieth & A. Al Masoom (eds), Towards the rational use of high salinity tolerant plants, Kluwer Academic Publishers, I : 35-44.
Angiosperm Phylogeny Group, 2016. An update of the Angiosperm Phylogeny Group classification for the orders and families of flowering plants: APG IV. Botanical Journal of the Linnean Society 181 : 1-20.
Annezo N., Bioret F. & Géhu J.-M., 1991. Précisions synécologiques et phytosociologiques sur les végétations à Limonium humile Mill. du littoral breton. Documents phytosociologiques, NS, XIII : 1-14.
Asri Y., Hamzek B. & Ghorbanli M., 1995. Étude phytosociologique de la végétation halophile de l’est du lac Oroumieh (nord-ouest de l’Iran). Documents phytosociologiques, NS, XV : 299-308.
Atri M., Asri Y. & Ghorbanli M., 1995. Étude préliminaire de la végétation halophile du littoral ouest du lac Oroumieh, Iran. Documents phytosociologiques, NS, XV : 205-210.
Babalonas D. & Papastergiadou E., 1990. Ein halophiles Gesellschaftsrelikt im griechischen Binnenland. Tuexenia 10 : 115-121.
Bacchetta G., Casti M. & Zavattero L., 2007. Analisi della vegetazione del distretto minerario di Montevecchio (Sardegna sud-occidentale). Fitosociologia 44 (2) : 83-108.
Barbour M.G & Billings W.D., 1988. North America terrestrial vegetation. Cambridge University Press, 434 p.
Bardat J., Bioret F., Botineau M., Boullet V., Delpech R., Géhu J.-M., Haury J., Lacoste A., Rameau J.-C., Royer J.-M., Roux G. & Touffet J., 2004. Prodrome des végétations de France. Patrimoines naturels (publications scientifiques du Muséum) 61 : 1-171.
Barrera I. & Cirujano S., 1986. Artemisio-Puccinellietum pungentis una nueva asociación de la clase Juncetea maritimi. Trabajos del Departamento de Botánica 13 :111-113.
Bartolo G., Brullo S., De Marco G., Dinelli A., Signorello P. & Spampinato G., 1992. Studio fitosociologico sulla vegetazione psammofila della Sardegna meridionale. Colloques phytosociologiques XIX, Végétation et qualité de l’enironnement côtier en Méditerranée : 251-273.
Beeftink W.G., 1962. Conspectus of the phanerogamic salt plant communities in the Netherlands. Biologisch Jaarboek 30 : 325-362.
Beeftink W.G., 1965. De zoutvegetatie van ZW-Nederland beschouwd in Europees Verband. Wageningen, 167 p.
Beeftink W.G. & Géhu J.-M., 1973. Spartinetea maritimae. Prodrome des groupements végétaux d’Europe 1 : 1-42.
Bertacchi A., Lombardi T., Saggese A. & Lazzeri V., 2021. The vegetation of a relict salt marsh area in the Pisan coast in the context of brackish wetlands of Tuscany. Plant Sociology 58 (1) : 41-43.
Biondi E., 1992a. The vegetation of sedimentary low coast in Corfu island. Colloques phytosociologiques XIX, Végétation et qualité de l’enironnement côtier en Méditerranée : 401-427.
Biondi E., 1992b. Studio fitosociologico dell’archipelago de la Maddalena, I – La vegetazione costiera. Colloques phytosociologiques XIX, Végétation et qualité de l’enironnement côtier en Méditerranée : 183-223.
Biondi E., Allegrezza M., Casavecchia S., Galdenzi D., Gasparri R., Pesaresi S., Vagge I. & Blasi C., 2014. New and validated syntaxa for the checklist of Italian vegetation. Plant Biosystems 148 (2) : 318-332.
Bioret F. & Lahondère Ch., 2010. Les végétations à Frankenia laevis et à Limonium à nervures parallèles des hauts schorres sablonneux et des falaises du littoral atlantique français. Braun-Blanquetia 46 : 129-137.
Birse E.L., 1980. Plant communities of Scotland; a preliminary phytocoenonia. Soil Survey of Scotland 4 : 1-235.
Blanché C. & Molero J., 1986. Las cubetas arreicas al sur de Bujaraloz (Valle del Ebro). Contribución a su estudio fitocenológico. Lazaroa 9 : 277-299.
Bolòs O. (de), 1962. El paisaje vegetal barcelonés. Fac. Filosofía Letras, Cátedra Ciudad de Barcelona, 192 p.
Bosseaux M., 1965. Végétation et flore des îles Saint-Pierre-et-Miquelon. Journal d’agriculture tropicale et de botanique appliquée 12 : 58-79, 194-210, 319-337, 545-495.
Bouabdallah E., 1992. La végétation steppique sur sols salés des hautes plaines sud-algéroises ; composition, structure et production. Thèse de doctorat d’État, Paris-Sud-Orsay, 206 p.
Bournérias M., 1976. La série de végétation des vases d’estran dans l’estuaire de la « rivière » Puvirnituq (Nouveau-Québec, Canada). Colloques phytosociologiques IV, La végétation des vases salées : 157-169.
Braun-Blanquet J., 1931. Aperçu des groupements végétaux du Bas-Languedoc. Communications de la Station internationale de géobotanique méditerranéenne et alpine 9 : 35-40.
Braun-Blanquet J. & De Leeuw W.C., 1936. Vegetationsskizze von Ameland. Nederlandsch kruidkundig archief 46 : 359-393.
Braun-Blanquet J., Roussine N. & Nègre R., 1952. Les groupements végétaux de la France méditerranéenne. CNRS, Paris, 297 p.
Braun-Blanquet J. & Tüxen R., 1952. Irische Pflanzengesellschaften. Veröffentlichungen des geobotanischen Institutes der E.T.H., Stiftung Rübel, in Zürich 25 : 224-421.
Braun-Blanquet J. & de Bolòs O. 1957. Les groupements végétaux du bassin moyen de l’Ebre et leur dynamisme. Anales Estación Experimental Aula Dei 5 (1-4): 1-266.
Brullo S. & Furnari F., 1976. Le associazioni vegetali degli ambienti palustri costieri della Sicilia. Notiziario delle Società Italiana di Fitosociologia 11 : 1-43.
Bueno Sánchez A., 1997. Flora y vegetación de los estuarios asturianos. Cuadernos de Medio Ambiente, Naturaleza 3 : 1-334.
Castroviejo S., 1975. La vegetación halophila costera del suroccidente Gallego. Documents phytosociologiques 9-14 : 51-62.
Catteau E. et onze co-auteurs, 2021. Végétation du nord de la France, guide de détermination. Biotope, Mèze, 400 p.
Celinski F. & Wika S., 1976. État des recherches sur la végétation halophile en Pologne. Colloques phytosociologiques IV, La végétation des vases salées : 141-151.
Choisnet G., Roux C., Cordonnier S., Hugonnot V. & Bioret F., 2020. La végétation des sources thermominérales salées d’Auvergne. BIOM (Revue scientifique pour la biodiversité du Massif central) 1 : 69-96.
Christiansen W.F., 1927. Die Außendeichsvegetation von Schleswig-Holstein mit besonderer Berücksichtigung von Föhr. Föhrer Heimatbücher 16 : 3-29.
Cirujano S., 1981. Las lagunas manchegas y su vegetación, II. Anales del Jardín Botánico de Madrid 38 (1) : 187-232.
Conard H., 1935. The plant associations of central Long Island. A study in descriptive plant sociology. The American Midland Naturalist 16 (4) : 433-516.
Corbetta F., Gratani L., Moriconi M. & Pirone G., 1992. Lineamenti vegetazionali e caratterizzazione ecologica delle spiagge dell’arco jonico da Taranto alla foce del Sini. Colloques phytosociologiques XIX, Végétation et qualité de l’environnement côtier en Méditerranée : 461-521.
Costa J.C., Lousã M. & Espírito-Santo M.D., 1997. A vegetação do Parque Natural da Ria Formosa (Algarve, Portugal). Studia Botanica 15 : 69-157.
Czirjak R., 2010. Contribution to the familiarization with the meadows of Ierului field. Analele Universitătii din Oradea Fascicula: Ecotoxicologie, Zootehnie şi Tehnologii de Industrie Alimentară : 394-401.
Dajić Stevanović Z., Aćić S., Luković M., Zlatković I., Vasin J., Topisirović G. & Šilc U., 2016. Classification of continental halophytic grassland vegetation of Southeastern Europe. Phytocoenologia 46 (3) : 317-331.
Dangien B., Hayon J.-C. & Pelt J.-M., 1974. Analyse phytosociologique de la végétation halophile d’origine industrielle de la basse vallée de la Meurthe. Documents phytosociologiques 5 : 1-41.
Dítě D., Eliáš Jr P., Šuvada R., Petrášová A. & Melečková Z., 2010. Current distribution and stage of community Artemisio santonici-Festucetum pseudovinae in Slovakia. Thaiszia Journal of Botany 20 : 77-86.
Dítě D., Dítě Z., Hájková P. & Šuvada R., 2019. Vegetation and ecological characteristics of the northernmost salt marshes of the European continent. Nordic Journal of Botany 2019 e02334, doi: 10.1111/njb.02334.
Dubyna D.V. & Neuhäuslová Z., 2000. Salt meadows of the Birjucij Island Spit, Azov Sea. Classes Juncetea maritimi and Bolboschoenetea maritimi. Acta Botanica Croatica 59 (1) : 167-178.
Emberger L. & Régnier P.R., 1926. Aperçu sur la végétation de l’embouchure du Bou Regreg. Bulletin de la Société des sciences naturelles du Maroc 6 : 78-86.
Enggravslia L., Hansen J.P.H., Ramtvedt A.E. & Vevle O., 1985. Hastrandvegetasjon i vestfold. Plantesosiologi og verneverdiar belyst med synsosiologiske metodar. In S. Bretten & A. Moen, Fagmøte i vegetasjonsøkologi på Kongsvoll, Kgl. Norske Videnskabers Selskab. Museet, Rapp., Bot. ser, 2 : 50-61 (en suédois).
Esteve F., 1968. Datos para el estudio de las clases Ammophiletea, Juncetea y Salicornietea en las Canarias Orientales. Collectanea Botanica (Barcelona) 7 : 303-323.
Feekes W., 1943. De Piamer Kooiwaard en Makkumerwaard. Nederlandsch kruidkundig archief, serie 3, 53 (1) : 288-330.
Foucault B. (de), 1987. Nouvelles recherches sur les structures systématiques végétales : caractérisation, ordination, signification. Phytocoenologia 15 (2) : 159-199.
Filigheddu R.S., Farris E. & Biondi E., 2000. The vegetation of S’Ena Arrubia lagoon (centre-western Sardinia). Fitosociologia 37 (1) : 39-59.
Foucault B. (de), 2013. Les journées de l’Association tunisienne de physiologie et de biosurveillance de l’environnement (12-15 mai 2012) ; compte rendu phytosociologique des herborisations. Revue Écologie-Environnement (Tiaret, Algérie) 9, non paginé (http://fsnv.univ-tiaret.dz/revues.php).
Foucault B. (de), 2018. La sortie phytosociologique du 28 mai 2017 à la Fontaine salée et ses environs en forêt domaniale de l’Eau salée (commune de Sougraigne). Bulletin de la Société d’études scientifiques de l’Aude CXVII : 189-196.
Foucault B. (de), 2020. Éloge du paradigme synusial : alternative à la classification phytosociologique de la végétation forestière européenne, ouest-asiatique et nord-africaine. Evaxiana 7 : 5-248.
Foucault B. (de), 2021a. Contribution à la connaissance de la végétation des étangs asséchés et des canaux du Narbonnais. Carnets botaniques 38 : 1-15 + 3 tableaux ; https://doi.org/10.34971/387K-6576
Foucault B. (de), 2021b. Contribution à une synthèse des Sarcocornietea fruticosae. Carnets botaniques 59 : 1-19 + 17 tableaux, https://doi.org/10.34971/8h0c-0b94.
Foucault B. (de) & Bioret F., 2010. Contribution au prodrome des végétations de France : les Saginetea maritimae Westhoff et al. 1962. Journal de botanique de la Société botanique de France 50 : 59-83.
Foucault B. (de) & Catteau E., 2012. Contribution au prodrome des végétations de France : les Agrostietea stoloniferae Oberd. 1983. Journal de botanique de la Société botanique de France 59 : 5-131.
Franck J., Géhu, J.-M., & Dhennin, R., 1982. Un exemple remarquable de séquence végétale topodynamique prés salés – bas-marais – landes dans l’anse de Goulven (nord-Finistère, France). Documents phytosociologiques, NS, VII : 419-434.
Frileux P.-N. & Géhu J.-M., 1976. Fragments relictuels de végétation halophile en baie de Seine (marais du Hode). Colloques phytosociologiques IV, La végétation des vases salées : 277-292.
Géhu J.-M., 1968. Essai sur la position systématique des végétations vivaces halonitrophiles des côtes atlantiques françaises (Agropyretea pungentis cl. nov.). Bulletin de la Société botanique du nord de la Fance XXL (2) : 71-77.
Géhu J.-M., 1973.Premiers compléments chorologiques au fascicule n° 1, Spartinetea maritimae, du prodrome des groupements végétaux d’Europe. Documents phytosociologiques 4 : 47-49.
Géhu J.-M., 1973b. L’Eleocharetum parvulae Gillner 1960 de la New Forest, Hants-England. Documents phytosociologiques 4 : 44-46.
Géhu J.-M., 1976. Approche phytosociologique synthétique de la végétation des vases salées du littoral atlantique français (synsystématique et synchorologie). Colloques phytosociologiques IV, La végétation des vases salées : 395-462.
Géhu J.-M., 1979. Éude phytocoenotique analytique globale de l’ensemble des vases et prés salés et saumâtres de la façade atlantique française. Document ministère de l’Environnement et du Cadre de vie, Paris, 514 p.
Géhu J.-M., 1983. Les prés salés de l’autoroute. Annales de la Fondation M. Yourcenar : 68-70.
Géhu J.-M. & Caron B. & Bon M., 1976. Données sur la végétation des prés salés de la baie de Somme. Colloques phytosociologiques IV, La végétation des vases salées : 197-223.
Géhu J.-M. & Delzenne C., 1976. Apport à la connaissance phytosociologique des prairies salées de l’Angleterre. Colloques phytosociologiques IV, La végétation des vases salées : 227-233.
Géhu J.-M. & Géhu-Franck J., 1976. L’estuaire de Sables-d’Or, un site halophile nord-breton à préserver Colloques phytosociologiques IV, La végétation des vases salées : 295-312.
Géhu J.-M. & Géhu-Franck J., 1982. La végétation du littoral Nord – Pas-de-Calais. Centre régional de phytosociologie, Bailleul, 361 p.
Géhu J.-M., Costa M., Scoppola A., Biondi E., Marchiori S., Peris J.B., Franck J., Caniglia G. & Veri L., 1984a. Essai synsystématique et synchorologique sur les végétations littorales italiennes dans un but conservatoire. I – Dunes et vases salées. Documents phytosociologiques, NS, VIII : 393-474.
Géhu J.-M., Costa M., Biondi E., Peris J.B. & Arnold N., 1984b. Données sur la végétation maritime des côtes méridionales de l’île de Chypre (plages, dunes, lacs salés et falaises). Documents phytosociologiques, NS, VIII : 343-364.
Géhu J.-M. & Géhu-Franck J., 1984. Schéma synsystématique et synchorologique des végétations phanérogamiques halophiles françaises. Documents phytosociologiques, NS, VIII : 51-70.
Géhu J.-M., Scoppola A., Caniglia G., Marchiori S. & Géhu-Franck J., 1984. Les systèmes végétaux de la côte nord-adriatique italienne, leur originalité à l’échelle européenne. Documents phytosociologiques, NS, VIII : 485-558.
Géhu J.-M., Biondi E., Géhu-Franck J. & Arnold K., 1986. Données synsysématiques et synchorologiques sur la végétation du littoral sédimentaire de la Grèce continentale. Documents phytosociologiques, NS, X (II) : 43-92.
Géhu J.-M., Biondi E., Géhu-Franck J. & Taffetani F., 1987. Données sur la végétation maritime du littoral oriental de la Corse. Informes (Universidad de La Laguna) 22 : 363-391.
Géhu J.-M. & Biondi E., 1988. Données sur la végétation des ceintures d’atterrissement des lacs Alimini (Salento, Italie). Documents phytosociologiques, NS, XI : 353-380.
Géhu J.-M. & Uslu T., 1989. Données sur la végétation littorale de la Turquie du nord-ouest. Phytocoenologia 17 (4) : 449-505.
Géhu J.-M., Arnold K., Géhu-Franck J. & Apostolidès N., 1992. Apport à la connaissance phytosociologique du littoral de l’Égypte et du Sinaï. Colloques phytosociologiques XIX, Végétation et qualité de l’environnement côtier en Méditerranée : 623-676.
Géhu J.-M., Biondi E., Géhu-Franck J. & Costa M., 1992. Interprétation phytosociologique actualisée de quelques végétations psammophiles et halophiles de Camargue. Colloques phytosociologiques XIX, Végétation et qualité de l’environnement côtier en Méditerranée : 103-131.
Géhu J.-M. & Bioret F., 1992. Étude synécologique et phytocoenotique des communautés à Salicornes des vases salées du littoral breton. Bulletin de la Société botanique du Centre-Ouest, NS, 23 : 347-419.
Géhu J.-M. & Géhu-Franck J., 1992a. Considérations taxonomiques et syntaxonomiques sur les végétation halophiles de l’estuaire du fleuve Saint-Laurent (Québec, Canada) et des îles de la Madeleine. Colloques phytosociologiques XVIII, Phytosociologie littorale et taxonomie : 261-321.
Géhu J.-M. & Géhu-Franck J., 1992b. Données nouvelles sur la végétation littorale psammophile et halophile du Sud tunisien. Colloques phytosociologiques XIX, Végétation et qualité de l’environnement côtier en Méditerranée : 677-723.
Géhu J.-M., Uslu T. & Costa M., 1992. Apport à la connaissance phytosociologique du littoral sud de la Turquie méridionale. Colloques phytosociologiques XIX, Végétation et qualité de l’environnement côtier en Méditerranée : 591-622.
Géhu J.-M. & Biondi E., 1994. Végétation du littoral de la Corse. Essai de synthèse phytosociologique. Braun-Blanquetia 13: 1-149.
Géhu J.-M., Kaabèche M. & Gharzouli R., 1993. Une remarquable toposéquence phytocoenotique en bordure du chott El Hodna (Algérie). Fragmenta Floristica et Geobotanica, suppl. 2 (2) : 513-520.
Géhu J.-M., Roman N. & Boullet V., 1994. Observations sur la végétation des côtes de Roumanie au sud du delta du Danube. Fitosociologia 27 : 73-89.
Gillner W., 1960. Vegetations- und Standortsuntersuchungen in den Strandwiesen der schwedischen Westküste. Acta phytogeographica Suecica 43 : 1-198.
Glemarec E. & Wattez J.-R., 2019. Contribution à l’étude des écotones prés salés/landes des rias du sud Morbihan : approche phytosociologique et conservatoire. Documents phytosociologiques, 3e série, 12 : 406-416.
Golub V.B. & Solomakha V.A., 1988. The highest units of the classification of the salt soil vegetation in the European part of the USSR. Byulleten’ Moskovskogo Obshchestva Ispytatelei Prirody, Biologie, 93 (6) : 80-92 (en russe).
Grandtner M.M., 1984. Le marais salé d’Ogunquit, Maine, USA. Documents phytosociologiques, NS, VIII : 1-13.
Hadač E., 1946. The plant-communities of Sassen Quarter, Vestspitsbergen. Studia Botanica Čechica 7 : 127-164.
Hadač E., 1989. Notes on plant communities of Spitsbergen. Folia Geobotanica et Phytotaxonomica 24 (2) : 131-169.
Hofmann W., 1969. Das Puccinellietum phryganodis in Südost-Spizbergen. Mitteilungen der Floristisch-soziologischen Arbeisgemeinschaft 14 : 224-230.
Horvatić S., 1934. Flora i vegetacija otoka Paga. Prirodoslovna istraživanja kraljevine Jugoslavije 19 : 116-372.
Horvatić S., 1939. Pregled vegetacija otoka Raba sa gledišta biljne sociologije. Prirodoslovna istraživanja kraljevine Jugoslavije 22 : 1-96.
Izco J., Guitián J. & Sánchez J.M., 1993. La marisma superior cántabro-atlántica meridional: estudio de las comunidades de Juncus maritimus y de Elymus pycnanthus. Lazaroa 13 :149-169.
Izco J. & Sánchez J.M., 1997. Los medios halófilos de la ría de Ortigueira (A Coruña, España). Vegetación de dunas y marismas. Thalassas 12 : 63-100.
Jasprica N., Milović M. & Romić M., 2015. Phytosociology and ecology of Cressa cretica L. (Convolvulaceae) on the eastern Adriatic coast. Hacquetia 14 (2) : 265-276.
Jeckel G., 1977. Flora und Vegetation des NSG, « Salzfloragebiet bei Schreyahn » in NE-Niedersachsen. Mitteilungen der Floristisch-soziologischen Arbeisgemeinschaft 19-20 : 241-251.
Julve Ph., 1993. Synopsis phytosociologique de la France (communautés de plantes vasculaires). Lejeunia, NS, 140 : 1-160.
Knapp R., 1976. Mehrjährige supra-littorale Salzmarsch-Gesellschaften an Küsten on Nord-Amerika. Colloques phytosociologiques IV, La végétation des vases salées : 181-191.
Korotkov K.O., Morozova O.V. & Belonovskaja E.A., 1991. The USSR vegetation syntaxa prodromus. G.E. Vilchek, Moscow, 346 p.
Kubitzki K., 1993. Plumbaginacae. In K. Kubitzki, J.G. Rohwer & V. Bittrich (eds), The families and genera of ascular plants, II :523-530.
Ladero M., Navarro F., Valle C., Marcos B., Ruiz T. & Santos M.T., 1984. Vegetación de los saladares castellano-leoneses. Studia Botanica 3 : 17-62.
Lavrinenko O. & Lavrinenko I., 2018. Classification of salt and brackish marshes vegetation of the Bolschezemel’skaya tundra (Barents sea coastal). Phytodiversity of eastern Europe XII (3) : 82-143. (en russe)
Lepping O. & Daniëls F.J.A., 2006 (publié 2007). Phytosociology of beach and salt marsh vegetation in northern West Greenland. Polarforschung 76 : 95-108.
Martínez Parras J.M., 1984. La vegetación lacustre de la depresión de Antequera (Andalucía). Collectanea Botanica (Barcelona) 15 : 289-306.
Máthé I., 1933. A hortobágyi Ohat-erdö vegetációja. Botanikai Közlemények XXX : 163-184.
Matysiak J.-P., 1993. Au sujet de Puccinellia distans. Bulletin de la Société botanique du nord de la France 46 (1-2) : 33-40.
Menke B., 1969. Vegetationskundliche und vegetationsgeschichtliche Untersuchungen an Strandwällen. Mitteilungen der Floristisch-soziologischen Arbeisgemeinschaft 14 : 95-120.
Mercadal i Corominas G., 2019. Els prats de dall de la terra baixa catalana; caracterització geobotànica, valoració agroambiental i estudi de les relacions fitosociològiques entre els prats dalladors de l’Europa occidental; 3 – Vegetació i gestió pradenca. Thèse de doctorat, universitat de Girona, 756 p.
Mercadal i Corominas G., 2020. Caracterización geobotánica y validación fitosociológica de algunos sintaxones de prados salobres (all. Juncion maritimi y Plantaginion crassifoliae, class. Juncetea maritimi) de Cataluña y del Mediterráneo occidental. Acta Botanica Malacitana 45 : 103-115.
Micevski K., 1965. Halofitska vegetacija Ovčeg polja. Acta Musei Macedonici Scientiarum Naturalium, Skopje, 10 : 67-90.
Miyawaki A. & Ohba T., 1965. Studien über Strand-Salzwiesengesellschaften auf OstHokkaido (Japan). Science Reports of the Yokohama National University, sect. II, 12 : 1-25.
Miyawaki A. & Ohba T., 1969. Studien über Strand-Salzwiesengesellschaften auf Honshu, Shikoku and Kyushu (Japan). Science Reports of the Yokohama National University, sect. II, 15 : 1-23.
Molenaar J.G. (de), 1974. Vegetation of the Angmagssalik district Southeast Greenland. I – Litoral vegetation. Meddel. Grønland 187 (1) : 1-79.
Molinier R. & Tallon G., 1965. Phytogéographie de la Camargue. La Terre et la Vie 19 : 1-185.
Mucina L., Bültmann H., Dierßen K., Theurillat J.-P., Raus Th., Čarni A., Šumberová K., Willner W., Dengler J., Gavilán García R., Chytrý M., Hájek M., Di Pietro R., Iakushenko D., Pallas J., Daniëls F.J.A., Bergmeier E., Santos Guerra A., Ermakov N., Valachovič M., Schaminée J.H.J., Lysenko T., Didukh Y.P., Pignatti S., Rodwell J.S., Capelo J., Weber H.E., Solomeshch A., Dimopoulos P., Aguiar C., Hennekens S.M. & Tichý L., 2016. Vegetation of Europe: hierarchical floristic classification system of vascular plant, bryophyte, lichen, and algal communities. Applied Vegetation Science 19 (1) : 3-264.
Muller S. & Etcheberry R., 2006. Esquisse de typologie des habitats naturels de flore de l’archipel de Saint-Pierre-et-Miquelon. In S. Muller, Conservation de la biodiversité à Saint-Pierre-et-Miquelon, rapport de mission dans l’archipel du 15 au 29 juillet 2006, annexe 3, ministère de l’Écologie et du Développement durable et université Paul-Verlaine (Metz) : 29-32.
Noble V. & Baret J., 2021. Catalogue des végétations du département des Bouches-du-Rhône. Conservatoire botanique national méditerranéen de Porquerolles, à paraître.
Nordhagen R., 1923. Planteveksten langs dovrebanen litt om dyrelivet langs dovrebanen. Særtryk av turistforeningens aarbok : 9-55.
Nordhagen R., 1954. Studies on the vegetation of salt and brackish marshes in Finmark (Norway). Vegetatio 5 : 381-394.
Paradis G. & Lorenzoni C., 1999. Description dans un but conservatoire des stations corses de l’espèce rare Cressa cretica L. (Convolvulaceae). Journal de botanique de la Société botanique de France 9 : 5-34.
Peinado M., Alcaraz F. & Delgadillo J., 1995. Syntaxonomy of some halophilous communities of North and Central America. Phytocoenologia 25 (1) : 23-31.
Quézel P., 1965. La végétation du Sahara, du Tchad à la Mauritanie. Geobotanica Selecta II : 1-333.
Reyes-Betancort J.A., Padrón Mederos M.A., Rosana Guma I., Santos Guerra A. & Navarro Déniz J., 2009. Sobre la presencia de la clase Thero-Salicornietea en las Islas Canarias. Lazaroa 30 : 65-71.
Rivas Goday S. (et collaboration Borja Carbonell J., Monasterio A., Galiano E.F. & Rivas-Martínez S.), 1955 (publié 1956). Aportaciones a la fitosociología hispánica (nota 1). Anales del Instituto Botánico A.J. Cavanilles 13 : 335-422.
Rivas-Martínez S., 1984. Vegetatio Hispaniae, notula VI. Stvdia Botanica 3 : 7-16.
Rivas-Martínez S. & Costa M., 1976. Datos sobre la vegetación halófila de La Mancha (España). Colloques phytosociologiques IV, La végétation des vases salées : 81-97.
Rivas-Martínez S., Costa M., Castroviejo S. & Valdés E., 1980. La vegetación de Doñana (Huelva, España). Lazaroa 2 : 5-190.
Rivas-Martínez S., Wildpret de la Torre W., del Arco Aguilar M., Rodríguez O., Pérez de Paz P.L., García Gallo A., Acebes Ginovés J.R., Díaz González T.E. & Fernández-González F., 1993. Las comunidades vegetales de la isla de Tenerife (Islas Canarias). Itinera Geobotanica 7 : 169-374.
Rønning O.I., 1979. Svalbards Flora. Norsk Polarinstitutt, Oslo, 128 p.
Schnell R., 1977. Flore et végétation de l’Afrique tropicale, 2. Gaulthier-Villars, Paris, 375 p.
Šeljag-Sosonko Ju.R. & Solomacha V., 1987. Novi syntaksony galofilnoj roslynnosti Ukrainy. Ukrayins’kyi botanichnyi zhurnal 44 (6) : 13-17.
Sergienko L., 2013. Salt marsh flora and vegetation of the Russian Arctic coasts. Czech Polar Report 3 : 30-37.
Sivim. Sistema de Investigación sobre la vegetación ibérica y macaronésica, www.sivim.info.
Slavnić S., 1948. Slaninska vegetacija Vojvodine. Arhiva za poljoprivedne nauke i tehniku 3 : 1-80.
Šmarda J., 1952. Příspěvek k poznání fytocenos slaných půd na jz. Slovensku. Preslia, Praha 24 : 95-104.
Soó R. (von), 1927. Geobotanische Monographie von Kolozsvár (Klausenburg), I. A Debreceni Tisza István Tudományos Társaság Honismetetö Bizottságának 15-16 :1-151.
Soó R. (von), 1930. A modern növényföldrajz problémái, irányai és irodalma. A növényszociológiai Magyarországon. A Magyar Biológiái Kutatóintézet Munkái 3 : 1-51.
Soó R. (von), 1957. Systematische Übersicht der pannonischen Pflanzengesellschaften, I. Acta Botanica Academiae Scientiarum Hungaricae 3 : 316-373.
Ştefan N., Sârbu I. & Oprea A., 2008. Phytocoenological contributions to the vegetation of Moldavia (Romania). Romanian Journal of Biology, Plant Biology 53 (1) : 39-45.
Stešević D., Küzmič F., Milanović Đ., Stanišić-Vujačić M. & Šilc U., 2019. Coastal sand dune vegeation of Velika plaža. Acta Botanica Croatica 79 (1) : 43-54.
Tadros T.M., 1953-54. A phytosociological study of halophilous communities from Mareotis (Egypt). Vegetatio IV : 101-124.
Taffetani F. & Biondi E., 1992. La vegetazione del littorale molisano pugliese tra le foci dei fiumi Biferno e Fortore (Adriatico centro-meridionale). Colloques phytosociologiques XVIII, Phytosociologie littorale et taxonomie : 323-350.
Taylor R.J., 1981. Shoreline vegetaton of the Arctic Alaska coast. Arctic 34 : 37-42.
Thannheiser D., 1974. Beobachtungen zur Küstenvegetation der Varanger-Halbinsel (Nord-Norwegen). Polarforschung 44 (2) : 148-159.
Thannheiser D., 1975. Beobachtungen zur Küstenvegetation auf dem westlichen kanadischen Arktis-Archipel. Polarforschung 45 : 1-16.
Thannheiser D., 1987. Die Pflanzengesellschaften der islandischen Salzwiese. Acta Botanica Islandica 9 : 35-60.
Thannheiser D. & Hofmann W., 1977. Pflanzengesellschaften am Meeresstrand im Kongs- und Krossfjord (West-Spizbergen). Documents phytosociologiques, NS, I : 297-303.
Theurillat J.-P., Willner W., Fernández-González F., Bültmann H., Čarni A., Gigante D., Mucina L. & Weber H., 2021. International Code of Phytosociological Nomenclature, 4th version. Applied Vegetation Science, https://doi.org/10.1111/avsc.12491.
Tison J.-M. & de Foucault B., 2014. Flora Gallica, Flore de France. Biotope, Mèze, xx + 1196 p.
Tüxen R., 1937. Die Pflanzengesellschaften Nordwestdeutschland. Mitteilungen der Floristisch-soziologischen Arbeisgemeinschaft in Niedersachsen 3 : 1-170.
Tüxen R. & Oberdorfer E., 1958. Eurosibirische Phanerogamen-Gesellschaften Spaniens. Veröffentlichungen des geobotanischen Institutes der E.T.H., Stiftung Rübel, in Zürich 32 (2) : 1-328.
Tyler G., 1980. Classification of Schoenus nigricans communities in south and south-east Sweden. Vegetatio 41 (2) : 69-84.
Tzonev R., Lysenko T., Gussev C. & Zhelev P., 2008. The halophytic vegetation in south-east Bulgaria and along the Black Sea coast. Hacquetia 7 (2) : 95-121.
Vanden Berghen C., 1994. Un groupement végétal halo-nitrophile à Puccinellia distans le long de nos routes. Les Naturalistes belges 75 : 41-46.
Vevle O., 1985. The salt marsh vegetation at Vinjekilen, Bamble, SE Norway, with special reference to the Puccinellietum maritimae. Vegetatio 61 : 55-63.
Vicherek J., 1973. Die Pflanzengesellschaften der Halophyten- und Subhalophytenvegetation der Tschechoslowakei. Vegetace ČSSR A 5 : 1-200.
Vlieger J., 1938. Plantensociologisch aanteekeningen in Oostelijk Zeeuwsch-Vlanderen. Nederlandsch kruidkundig archief, serie 3, 48 : 35-43.
Warming E., 1906. Dansk Plantevaekst. I – Strandvegetation. Gyldendalske Boghandel Nordisk Forlag.
Wendelberger G., 1943. Die Salzpflanzengesellschaften des Neusiedler Sees. Wiener botanische Zeitschrift 92 : 124-144.
Zahran M.A., El-Amier Y.A. & Shawky R.A., 2016. Natural vegetation of the Egyptian deserts: ecology and economic potentialities. Journal of Environmental Sciences 45 (3-4) : 269-282.
Zamfirescu O., 2011. Vegetation aspects of some habitats with Vipera ursinii from Sărăturile levee (Danube delta). Analele ştiinţifice ale Universităţii « Al. I. Cuza » Iaşi LVII (1), Biologie vegetală : 65-71.
Remerciements
Merci à Zora Dajić Stevanović (université de Belgrade, Serbie) et Nenad Jasprica (université de Dubrovnik, Croatie) pour l’aide à la recherche de publications difficiles à trouver en France, à V. Gaudillat (cellule Habitats, UMS 2006 Patrimoine naturel, MNHN), à O. Argagnon, L. Sirven et C. Gritti pour leur relecture, à F. Le Driant (FloreAlpes.com) pour l’autorisation d’utiliser deux de ses magnifiques photos.